白磷、红磷都是可燃物,都可以在一定条件下燃烧。以下是利用它们的可燃性进行的三个实验,请分别回答问题
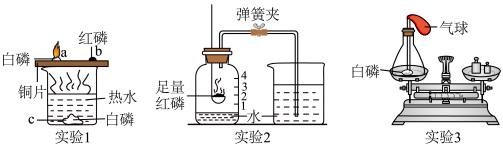
(1)通过实验1可以探究燃烧的条件。烧杯中放有热水,a、b、c处分别放有药品,实验中只有a处的白磷燃烧。a与c对比;a与b对比,说明燃烧需要的条件是可燃物与___________ 接触和__________ 。
(2)通过实验2可以测定________ 。待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到__________ 的现象时,可达到该实验目的。
(3)通过实验3可以验证质量守恒定律。实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平保持平衡。整个实验过程中气球会出现的现象是___________ 。
(4)综合分析上述三个实验,以下说法正确的是________ 。(填①~⑥序号)
①实验1中的热水只起隔绝空气的作用
②实验2中红磷可以换成木炭
③实验2若未达到实验目的,可能是由于装置气密性不好
④实验3中的气球起到了平衡瓶内外气体压强的作用
⑤实验3中的气球作用是收集产生的气体
⑥实验3锥形瓶内事先放少量细沙的作用是防止瓶底炸裂

(1)通过实验1可以探究燃烧的条件。烧杯中放有热水,a、b、c处分别放有药品,实验中只有a处的白磷燃烧。a与c对比;a与b对比,说明燃烧需要的条件是可燃物与
(2)通过实验2可以测定
(3)通过实验3可以验证质量守恒定律。实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平保持平衡。整个实验过程中气球会出现的现象是
(4)综合分析上述三个实验,以下说法正确的是
①实验1中的热水只起隔绝空气的作用
②实验2中红磷可以换成木炭
③实验2若未达到实验目的,可能是由于装置气密性不好
④实验3中的气球起到了平衡瓶内外气体压强的作用
⑤实验3中的气球作用是收集产生的气体
⑥实验3锥形瓶内事先放少量细沙的作用是防止瓶底炸裂
更新时间:2019-10-05 21:18:39
|
相似题推荐
实验题
|
较难
(0.4)
解题方法
【推荐1】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验 (图 1)。

(1)镁与氧气反应的化学方程式为_________ 。
(2)小明认为根据质量守恒定律,燃烧产物的质量应大于反应物镁条的质量。镁条完全燃烧后,称量发现石棉网上的燃烧产物质量反而比反应前镁条质量小,其主要原因是_________ 。
(3)小红按图 2 装置改进实验,验证了质量守恒定律,却发现产物中还有一些黄色固体。
(提出问题)黄色固体是什么呢?
(查阅资料)①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
(做出猜想)黄色固体为 Mg3N2
(实验探究)
(反思交流)①为什么在发生化学反应前后各物质的质量总和相等?请从微观角度解释。_________
②空气中 N2的含量远大于 O2的含量,而镁条在空气中燃烧生成的 MgO 却远多于Mg3N2,为什么呢?请给出合理的解释_________ 。
(拓展延伸)如果用图 2 装置(气密性良好)和药品(足量)测定空气中氧气含量,该实验所测得的氧气体积分数______ 1/5 (填“大于”、“小于”或“等于”)。

(1)镁与氧气反应的化学方程式为
(2)小明认为根据质量守恒定律,燃烧产物的质量应大于反应物镁条的质量。镁条完全燃烧后,称量发现石棉网上的燃烧产物质量反而比反应前镁条质量小,其主要原因是
(3)小红按图 2 装置改进实验,验证了质量守恒定律,却发现产物中还有一些黄色固体。
(提出问题)黄色固体是什么呢?
(查阅资料)①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水反应生成氨气,氨气能使酚酞溶液变红。
(做出猜想)黄色固体为 Mg3N2
(实验探究)
| 实验操作 | 实验现象及结论 |
如图,取燃烧产物于烧杯 B 中,加入适量水,然后用大烧杯罩住小烧杯 A 和 B | 现象: 结论:燃烧产物中含Mg3N2 |
(反思交流)①为什么在发生化学反应前后各物质的质量总和相等?请从微观角度解释。
②空气中 N2的含量远大于 O2的含量,而镁条在空气中燃烧生成的 MgO 却远多于Mg3N2,为什么呢?请给出合理的解释
(拓展延伸)如果用图 2 装置(气密性良好)和药品(足量)测定空气中氧气含量,该实验所测得的氧气体积分数
您最近一年使用:0次
实验题
|
较难
(0.4)
【推荐2】某校化学兴趣小组同学对质置守恒定律进行实验探究,甲组同学用在空气中燃烧镁带的实验来探究,乙组同学用图二进行探究。回答下列问题:

(1)镁条燃烧时产生的现象是____________ 。甲组同学待镁条燃烧后,称量留在石棉网上固体的质量。发现比反应前镁条的质量要轻,请你分析其中的原因可能是____________ 。经过分析后,该组同学在燃烧的镁条上方罩上罩,使夹持的镁条完全燃烧并使生成物全部收集起来称量,则称得的质量和原镁条质量比____________ (填“相等”或“变大”或“变小”),该反应的化学方程式是 ____________ 。
(2)乙组同学实验现象是:天平____________ (“保持平衡”或“向左偏转”或“向右偏转”),其原因是____________ 。
(3)通过以上两个实验,你获得的启示是__________ 。

(1)镁条燃烧时产生的现象是
(2)乙组同学实验现象是:天平
(3)通过以上两个实验,你获得的启示是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐3】请根据题目要求回答下列问题。

(1)图1为托盘天平,使用托盘天平称物品的正确操作顺序为________ (填序号)。
①调游码 ②放称量纸 ③称量物放左盘 ④调零点 ⑤加质量大的砝码 ⑥加质量小的砝码
A①②③④⑤⑥
B④②③⑤⑥①
C④⑤⑥①②③
(2)通过学习我们知道,在化学变化中物质发生了改变,但质量是否改变了呢?为此某校甲、乙两个兴趣小组对这个问题进行了探究,过程如下:
【提出问题】参加反应的反应物总质量与生成物总质量是否相等?
【实验方案】甲、乙两个兴趣小组分别设计了如图所示的实验。
【进行实验】如图2所示,甲小组把盛有适量NaOH溶液的小试管放入盛有CuSO4溶液的烧杯中,乙小组把盛有适量H2O2溶液的小试管放入盛有MnO2的烧杯中;然后将烧杯放到天平上调至平衡;接着取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,观察天平是否平衡。
【实验现象】反应后,甲小组的天平指针指向刻度盘的__________ (填“左边”“右边”或“中间”),乙小组的天平指针指向刻度盘的右边。
【解释与结论】甲小组的结论为___________ 。化学方程式为___________ 。乙小组的指针偏向右边是因为____________ 。
【实验反思】在验证质量守恒定律时,若利用有气体参加或气体生成的化学反应来进行实验时,在装置方面应做到____________ 。

(1)图1为托盘天平,使用托盘天平称物品的正确操作顺序为
①调游码 ②放称量纸 ③称量物放左盘 ④调零点 ⑤加质量大的砝码 ⑥加质量小的砝码
A①②③④⑤⑥
B④②③⑤⑥①
C④⑤⑥①②③
(2)通过学习我们知道,在化学变化中物质发生了改变,但质量是否改变了呢?为此某校甲、乙两个兴趣小组对这个问题进行了探究,过程如下:
【提出问题】参加反应的反应物总质量与生成物总质量是否相等?
【实验方案】甲、乙两个兴趣小组分别设计了如图所示的实验。
【进行实验】如图2所示,甲小组把盛有适量NaOH溶液的小试管放入盛有CuSO4溶液的烧杯中,乙小组把盛有适量H2O2溶液的小试管放入盛有MnO2的烧杯中;然后将烧杯放到天平上调至平衡;接着取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,观察天平是否平衡。
【实验现象】反应后,甲小组的天平指针指向刻度盘的
【解释与结论】甲小组的结论为
【实验反思】在验证质量守恒定律时,若利用有气体参加或气体生成的化学反应来进行实验时,在装置方面应做到
您最近一年使用:0次
实验题
|
较难
(0.4)
名校
【推荐1】某科学兴趣小组对“测定空气中氧气含量”的实验进行了改进:将数显设备、气体压强传感器 和空气中氧气含量测量装置按下图连接。装置气密性良好,调节右边敞口容器和集气瓶里的水面相平,此时集气瓶内气体的体积为V1。关闭活塞,点燃燃烧匙内的红磷,立即塞紧瓶塞,待火焰熄灭后,过一段时间打开活塞,观察到集气瓶中的水位上升。待集气瓶内的水面不再上升时,集气瓶内的气体体积为V2。然后向右边容器内加入一定量的水至两边水面再次相平,此时集气瓶内的气体体积为V3。在点燃红磷至打开活塞这一过程中,观察到数显设备显示集气瓶内的气体压强 先上升后下降,再趋于稳定

(1)写出红磷燃烧的符号表达式:_______________________ ,红磷燃烧的现象是: _____________________
(2)数显设备显示,开始一段时间集气瓶内气体压强上升,这是因为温度升高导致的气压变化量______ (选填“大于”、“ 等于”或“小于”)氧气量减少导致的气压变化量。
(3)基于数显设备显示的气压变化,“ 过一段时间打开活塞” 中的“ 一段时间” 指的是火焰熄灭后到_____________________ 所经历的时间。
(4)在整个实验过程中,集气瓶中减少的氧气体积为______________________ (选填“V1-V2”,“V1-V3”,“V2-V3”)
(5)思考:本实验导致结果小于 1/5 的原因是_____________________
(6)用红磷测定空气中氧气含量的实验结束后,反应容器内剩下的气体主要是_____________________

(1)写出红磷燃烧的符号表达式:
(2)数显设备显示,开始一段时间集气瓶内气体压强上升,这是因为温度升高导致的气压变化量
(3)基于数显设备显示的气压变化,“ 过一段时间打开活塞” 中的“ 一段时间” 指的是火焰熄灭后到
(4)在整个实验过程中,集气瓶中减少的氧气体积为
(5)思考:本实验导致结果小于 1/5 的原因是
(6)用红磷测定空气中氧气含量的实验结束后,反应容器内剩下的气体主要是
您最近一年使用:0次
实验题
|
较难
(0.4)
名校
【推荐2】“富氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗炼钢等。在2019年年末出现的“新型肺炎”重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质也和“富氧空气”差不多,化学兴趣小组欲混制“富氧空气”并开展相关探究,进行以下实验。
实验一:混制“富氧空气”
(1)用高锰酸钾制取氧气
①写出反应的化学方程式:___________________________________ ;
②仪器C的名称为_______________ ;
③组装发生装置所需的仪器:_____________ (选填标号)。

(2)混制“富氧空气”

如图,用纯氮气及上述实验制取的氧气,混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,气体应从装置中的管____________ (选“a”或“b”)通入,先通入氮气排出120 mL水,再通入氧气排出_____ mL水。
实验二:测定“富氧空气”中氧气的含量
用下图装置测定“富氧空气”中氧气的含量(集气瓶中“富氧空气”体积为100 ml,底部残留少量水,燃烧匙内有足量红磷)。操作如下:

i.往量筒内加入适量水,读出量筒内水的体积为V1 mL;
ii.用电点火装置点燃红磷,充分反应;
iii.打开止水夹,待右侧量筒内液面不再变化时,排出气球中的气体,调节两边液面在同一水 平面上,读出量筒内水的体积为V2 mL。
回答问题:
(3)实验前,检查装置气密性的方法:______________________ ;
(4)操作ii中可观察到现象:______________________________ ;
(5)本次实验测得“富氧空气”中氧气的含量为_____________ (用含V1、V2的式子表示)。
(6)若读取V1时仰视,读取V2时俯视,则测得实验结果_____ (选填“偏大”“偏小”或“无影响”)。
实验三:研究“富氧空气”的应用
通过重油、褐煤在氧气含量不同的空气中燃烧的实验,得到有关数据如下图:

(7)结合图1,说明空气中氧气含量与燃烧产生的温度的关系:_____________________ 。
(8)结合图2,简述减少燃料燃烧尾气污染的措施:________________________________ 。
实验一:混制“富氧空气”
(1)用高锰酸钾制取氧气
①写出反应的化学方程式:
②仪器C的名称为
③组装发生装置所需的仪器:

(2)混制“富氧空气”

如图,用纯氮气及上述实验制取的氧气,混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,气体应从装置中的管
实验二:测定“富氧空气”中氧气的含量
用下图装置测定“富氧空气”中氧气的含量(集气瓶中“富氧空气”体积为100 ml,底部残留少量水,燃烧匙内有足量红磷)。操作如下:

i.往量筒内加入适量水,读出量筒内水的体积为V1 mL;
ii.用电点火装置点燃红磷,充分反应;
iii.打开止水夹,待右侧量筒内液面不再变化时,排出气球中的气体,调节两边液面在同一水 平面上,读出量筒内水的体积为V2 mL。
回答问题:
(3)实验前,检查装置气密性的方法:
(4)操作ii中可观察到现象:
(5)本次实验测得“富氧空气”中氧气的含量为
(6)若读取V1时仰视,读取V2时俯视,则测得实验结果
实验三:研究“富氧空气”的应用
通过重油、褐煤在氧气含量不同的空气中燃烧的实验,得到有关数据如下图:

(7)结合图1,说明空气中氧气含量与燃烧产生的温度的关系:
(8)结合图2,简述减少燃料燃烧尾气污染的措施:
您最近一年使用:0次
实验题
|
较难
(0.4)
名校
【推荐3】探究空气中氧气含量的实验(如图所示),回答下列问题:

(1)甲同学点燃燃烧匙中的红磷,观察到红磷燃烧,放热,并产生大量的_________ ,该反应的文字表达式___________ 。冷却后,打开弹簧夹,出现___________ 的现象。
(2)乙同学用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏小,其原因可能是__________________ 。(要求答出一种)
(3)实验结束后,集气瓶中剩余的气体主要是氮气,且瓶内水面上升到一定高度后不再上升了,由此分析说明,氮气具有的一条性质:________________________________ 。
(4)丙同学探究能否用镁条代替红磷,将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁的粉末。请写出镁在氮气中燃烧反应的文字表达式________________ ,分析后认为________ (填“能”或“不能”)代替红磷,原因是_____________ 。若用镁代替红磷实验,进入瓶中水的体积会________ (填 > 或< 或 =)瓶内空气体积的1/5.
(5)下列有关测定空气中氧气含量实验说法正确的是___________ (填字母).
A.燃烧匙中的红磷越多,水位上升越高
B.本实验可以证明空气含有N2、O2、CO2和稀有气体.
C.选用红磷是因为只能与空气中的氧气反应,且生成物为固体
D.集气瓶中先装入少量水是为了吸收生成物,防止污染空气

(1)甲同学点燃燃烧匙中的红磷,观察到红磷燃烧,放热,并产生大量的
(2)乙同学用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏小,其原因可能是
(3)实验结束后,集气瓶中剩余的气体主要是氮气,且瓶内水面上升到一定高度后不再上升了,由此分析说明,氮气具有的一条性质:
(4)丙同学探究能否用镁条代替红磷,将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁的粉末。请写出镁在氮气中燃烧反应的文字表达式
(5)下列有关测定空气中氧气含量实验说法正确的是
A.燃烧匙中的红磷越多,水位上升越高
B.本实验可以证明空气含有N2、O2、CO2和稀有气体.
C.选用红磷是因为只能与空气中的氧气反应,且生成物为固体
D.集气瓶中先装入少量水是为了吸收生成物,防止污染空气
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐1】燃烧是一种发光、发热的剧烈的化学反应,认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。
(1)物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,另外两个条件分别是______ 、______ 。
(2)如图是验证燃烧条件的实验装置图。

已知木炭是一种可燃物。请验证:木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能发生燃烧(两个条件须分别验证),只有同时具备这两个条件才能发生燃烧。某化学实验小组已经在完成气密性的检查后为你填装好了药品,并在整个装置中充满了氮气。请你继续设计实验步骤完成后续探究,要求实验过程中不得拆、装仪器。
(3)①装置C中发生反应的方程式为______ 。
②装置B在“盖灭酒精灯,待仪器恢复到常温”这一步中的作用是______ 。
③小华同学认为,x处的气体不应直接排放到空气中去,大家经讨论后认为很有道理,你认为其中的道理是______ 。
(1)物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,另外两个条件分别是
(2)如图是验证燃烧条件的实验装置图。

已知木炭是一种可燃物。请验证:木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能发生燃烧(两个条件须分别验证),只有同时具备这两个条件才能发生燃烧。某化学实验小组已经在完成气密性的检查后为你填装好了药品,并在整个装置中充满了氮气。请你继续设计实验步骤完成后续探究,要求实验过程中不得拆、装仪器。
| 步骤 | 操作 | 预计现象及得出的结论 |
| ① | 澄清石灰水未变浑,说明燃烧还需要氧气 | |
| ② | 盖灭酒精灯,待恢复到常温 | / |
| ③ | ||
| ④ | 点燃酒精灯加热,继续通氧气 |
②装置B在“盖灭酒精灯,待仪器恢复到常温”这一步中的作用是
③小华同学认为,x处的气体不应直接排放到空气中去,大家经讨论后认为很有道理,你认为其中的道理是
您最近一年使用:0次
实验题
|
较难
(0.4)
【推荐2】利用表中装置进行下列实验。
(1)实验1:甲中发生反应的化学方程式为_____ ;对比乙和丙中的实验现象,说出本实验欲探究的燃烧条件是_____ 。
(2)实验1:步骤③的现象说明装置内压强减小,压强减小的原因是_____ 。
(3)实验2:甲中发生反应的化学方程式为_____ ;打开K1,乙中的现象是_____ 。
| 实验装置 | 实验1 | 实验2 |
 | ①甲的试管中放入少量MnO2,滴管中放入过氧化氢溶液,乙、丙中各放入一小块白磷,依次加入适量的80℃的水。白磷均不燃烧 ②打开K1、K2,将过氧化氢溶液滴入试管中,观察到乙中白磷不燃烧,丙中白磷燃烧 ③一段时间后,丙中导管内液面上升 | ①关闭K1,打开K2,甲的试管中充满CO2,滴管中放入浓NaOH溶液;乙试管中放入足量的铁粉,丙中放入约半试管的稀盐酸 ②将浓NaOH溶液滴入甲试管中,一段时间后,打开K1 |
(2)实验1:步骤③的现象说明装置内压强减小,压强减小的原因是
(3)实验2:甲中发生反应的化学方程式为
您最近一年使用:0次
实验题
|
较难
(0.4)
【推荐3】某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验。
[实验一](已知:白磷的着火点为40°C,白磷不溶于水也不与水反应)
(1)请写出白磷燃烧的化学方程式_________ ;
(2)对比步骤3和4的现象可知,可燃物燃烧的条件是________ ;
(3)待装置冷却--段时间后,打开K2如果观察到________ ;说明空气中氧气的体积约占1/5。
[实验二]
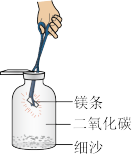
(1)按图实验(集气瓶底部有少量沙子)可观察到:镁条在二氧化碳气体中剧烈燃烧,集气瓶内部有黑色的碳和白色固体氧化镁生成。请写出反应的方程式________ ;此反应中碳元素的化合价如何变化:____ 。
(2) [查阅资料]纳米铁粉在空气中会自燃。
“铁丝在空气中很难燃烧,纳米铁粉却可以在空气中自燃”,你对燃烧的条件有了哪些新的认识:________ 。
| 实验装置 | 实验步骤及现象 |
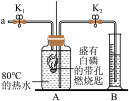 | 步骤1:检验装置的气密性,气密性良好 步骤2:将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧。 步骤3:向A瓶中加满80°C热水,塞紧瓶塞,白磷不燃烧。 步骤4:打开K1、K2,从A口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2,此时进入量筒B中水的体积为200mL ,观察到A瓶中的白磷燃烧。 |
(1)请写出白磷燃烧的化学方程式
(2)对比步骤3和4的现象可知,可燃物燃烧的条件是
(3)待装置冷却--段时间后,打开K2如果观察到
[实验二]

(1)按图实验(集气瓶底部有少量沙子)可观察到:镁条在二氧化碳气体中剧烈燃烧,集气瓶内部有黑色的碳和白色固体氧化镁生成。请写出反应的方程式
(2) [查阅资料]纳米铁粉在空气中会自燃。
“铁丝在空气中很难燃烧,纳米铁粉却可以在空气中自燃”,你对燃烧的条件有了哪些新的认识:
您最近一年使用:0次



