解题方法
1 . 下列实验方案无法达到实验目的的一项是
| 选项 | 实验目的 | 实验方案 |
| A | 把pH=10的溶液变成pH=4的溶液 | 加入过量的水或者过量的稀盐酸 |
| B | 除去ZnSO4溶液中的CuSO4溶液 | 加入过量锌粉,充分反应后过滤 |
| C | 除去CO中的CO2 | 把气体通入足量NaOH溶液中,充分反应后干燥 |
| D | 鉴别Fe粉、CuO粉末、木炭粉 | 分别取样,加入足量稀硫酸,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023·新疆·模拟预测
解题方法
2 . 如图是实验室模拟工业上用大理石(含少量Fe2O3和SiO2)为原料提纯碳酸钙的实验流程,请回答下列问题:
已知:①SiO2不溶于水也不溶于酸
②氨水呈碱性,与盐酸反应的化学方程式为:NH3•H2O+HCl=NH4Cl+H2O

(1)稀盐酸不能用稀硫酸代替,原因是_______ 。
(2)操作a中需要用到的玻璃仪器有烧杯、玻璃棒和_______ 。
(3)写出滤液A中加氨水生成Fe(OH)3的化学方程式_______ 。
(4)滤液B中加入试剂X,恰好完全反应,若滤液C中只含有两种溶质,则试剂X的化学式为_______ 。
已知:①SiO2不溶于水也不溶于酸
②氨水呈碱性,与盐酸反应的化学方程式为:NH3•H2O+HCl=NH4Cl+H2O

(1)稀盐酸不能用稀硫酸代替,原因是
(2)操作a中需要用到的玻璃仪器有烧杯、玻璃棒和
(3)写出滤液A中加氨水生成Fe(OH)3的化学方程式
(4)滤液B中加入试剂X,恰好完全反应,若滤液C中只含有两种溶质,则试剂X的化学式为
您最近一年使用:0次
名校
解题方法
3 . 氯化钾样品中含有少量氯化钙、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作(注意事项:①所加试剂必须过量;②过量试剂必须除去;③不能引入新的杂质)。
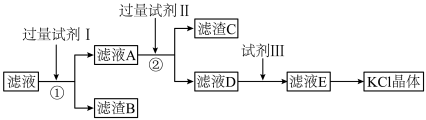
(1)写出滤渣B的化学式______ 。
(2)②中所加试剂II是______ (填化学式),滤渣C中有_______ 种固体;
(3)滤液E中除K+和Cl-外,还含有的离子是______ (填离子符号);
(4)由所得KC1溶液制成氯化钾晶体的操作_____ 。
(5)如果称得加入的样品质量为3g,实验得到的氯化钾晶体质量为3.1g,则下列分析不正确的是______(填字母)。

(1)写出滤渣B的化学式
(2)②中所加试剂II是
(3)滤液E中除K+和Cl-外,还含有的离子是
(4)由所得KC1溶液制成氯化钾晶体的操作
(5)如果称得加入的样品质量为3g,实验得到的氯化钾晶体质量为3.1g,则下列分析不正确的是______(填字母)。
| A.蒸发过程中可能有水分没有蒸干 |
| B.溶解操作中氯化钾没有完全溶解 |
| C.除杂过程中有氯化钾生成 |
您最近一年使用:0次
解题方法
4 . 某氯化钠样品中混有少量氯化钡,小丽同学为了除去氯化钠中混有的氯化钡,她进行了如下实验,请你与她一道完成。
(1)取少量该混合物样品于烧杯中,然后向烧杯中加入足量的水,为了加速溶解,使样品溶解形成溶液,她可采取的简洁方法是_____________________ 。
(2)取少量溶液于试管中,向其中滴入少量无色某溶液,产生白色沉淀,她由此推断加入的无色溶液为硫酸钠溶液,发生的化学方程式为___________________ ,若你对她的推断有异议,请你表达提出异议的原因是______ (用化学方程式作答)。
(3)为了探究所加溶液为何种溶液,请你设计完成相应的探究实验。
(1)取少量该混合物样品于烧杯中,然后向烧杯中加入足量的水,为了加速溶解,使样品溶解形成溶液,她可采取的简洁方法是
(2)取少量溶液于试管中,向其中滴入少量无色某溶液,产生白色沉淀,她由此推断加入的无色溶液为硫酸钠溶液,发生的化学方程式为
(3)为了探究所加溶液为何种溶液,请你设计完成相应的探究实验。
| 实验步骤 | 实验现象 | 实验结论 |
您最近一年使用:0次
22-23九年级上·全国·课时练习
解题方法
5 . 下列各组混合物可用过滤法进行分离的是
| A.铁粉和铜粉 | B.食盐和泥沙 |
| C.酒精和水 | D.食盐水 |
您最近一年使用:0次
6 . 草木灰是农家肥料,主要含钾盐。请回答相关问题。
【分离提纯】Ⅰ.在烧杯里放一定量的草木灰,加入水,同时用玻璃棒搅拌。
Ⅱ.把烧杯中的草木灰连同浸出液一起过滤。
Ⅲ.把滤液倒入蒸发皿里,加热,用玻璃棒搅拌。当蒸发到___________ 时,停止加热。
【定性分析】取分离提纯所得的晶体进行实验。
【实验反思】
(1)实验一中发生反应 的化学方程式有___________ 。
(2)为证明实验二中的溶液呈碱性是由CO32-引起的,再向红色溶液中加入__________ ,当看到____________________________ 时即可证明。
(3)草木灰不能与下列化肥中的________ (填“序号”)混合使用。
A.CO(NH2)2 B.KNO3 C.NH4Cl D.磷矿粉
【定量分析】测定草木灰中碳酸钾的含量(假设草木灰中的杂质不含碳酸根,不与酸反应)
测定原理:利用图一中的A装置将草木灰中的碳酸钾转化成二氧化碳,通过测定二氧化碳的质量或体积,计算出草木灰中的碳酸钾的质量。

(4)实验前,向图一A的分液漏斗中加入水,用弹簧夹夹住A、B间的橡胶管……。这样做的目的是_______ ;装置B的作用是_______ 。
(5)图一装置中欲测定生成的二氧化碳的质量,需测定的数据是___________ 。
(6)图二中的D装置可用于测定生成的二氧化碳的体积,测定时____________ (“需要”、“不需要”)等A、B装置中的空气排尽时再连接。
(7)用图一测出的碳酸钾的质量分数偏小,可能的原因是___________ 。
【分离提纯】Ⅰ.在烧杯里放一定量的草木灰,加入水,同时用玻璃棒搅拌。
Ⅱ.把烧杯中的草木灰连同浸出液一起过滤。
Ⅲ.把滤液倒入蒸发皿里,加热,用玻璃棒搅拌。当蒸发到
【定性分析】取分离提纯所得的晶体进行实验。
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取样,加入足量的稀盐酸,将生成的气体通入澄清的石灰水 | 该晶体中含有碳酸根离子 | |
| 实验二 | 取样,溶于水滴入 | 溶液变红色 | 溶液呈碱性 |
(1)实验一中
(2)为证明实验二中的溶液呈碱性是由CO32-引起的,再向红色溶液中加入
(3)草木灰不能与下列化肥中的
A.CO(NH2)2 B.KNO3 C.NH4Cl D.磷矿粉
【定量分析】测定草木灰中碳酸钾的含量(假设草木灰中的杂质不含碳酸根,不与酸反应)
测定原理:利用图一中的A装置将草木灰中的碳酸钾转化成二氧化碳,通过测定二氧化碳的质量或体积,计算出草木灰中的碳酸钾的质量。

(4)实验前,向图一A的分液漏斗中加入水,用弹簧夹夹住A、B间的橡胶管……。这样做的目的是
(5)图一装置中欲测定生成的二氧化碳的质量,需测定的数据是
(6)图二中的D装置可用于测定生成的二氧化碳的体积,测定时
(7)用图一测出的碳酸钾的质量分数偏小,可能的原因是
您最近一年使用:0次
2022-12-27更新
|
216次组卷
|
2卷引用:江苏省南通市海安城南实验中学2022-2023学年九年级上学期期末复习化学试题2
解题方法
7 . 回答下列问题。
(1)为分离CO和CO2混合气体,某同学设计了如图的实验流程,请回答有关问题。
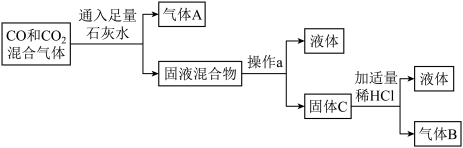
①气体A的化学式是_______ ,气体B的化学式是_______ 。
②混合气体通入石灰水发生反应的化学方程式是_______ 。
③判断加入的稀盐酸为“适量”的现象是_______ 。
(2)在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水,广泛应用于实际生产和生活中,在工业上,制取氯气的主要工艺流程如图:
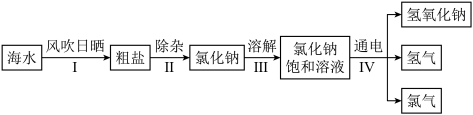
①步骤Ⅰ利用风吹日晒可以从海水中提取租盐,该过程主要发生_______ (选填“物理”或“化学”)变化。
②步骤Ⅱ若要除去食盐水中混有的少量泥沙,可选择的操作方法是_______ ,在实验室中该操作所需要的玻璃仪器有烧杯、玻璃棒、_______ 。
③请写出步骤Ⅳ发生反应的化学方程式:_______ 。
(1)为分离CO和CO2混合气体,某同学设计了如图的实验流程,请回答有关问题。

①气体A的化学式是
②混合气体通入石灰水发生反应的化学方程式是
③判断加入的稀盐酸为“适量”的现象是
(2)在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水,广泛应用于实际生产和生活中,在工业上,制取氯气的主要工艺流程如图:

①步骤Ⅰ利用风吹日晒可以从海水中提取租盐,该过程主要发生
②步骤Ⅱ若要除去食盐水中混有的少量泥沙,可选择的操作方法是
③请写出步骤Ⅳ发生反应的化学方程式:
您最近一年使用:0次
2022-12-22更新
|
263次组卷
|
5卷引用:广东省阳江市江城区2022-2023学年九年级上学期期末化学试题
广东省阳江市江城区2022-2023学年九年级上学期期末化学试题2023口袋书系列-专题01 化学用语-知识手册-提高练习广东省阳江市2022-2023学年九年级上学期期末化学试题广东省阳江市江城区2022-2023学年九年级上学期期末化学试题(已下线)专题11 物质鉴别、除杂、推断与流程题-【好题汇编】备战2023-2024学年九年级化学上学期期末真题分类汇编(广东专用)
解题方法
8 . 分离和提纯是获得物质的重要方法,下列实验操作能达到实验目的的是
| A.除去二氧化碳气体中的一氧化碳—通入适量氧气并点燃 |
| B.除去氧化钙中的氯化钙—加适量的水溶解、过滤、洗涤、干燥 |
| C.除去铜粉中的镁粉—加入过量的稀盐酸,充分反应后过滤、洗涤、干燥 |
| D.除去氯化钾固体中的氯酸钾—加入少量二氧化锰,加热 |
您最近一年使用:0次
解题方法
9 . 下列各组物质,能用过滤方法分离的是
| A.食盐和沙子 | B.食用油和水 |
| C.酒精和食醋 | D.铁粉和铜粉 |
您最近一年使用:0次
解题方法
10 . 氯化钠既是一种重要的调味品,又是重要的化工原料,工业上以粗盐(主要成分 NaCl,含有少量MgCl2、CaCl2、Na2SO4和泥沙)为原料制备较纯的NaCl晶体的流程如图。
回答下列问题:

(1)粗盐加水“溶解”时,需要进行搅拌,目的是_______ 。
(2)Ba(OH)2溶液与“滤液1”中的______ (填离子符号)生成白色沉淀。
(3)“滤液2”的pH______ 7(填“>”、“<”或“=”)。
(4)加入过量Na2CO3溶液的目的是________ 。
回答下列问题:

(1)粗盐加水“溶解”时,需要进行搅拌,目的是
(2)Ba(OH)2溶液与“滤液1”中的
(3)“滤液2”的pH
(4)加入过量Na2CO3溶液的目的是
您最近一年使用:0次



