解题方法
1 . 学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究。
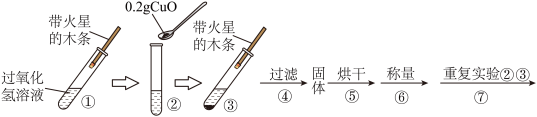
【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后___________ 。
【实验】用天平称量0.2g CuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:
(1)填写下表:
(2)步骤①的目的是___________ ;步骤⑦的目的是______________ ;
(3)步骤⑥需用到的主要实验仪器是___________ ;
(4)过氧化氢能被CuO催化分解放出O2的符号表达式为___________ ;
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是____________ (写一种)。

【猜想】Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后
【实验】用天平称量0.2g CuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:
(1)填写下表:
| 步骤③的现象 | 步骤⑥的现象 | 步骤⑦的现象 | 结论 |
| 带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立 |
(3)步骤⑥需用到的主要实验仪器是
(4)过氧化氢能被CuO催化分解放出O2的符号表达式为
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是
您最近一年使用:0次
解题方法
2 . 小明同学探究质量守恒定律:
【查阅资料】①铁和硫酸铜反应生成铜和硫酸亚铁;
②碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳。
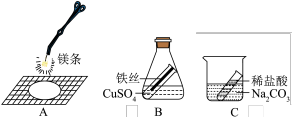
(1)图A中,镁带完全燃烧后,生成的氧化镁比镁条的质量大,反应前后固体质量不相等的原因是______ 。
(2)写出图B实验发生的化学反应方程式______ 。
(3)用图C做实验,完全反应后发现指针偏______ (填“左”或“右”),如何改进实验装置______ 。
【查阅资料】①铁和硫酸铜反应生成铜和硫酸亚铁;
②碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳。

(1)图A中,镁带完全燃烧后,生成的氧化镁比镁条的质量大,反应前后固体质量不相等的原因是
(2)写出图B实验发生的化学反应方程式
(3)用图C做实验,完全反应后发现指针偏
您最近一年使用:0次
2022-07-28更新
|
61次组卷
|
2卷引用:内蒙古呼伦贝尔市2021-2022学年九年级上学期期末化学试题
解题方法
3 . 如图所示,在试管中的滤纸条上A、B、C三处各滴上一滴无色酚酞,再向试管口的棉花团上滴一些浓氨水.
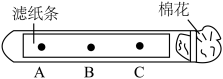
(1)实验中,可以观察到A、B、C三处的酚酞溶液由__ (填A、B、C或C、B、A)顺序先后变成__ 色。
(2)实验中,往往在试管下放一张白纸,白纸的作用是__ 。

(1)实验中,可以观察到A、B、C三处的酚酞溶液由
(2)实验中,往往在试管下放一张白纸,白纸的作用是
您最近一年使用:0次
2022-06-10更新
|
33次组卷
|
2卷引用:2022年内蒙古呼伦贝尔市阿荣旗中考一模化学试题
解题方法
4 . 在学习常见的酸和碱的知识后,某兴趣小组对物质的性质进行相关探究。
【探究一】氢氧化钠与二氧化碳反应。
CO2通入NaOH溶液中无明显现象,CO2与NaOH溶液能否发生化学反应呢?小组同学对此进行探究。
【查阅资料】
常温下,NaOH、Na2CO3在水、乙醇中的溶解性如下表所示:
【实验一】
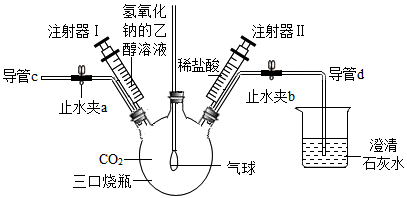
小组同学设计了多角度验证CO2与NaOH溶液反应的实验,如图所示(装置已连接好,气密性良好,止水夹a和b已关闭,部分仪器已略去)。
【温馨提示】
CO2与乙醇不反应,本实验条件下CO2在乙醇中的溶解忽略不计。
(1)把注射器I中氢氧化钠的乙醇溶液注入充满CO2的三口烧瓶中,轻轻振荡,观察到的现象是___ 。写出该反应的化学方程式:_____ 。
(2)把导管d移出石灰水,打开止水夹a、b,再从导管c端往三口烧瓶中鼓入N2,目的是____ 。过了一段时间后,先把导管d放入澄清石灰水中,接着关闭止水夹a,再把注射器II中的稀盐酸注入三口烧瓶中,观察到三口烧瓶中产生气泡,烧杯中的澄清石灰水变浑浊。此实验从_____ (填“生成物”或“反应物”)角度证明了CO2与NaOH溶液发生了反应。
【探究一】氢氧化钠与二氧化碳反应。
CO2通入NaOH溶液中无明显现象,CO2与NaOH溶液能否发生化学反应呢?小组同学对此进行探究。
【查阅资料】
常温下,NaOH、Na2CO3在水、乙醇中的溶解性如下表所示:
| 氢氧化钠 | 碳酸钠 | |
| 水 | 极易溶 | 易溶 |
| 乙醇 | 易溶 | 微溶 |

【实验一】
小组同学设计了多角度验证CO2与NaOH溶液反应的实验,如图所示(装置已连接好,气密性良好,止水夹a和b已关闭,部分仪器已略去)。
【温馨提示】
CO2与乙醇不反应,本实验条件下CO2在乙醇中的溶解忽略不计。
(1)把注射器I中氢氧化钠的乙醇溶液注入充满CO2的三口烧瓶中,轻轻振荡,观察到的现象是
(2)把导管d移出石灰水,打开止水夹a、b,再从导管c端往三口烧瓶中鼓入N2,目的是
您最近一年使用:0次
5 . 某校化学兴趣小组的同学发现长期露置在空气中的金属M表面会被锈蚀,于是他们一起探究金属M锈蚀的原因。经检测,锈蚀物中除含有M元素外,还含有C、H、O三种元素。
(1)甲同学依据锈蚀物中的组成元素,推测空气中_____ 肯定参加了反应,但不能确定空气中的氧气是否参与反应。为了确认空气中的氧气是否参加反应,设计如图系列实验,你认为其中必须要做的对照实验是_____ (填字号)。

若观察到_____ (填现象),证明氧气参加了反应。
(2)若金属M是铜,铜器据长期露置在空气中会生成绿色铜锈,它的主要成分是碱式碳酸铜(铜Cu2(OH)2CO3)。小组同学欲探究Cu2(OH)2CO3的性质。
查阅资料:①Cu2(OH)2CO3的化学性质与Cu(OH)2和CuCO3混合物的性质相同
②Cu(OH)2受热分解生成CuO和H2O,CuCO3的化学性质和CaCO3相似
③白色CuSO4粉末遇水变蓝色
结合以上信息分析Cu2(OH)2CO3加热分解产物为_____ 。
【实验探究】
为进一步验证Cu2(OH)2CO3受热分解产物,从如图中选择部分装置进行实验。装置的连接顺序为_____ ;实验中可观察到的现象是_____ 。
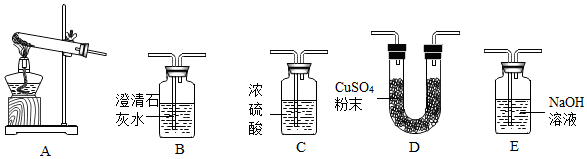
【实验结论】碱式碳酸铜受热易分解。
(1)甲同学依据锈蚀物中的组成元素,推测空气中

若观察到
(2)若金属M是铜,铜器据长期露置在空气中会生成绿色铜锈,它的主要成分是碱式碳酸铜(铜Cu2(OH)2CO3)。小组同学欲探究Cu2(OH)2CO3的性质。
查阅资料:①Cu2(OH)2CO3的化学性质与Cu(OH)2和CuCO3混合物的性质相同
②Cu(OH)2受热分解生成CuO和H2O,CuCO3的化学性质和CaCO3相似
③白色CuSO4粉末遇水变蓝色
结合以上信息分析Cu2(OH)2CO3加热分解产物为
【实验探究】
为进一步验证Cu2(OH)2CO3受热分解产物,从如图中选择部分装置进行实验。装置的连接顺序为

【实验结论】碱式碳酸铜受热易分解。
您最近一年使用:0次
6 . “鱼浮灵”是常用的化学增氧剂,主要成分是过氧碳酸钠(2Na2CO3•3H2O2),溶于水能迅速增加水体溶氧量,提高鱼苗及活鱼运输成活率。某化学兴趣小组对“鱼浮灵”的化学性质、增氧原理进行了探究。
【查阅资料】a.过氧碳酸钠具有碳酸钠和过氧化氢的双重性质,其水溶液中含有Na+、OH-、CO32-、H2O2。
b.Na+不能催化过氧化氢分解。
c.相同温度下,pH相同的溶液,OH-的浓度也相同。
探究一 过氧碳酸钠的化学性质
探究二“鱼浮灵”增氧原理
【提出问题】过氧碳酸钠溶液中的哪种微粒对过氧化氢分解有催化作用?
【猜想假设】猜想一:CO32- 猜想二:OH-猜想三:______________
【实验过程】相同温度下,进行H2O2溶液以及H2O2溶液中分别加Na2CO3、NaOH的实验,测定相同时间内溶液的pH、溶解氧含量(mg/L),数据如下:
【实验结论】对比实验数据,证明猜想_______ 正确。
【反思交流】设计实验2、3的目的是_______ 。
【查阅资料】a.过氧碳酸钠具有碳酸钠和过氧化氢的双重性质,其水溶液中含有Na+、OH-、CO32-、H2O2。
b.Na+不能催化过氧化氢分解。
c.相同温度下,pH相同的溶液,OH-的浓度也相同。
探究一 过氧碳酸钠的化学性质
| 实验步骤 | 实验现象 | 实验解释(化学方程式) |
| 1.取样,溶于水,滴加 | 有白色沉淀生成 | / |
| 2.取样,溶于水,加入二氧化锰粉末 | | |
【提出问题】过氧碳酸钠溶液中的哪种微粒对过氧化氢分解有催化作用?
【猜想假设】猜想一:CO32- 猜想二:OH-猜想三:
【实验过程】相同温度下,进行H2O2溶液以及H2O2溶液中分别加Na2CO3、NaOH的实验,测定相同时间内溶液的pH、溶解氧含量(mg/L),数据如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 试剂 | H2O2 | H2O2+Na2CO3 | H2O2+NaOH | H2O2+NaOH |
| pH | 6.01 | 8.14 | 8.14 | 9.26 |
| 溶解氧 | 6.44 | 9.11 | 9.11 | 10.97 |
【反思交流】设计实验2、3的目的是
您最近一年使用:0次
2019-07-22更新
|
343次组卷
|
3卷引用:2022年内蒙古赤峰市松山区中考二模化学试题
7 . 某校科学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:
①取 只
只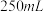 集气瓶,向
集气瓶,向 只集气瓶中分别装入
只集气瓶中分别装入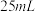 、
、 、
、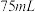 、
、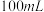 、
、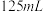 的水,并用毛玻璃片盖住,依次编号为
的水,并用毛玻璃片盖住,依次编号为 、
、 、
、 、
、 、
、 ;
;
②用分解过氧化氢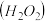 的方法制取氧气,用制取的氧气通过排水法将上述
的方法制取氧气,用制取的氧气通过排水法将上述 号瓶中的水排去;③将带火星的木条依次插入
号瓶中的水排去;③将带火星的木条依次插入 号瓶中,把观察到现象和计算数据,填入下表.
号瓶中,把观察到现象和计算数据,填入下表.
试回答下列问题:
 集气瓶
集气瓶 中氧气的体积分数为
中氧气的体积分数为________ .(空气中氧气的体积分数以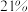 计)
计)
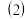 根据以上实验事实,下列说法中正确的是
根据以上实验事实,下列说法中正确的是________ (填写相应的字母).
 .只有在纯氧中才能使带火星的木条复燃
.只有在纯氧中才能使带火星的木条复燃
 .集气瓶中氧气的体积分数
.集气瓶中氧气的体积分数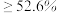 时,带火星的木条就能复燃
时,带火星的木条就能复燃
 .只要有氧气存在就可使带火星的木条复燃.
.只要有氧气存在就可使带火星的木条复燃.
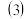 上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈.请你再举一例,将实验内容和实验现象填写在下表中:
上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈.请你再举一例,将实验内容和实验现象填写在下表中:
①取
 只
只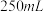 集气瓶,向
集气瓶,向 只集气瓶中分别装入
只集气瓶中分别装入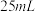 、
、 、
、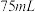 、
、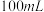 、
、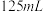 的水,并用毛玻璃片盖住,依次编号为
的水,并用毛玻璃片盖住,依次编号为 、
、 、
、 、
、 、
、 ;
;②用分解过氧化氢
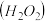 的方法制取氧气,用制取的氧气通过排水法将上述
的方法制取氧气,用制取的氧气通过排水法将上述 号瓶中的水排去;③将带火星的木条依次插入
号瓶中的水排去;③将带火星的木条依次插入 号瓶中,把观察到现象和计算数据,填入下表.
号瓶中,把观察到现象和计算数据,填入下表.| 集气瓶标号 |  |  |  |  |  |
| 集气瓶中氧气的体积分数 |  | 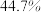 |  | 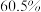 | |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 |
 集气瓶
集气瓶 中氧气的体积分数为
中氧气的体积分数为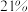 计)
计)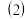 根据以上实验事实,下列说法中正确的是
根据以上实验事实,下列说法中正确的是 .只有在纯氧中才能使带火星的木条复燃
.只有在纯氧中才能使带火星的木条复燃 .集气瓶中氧气的体积分数
.集气瓶中氧气的体积分数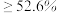 时,带火星的木条就能复燃
时,带火星的木条就能复燃 .只要有氧气存在就可使带火星的木条复燃.
.只要有氧气存在就可使带火星的木条复燃.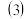 上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈.请你再举一例,将实验内容和实验现象填写在下表中:
上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈.请你再举一例,将实验内容和实验现象填写在下表中:| 实验内容 | 实验现象 | 实验结论 |
| | | 氧气浓度越大,燃烧越剧烈 |
您最近一年使用:0次
2018-09-15更新
|
159次组卷
|
3卷引用:内蒙古赤峰市临西县繁荣中学2018届九年级上学期期中考试化学试题
8 . 下列是初中化学中的一些重要实验,请回答:
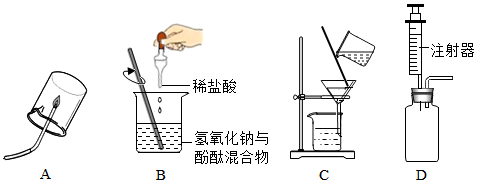
(1)A是氢气或甲烷的燃烧实验,点燃前必须__________ ;
(2)B实验中能够说明盐酸与氢氧化钠发生了反应的现象是__________________ ;
(3)C是除去粗盐中难溶性杂质实验中的过滤操作,其中玻璃棒的作用是____________________ ;
(4)D是用碳酸钠粉末与稀盐酸反应制取二氧化碳的简易装置,此装置的最大优点是__________ .

(1)A是氢气或甲烷的燃烧实验,点燃前必须
(2)B实验中能够说明盐酸与氢氧化钠发生了反应的现象是
(3)C是除去粗盐中难溶性杂质实验中的过滤操作,其中玻璃棒的作用是
(4)D是用碳酸钠粉末与稀盐酸反应制取二氧化碳的简易装置,此装置的最大优点是
您最近一年使用:0次



