解题方法
1 . “科学探究和创新意识”是化学学科的核心素养。经过近一年的学习,化学小组的同学们对化学实验室的物质产生了浓厚的兴趣,于是展开了下列活动探究。
活动一:探究失去标签的物质的成分
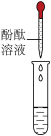
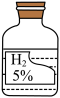
实验室中有一瓶标签受损的无色液体,如图所示。这瓶无色液体是什么呢?实验老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸和蒸馏水中的一种。
【进行实验】
(1)为确定该液体成分,同学们继续进行了如表实验探究:
【归纳总结】通过实验探究,小组同学最终确定该失去标签的溶液是稀硫酸。
活动二:探究酸碱中和反应
(2)在实验老师引导下开展探究活动,同学们将一定量的稀H2SO4。加入盛有NaOH溶液的小烧杯中,充分混合后,未观察到明显现象。请写出该反应的化学方程式:______ 。
【提出问题】反应后溶液中溶质是什么呢?
【假设猜想】
(3)猜想一:溶质有Na2SO4
猜想二:溶质有Na2SO4和H2SO4
猜想三:溶质有______ 。
(4)【实验探究】
【评价反思】
(5)小组同学对方案1提出质疑,认为该方案是错误的。理由是______ 。
【得出结论】通过探究,小组同学一致确定猜想三是正确的。
活动一:探究失去标签的物质的成分
实验室中有一瓶标签受损的无色液体,如图所示。这瓶无色液体是什么呢?实验老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸和蒸馏水中的一种。
【进行实验】
(1)为确定该液体成分,同学们继续进行了如表实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 取该液体适量于试管中,向其中加入少量 | 没有气泡产生 | 该液体不是过氧化氢溶液 |
| 取该液体适量于试管中,向其中加入少量碳酸钠溶液 | 该液体是稀硫酸 |
【归纳总结】通过实验探究,小组同学最终确定该失去标签的溶液是稀硫酸。
活动二:探究酸碱中和反应
(2)在实验老师引导下开展探究活动,同学们将一定量的稀H2SO4。加入盛有NaOH溶液的小烧杯中,充分混合后,未观察到明显现象。请写出该反应的化学方程式:
【提出问题】反应后溶液中溶质是什么呢?
【假设猜想】
(3)猜想一:溶质有Na2SO4
猜想二:溶质有Na2SO4和H2SO4
猜想三:溶质有
(4)【实验探究】
| 实验方案 | 实验现象 | 实验结论 |
| 1.取少量反应后溶液于试管中,向其中加入硝酸钡溶液 | 产生白色沉淀 | 猜想二成立 |
| 2.取少量反应后溶液于试管中,向其中加入氯化铁溶液 | 猜想三成立 |
【评价反思】
(5)小组同学对方案1提出质疑,认为该方案是错误的。理由是
【得出结论】通过探究,小组同学一致确定猜想三是正确的。
您最近一年使用:0次
解题方法
2 . 盐碱地中所含的盐分影响作物的正常生长,对其开发利用是提高农业产能的途径,但也是世界性难题。某化学兴趣小组对盐碱地土壤进行了研究。
【查阅资料】盐碱地的土壤中可能含有的物质有Na2CO3、NaCl、Na2SO4。
【探究一】土壤的酸碱度
(2)经测定,滤液的pH值为8,同学们对当地农民施肥给出了建议,在施加氮肥时,可以选择
【探究二】土壤所含的成分
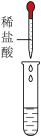
(3)小明取少量滤液a,加入适量稀盐酸,观察到有气泡产生,证明土壤中含有___________ 。
(4)小青取少量滤液a,加入适量BaCl2溶液,观察到有白色沉淀生成。
他得出结论:滤液a中含有Na2SO4。
同学们认为小青的结论不严谨,理由是___________ (用化学方程式表示)。
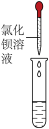
【设计实验】为进一步探究滤液a的成分,小季进行了如图所示的实验。___________ 。
【得出结论】该地块的土壤中除了含有Na2CO3外,还含有NaCl和Na2SO4
【反思交流】
(6)同学们认为小季的实验无法得出该土壤中含有NaCl,其原因是___________ 。
【查阅资料】盐碱地的土壤中可能含有的物质有Na2CO3、NaCl、Na2SO4。
【探究一】土壤的酸碱度
实验步骤: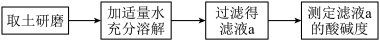
| A.紫色石蕊溶液 | B.无色酚酞溶液 | C.pH试纸 |
(2)经测定,滤液的pH值为8,同学们对当地农民施肥给出了建议,在施加氮肥时,可以选择
| A.NH4Cl | B.CO(NH2)2 | C.NH4HCO3 |
【探究二】土壤所含的成分
(3)小明取少量滤液a,加入适量稀盐酸,观察到有气泡产生,证明土壤中含有
(4)小青取少量滤液a,加入适量BaCl2溶液,观察到有白色沉淀生成。
他得出结论:滤液a中含有Na2SO4。
同学们认为小青的结论不严谨,理由是
【设计实验】为进一步探究滤液a的成分,小季进行了如图所示的实验。
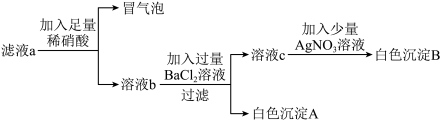
【得出结论】该地块的土壤中除了含有Na2CO3外,还含有NaCl和Na2SO4
【反思交流】
(6)同学们认为小季的实验无法得出该土壤中含有NaCl,其原因是
您最近一年使用:0次
名校
解题方法
3 . 化学课上,同学们设计了如图装置探究CO2的制法和性质,并展开了拓展学习与探究。
Ⅰ、检查装置气密性。
Ⅱ、在制气管A中加入石灰石颗粒,并推压注射器活塞加入适量稀盐酸,将产生的气体通入试管B中,溶液无明显变化。
Ⅲ、当制气管A中的反应停止一段时间后,可观察到试管B中溶液全部倒吸进入制气管A中,一段时间后,产生大量气泡,最终变为无色澄清溶液。
同学们对相关问题分组展开如下探究。
(1)
【反思交流】
(2)实验步骤Ⅱ中产生气体的化学反应方程式为______ 。
(3)实验步骤Ⅲ中溶液全部倒吸的现象______ (填“能”或“不能”)证明NaOH与CO2发生了反应。
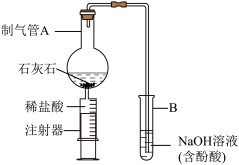
Ⅰ、检查装置气密性。
Ⅱ、在制气管A中加入石灰石颗粒,并推压注射器活塞加入适量稀盐酸,将产生的气体通入试管B中,溶液无明显变化。
Ⅲ、当制气管A中的反应停止一段时间后,可观察到试管B中溶液全部倒吸进入制气管A中,一段时间后,产生大量气泡,最终变为无色澄清溶液。
同学们对相关问题分组展开如下探究。
| 探究环节 | 甲组的探究 | 乙组的探究 |
| 【提出问题】 | 步骤Ⅱ,试管B中NaOH溶液是否与CO2发生了反应? | 步骤Ⅲ,制气管A中所得无色澄清溶液的溶质是什么? |
| 【做出猜想】 | 猜想一:NaOH未反应 猜想二:NaOH部分反应 猜想三:NaOH全部反应 | 猜想二:NaCl、CaCl2 猜想二:NaCl、CaCl2、HCl |
(1)
| 探究环节 | 甲组的探究 | 乙组的探究 |
| 【实验验证】 | 甲同学取少量B中溶液于试管中,向其中滴加过量BaCl2溶液,若观察到 | 取少量实验结束后A中的溶液,加入到盛有少量铁粉的试管中,观察到有气泡产生,固体逐渐减少,溶液由无色变为 |
【反思交流】
(2)实验步骤Ⅱ中产生气体的化学反应方程式为
(3)实验步骤Ⅲ中溶液全部倒吸的现象
您最近一年使用:0次
4 . 中国古代采用卓筒井汲取地下卤水,卤水主要含氯化钠和氯化钾。下表是氯化钠、氯化钾的溶解度数据。
(1)40℃时,氯化钾的溶解度是________ 。
(2)20℃时,取40g氯化钠,分两次每次加入50g水。___ g;要使丙中剩余固体溶完,应至少再加入水_______ g(保留一位小数)。
(3)某地卓筒井获得的卤水中约含10%氯化钠、1%氯化钾以及其他少量的可溶性杂质,还有少量的泥沙。制作井盐流程为:钻井(修治井)—汲卤——晒卤——滤卤——煎盐。“晒卤”将卤水中氯化钠浓度提升至约20%,“滤卤”是将泥沙过滤除去。请说出“晒卤”先于“滤卤、煎盐”的主要作用是___________ 。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度(g/100g水) | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 氯化钾 | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |
(1)40℃时,氯化钾的溶解度是
(2)20℃时,取40g氯化钠,分两次每次加入50g水。
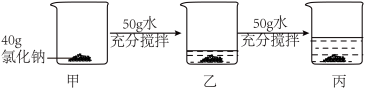
(3)某地卓筒井获得的卤水中约含10%氯化钠、1%氯化钾以及其他少量的可溶性杂质,还有少量的泥沙。制作井盐流程为:钻井(修治井)—汲卤——晒卤——滤卤——煎盐。“晒卤”将卤水中氯化钠浓度提升至约20%,“滤卤”是将泥沙过滤除去。请说出“晒卤”先于“滤卤、煎盐”的主要作用是
您最近一年使用:0次
名校
解题方法
5 . 对于金属材料,我们应该从多角度了解。
Ⅰ.金属冶炼。《大治赋》记载由磁化铜矿(主要成分 ,杂质不与酸反应,也不溶于水)制取
,杂质不与酸反应,也不溶于水)制取 溶液,再用铁片浸取得到铜的方法.磁化铜矿中
溶液,再用铁片浸取得到铜的方法.磁化铜矿中 转化的流程如图:
转化的流程如图:______ 。
(2)写出滤液中加入Fe后一定发生反应的化学方程式______ 。
Ⅱ.金属的活动性。为比较金属M与Fe、Zn的金属活动性强弱,实验小组设计了如下图1装置(金属片均足量)的实验。待甲中充分反应后打开 ,使甲中溶液全部进入乙中,乙中无明显现象,打开
,使甲中溶液全部进入乙中,乙中无明显现象,打开 使乙中溶液全部进入丙中,观察到Zn片表面变黑。回答下列问题:
使乙中溶液全部进入丙中,观察到Zn片表面变黑。回答下列问题:
(4)如图2所示,向一定量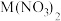 溶液中加入铁和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙。已知
溶液中加入铁和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙。已知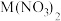 溶液呈无色。若溶液甲是无色,则溶液甲一定含有的金属阳离子是
溶液呈无色。若溶液甲是无色,则溶液甲一定含有的金属阳离子是______ 。(填离子符号)
Ⅰ.金属冶炼。《大治赋》记载由磁化铜矿(主要成分
 ,杂质不与酸反应,也不溶于水)制取
,杂质不与酸反应,也不溶于水)制取 溶液,再用铁片浸取得到铜的方法.磁化铜矿中
溶液,再用铁片浸取得到铜的方法.磁化铜矿中 转化的流程如图:
转化的流程如图: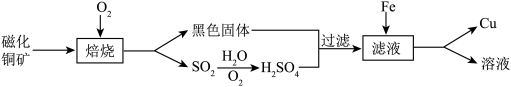
(2)写出滤液中加入Fe后一定发生反应的化学方程式
Ⅱ.金属的活动性。为比较金属M与Fe、Zn的金属活动性强弱,实验小组设计了如下图1装置(金属片均足量)的实验。待甲中充分反应后打开
 ,使甲中溶液全部进入乙中,乙中无明显现象,打开
,使甲中溶液全部进入乙中,乙中无明显现象,打开 使乙中溶液全部进入丙中,观察到Zn片表面变黑。回答下列问题:
使乙中溶液全部进入丙中,观察到Zn片表面变黑。回答下列问题: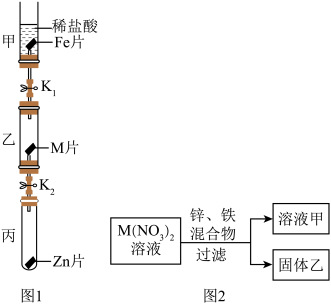
| A.甲中反应后得到黄色溶液 |
B.乙中现象证明金属活动性 |
| C.丙中反应后溶液质量增大 |
| D.将M片和Zn片互换位置仍能达到实验目的 |
(4)如图2所示,向一定量
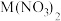 溶液中加入铁和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙。已知
溶液中加入铁和锌的混合物粉末,充分反应过滤,得到溶液甲和固体乙。已知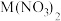 溶液呈无色。若溶液甲是无色,则溶液甲一定含有的金属阳离子是
溶液呈无色。若溶液甲是无色,则溶液甲一定含有的金属阳离子是
您最近一年使用:0次
解题方法
6 . 小明喜欢吃皮蛋。于是对妈妈用皮蛋粉制作皮蛋产生了浓厚的兴趣并开展了以“皮蛋制作”为主题的项目式学习。
任务一:配制皮蛋粉
小明将生石灰、纯碱和食盐按照一定比例混合,制成皮蛋粉。
任务二:浸鲜蛋
向配制的皮蛋粉中加入一定量的水,充分反应后产生白色沉淀,过滤,所得滤液称为浸出液。
(1)将新鲜鸭蛋放入其中浸泡即可。向皮蛋粉中加水时,发生反应的化学方程式为___________ 、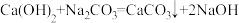 。
。
【提出问题】
浸出液中含有哪些溶质?
【做出猜想】
(2)猜想1:___________
猜想2:NaCl、NaOH和Ca(OH)2
猜想3:NaCl、NaOH和Na2CO3
(3)【实验验证】
【反思拓展】
(4)小丽认为还可以选择如下两个方案来验证猜想。
方案①:测浸出液的pH
方案②:向浸出液中通入CO2气体
小明认为两个方案均无法验证猜想,请任选一种方案说明理由___________ 。
任务三:品皮蛋
(5)皮蛋宜合理食用。下列说法正确的是___________(填字母)。
任务一:配制皮蛋粉
小明将生石灰、纯碱和食盐按照一定比例混合,制成皮蛋粉。
任务二:浸鲜蛋
向配制的皮蛋粉中加入一定量的水,充分反应后产生白色沉淀,过滤,所得滤液称为浸出液。
(1)将新鲜鸭蛋放入其中浸泡即可。向皮蛋粉中加水时,发生反应的化学方程式为
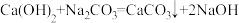 。
。【提出问题】
浸出液中含有哪些溶质?
【做出猜想】
(2)猜想1:
猜想2:NaCl、NaOH和Ca(OH)2
猜想3:NaCl、NaOH和Na2CO3
(3)【实验验证】
| 实验方案 | 实验现象 | 实验结论 |
| 取少量浸出液于试管中,滴加碳酸钠溶液 | 无明显现象 | 猜想 |
| 另取少量浸出液于试管中,加入足量稀盐酸 | 猜想3成立 |
【反思拓展】
(4)小丽认为还可以选择如下两个方案来验证猜想。
方案①:测浸出液的pH
方案②:向浸出液中通入CO2气体
小明认为两个方案均无法验证猜想,请任选一种方案说明理由
任务三:品皮蛋
(5)皮蛋宜合理食用。下列说法正确的是___________(填字母)。
| A.皮蛋含铁元素,适量食用有助于预防贫血 |
| B.剥开的皮蛋久置后虽易感染细菌,但不影响食用 |
| C.制作过程中,碱液会渗入皮蛋使之略带涩味,食用时可用食醋去涩 |
您最近一年使用:0次
名校
解题方法
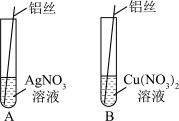
7 . 如图为同学们验证铝、铜、银金属活动性顺序的实验药品及仪器,请回答:_______ 。
(2)实验前打磨铝丝的目的是______ 。
(3)有同学认为上述实验无法验证三者的活动性顺序。请你补充一组试剂组合来完善实验______ 。
(2)实验前打磨铝丝的目的是
(3)有同学认为上述实验无法验证三者的活动性顺序。请你补充一组试剂组合来完善实验
您最近一年使用:0次
解题方法
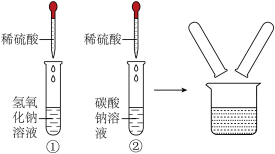
8 . 某化学学习小组在“利用稀硫酸分别鉴别氢氧化钠和碳酸钠”的实验充分反应后,将废液倒入废液缸中,发现又有气泡冒出:_______ 。
为了处理废液,需要对废液的成分进行分析:
【提出问题】废液缸中溶质的成分是什么?
【作出猜想】
(2)猜想一:溶质为Na2SO4;猜想二:溶质为_______ ;猜想三:溶质为Na2SO4和Na2CO3。
【查阅资料】Na2SO4溶液是中性的。
【设计方案】为验证猜想,小组的四位同学分别设计了如表实验:
【得出结论】猜想三成立。
【表达交流】
(3)①实验一溶液变红的原因是_______ 。
②小羽认为实验二的方案是错误的。原因是______ 。
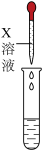
③实验四用到的X溶液的溶质类别与实验一、二、三不同,则X溶液溶质的化学式是______ 。
【反思评价】
(4)将上述废液加水稀释后可与油污反应,从而去除油污,厨房常用洗洁精清洗餐具上的油污,下列洗涤方法中与洗洁精清洗油污不相同的是_______。
为了处理废液,需要对废液的成分进行分析:
【提出问题】废液缸中溶质的成分是什么?
【作出猜想】
(2)猜想一:溶质为Na2SO4;猜想二:溶质为
【查阅资料】Na2SO4溶液是中性的。
【设计方案】为验证猜想,小组的四位同学分别设计了如表实验:
| 实验编号 | 实验一 | 实验二 | 实验三 | 实验四 |
| 实验方案 |
|
|
|
|
| 实验现象 | 溶液变为红色 | 产生白色沉淀 | 产生气泡 | 有明显实验现象 |
| 实验结论 | 猜想三成立 | 猜想三成立 | 猜想三成立 | 猜想三成立 |
【表达交流】
(3)①实验一溶液变红的原因是
②小羽认为实验二的方案是错误的。原因是
③实验四用到的X溶液的溶质类别与实验一、二、三不同,则X溶液溶质的化学式是
【反思评价】
(4)将上述废液加水稀释后可与油污反应,从而去除油污,厨房常用洗洁精清洗餐具上的油污,下列洗涤方法中与洗洁精清洗油污不相同的是_______。
| A.用汽油除去衣服上的油污 | B.用肥皂液洗衣服 | C.用沐浴露洗澡 |
您最近一年使用:0次
解题方法
9 . 《天工开物》描述了锡和锌的冶炼方法,下列说法不正确的是
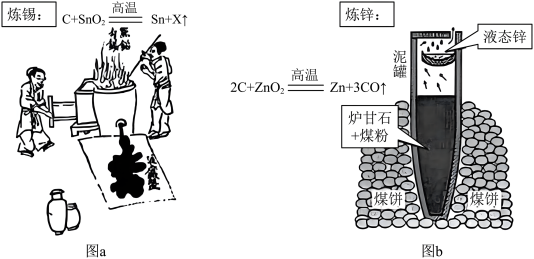
A.图a中X为 |
| B.图a炼锡时混入少许铅形成合金,产物更难熔化流出 |
| C.图b泥罐外煤饼的主要作用是燃烧提高热量 |
| D.图b必须冷却后才能取锌,是为了防止锌在较高的温度下又被氧化 |
您最近一年使用:0次
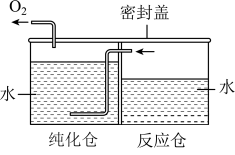
10 . 兴趣小组在跨学科实践课上制作了一台简易化学“制氧机”,原理如图所示。制氧时,在反应仓中加入适量水,再先后加入过碳酸钠和二氧化锰,反应仓中快速产生大量气泡,仓壁变得温热,纯化仓底部导气管口有气泡冒出。
(1)反应仓中过氧化氢生成氧气的化学方程式为______ ,二氧化锰所起的作用是______ 。
(2)纯化仓中的水除了有吸收杂质提纯氧气的作用,还可起到的作用是______ (填序号)。
①可以通过气泡观察氧气生成的速率
②降低氧气温度
③加快氧气的生成
(3)实验室用过氧化氢溶液和二氧化锰制取氧气时,应从下图中选择的发生和收集装置是_______ (填字母)。反应后进行过滤可回收 ,需用到的玻璃仪器有烧杯、玻璃棒和
,需用到的玻璃仪器有烧杯、玻璃棒和________ 。
(1)反应仓中过氧化氢生成氧气的化学方程式为
(2)纯化仓中的水除了有吸收杂质提纯氧气的作用,还可起到的作用是
①可以通过气泡观察氧气生成的速率
②降低氧气温度
③加快氧气的生成
(3)实验室用过氧化氢溶液和二氧化锰制取氧气时,应从下图中选择的发生和收集装置是
 ,需用到的玻璃仪器有烧杯、玻璃棒和
,需用到的玻璃仪器有烧杯、玻璃棒和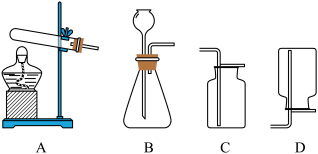
您最近一年使用:0次
2024-04-11更新
|
49次组卷
|
2卷引用:2024年陕西省西咸新区沣东上林学校九年级化学三模试题