解题方法
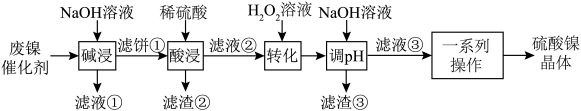
1 . 某废镍催化剂主要含金属Ni,还有少量的金属Al、Fe及其氧化物,少量的不溶性杂质。采用如图工艺流程回收其中的镍制备硫酸镍晶体(NiSO4•7H2O):
②H2O2可将FeSO4转化为Fe2(SO4)3。
③金属Ni的活泼性与铁相近。
回答下列问题:
(1)“酸浸”前将滤饼粉碎的目的是_______ 。
(2)“酸浸”步骤中发生的主要化学反应是_______ 。
(3)滤渣③的主要成分是______ (填化学式)。
(4)请用方程式表示“转化”过程中温度不能太高的原因______ 。
(5)“一系列操作”指的是______ 。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是_______ 。
②H2O2可将FeSO4转化为Fe2(SO4)3。
③金属Ni的活泼性与铁相近。
回答下列问题:
(1)“酸浸”前将滤饼粉碎的目的是
(2)“酸浸”步骤中发生的主要化学反应是
(3)滤渣③的主要成分是
(4)请用方程式表示“转化”过程中温度不能太高的原因
(5)“一系列操作”指的是
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
2 . 三氯化硼(BCl3)用于制备光导纤维和有机硼化物等,制备原理:B2O3+3C+3Cl2=2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示。
实验(一):制备BCl3。
(1)水浴R选择_______ (填“热水浴”或“冰水浴”),装碱石灰的仪器是_______ (填名称)。
(2)装置A中玻璃管a的作用是______ 。
(3)E装置的作用是______ 。
(4)写出BCl3水解产生H3BO3的化学方程式______ 。
实验(二):BCl3纯度的测定。
(5)准确称取wg产品,置于蒸馏水中,完全水解。用硝酸银进行含量测定,发现消耗mg质量分数为b%硝酸银溶液,则产品的纯度为______ 。(用含字母w、b、m的式子表示)

实验(一):制备BCl3。
(1)水浴R选择
(2)装置A中玻璃管a的作用是
(3)E装置的作用是
(4)写出BCl3水解产生H3BO3的化学方程式
实验(二):BCl3纯度的测定。
(5)准确称取wg产品,置于蒸馏水中,完全水解。用硝酸银进行含量测定,发现消耗mg质量分数为b%硝酸银溶液,则产品的纯度为
您最近一年使用:0次
3 . 硫酸亚铁铵【(NH4)2SO4·FeSO4·6H2O】俗称摩尔盐,可用于净水和治疗缺铁性贫血。工业上常利用机械加工行业产生的废铁屑(含有少量杂质Fe2O3)为原料制备(如图)。某化学兴趣小组拟用下列方案制备硫酸亚铁铵并进行相关探究。查阅资料:
(1)Fe和Fe3+会反应生成Fe2+
(2)FeSO4易被氧气氧化为Fe2(SO4)3,影响硫酸亚铁铵的等级。
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体,该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(4)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。
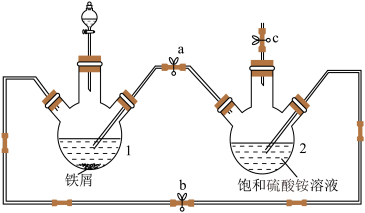
用下图所示装置制备硫酸亚铁铵。下列说法错误的是
(1)Fe和Fe3+会反应生成Fe2+
(2)FeSO4易被氧气氧化为Fe2(SO4)3,影响硫酸亚铁铵的等级。
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体,该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(4)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。
用下图所示装置制备硫酸亚铁铵。下列说法错误的是

| A.先关闭止水夹a,再打开止水夹b和c,滴加稀硫酸,充分反应后,烧瓶1溶液中有两种金属阳离子 |
| B.该过程中氢气的作用是防止硫酸亚铁被氧化成硫酸铁 |
| C.待烧瓶1中不再产生气泡时,关闭止水夹b、c,打开止水夹a,烧瓶2中有晶体出现 |
| D.为获得产品,需将烧瓶2中(NH4)2SO4·FeSO4·6H2O粗产品洗涤后干燥,洗涤的方式是先用冷水洗,后用无水乙醇洗 |
您最近一年使用:0次
解题方法
4 . 生活处处有化学,某兴趣小组同学对身边的物质进行了探究。
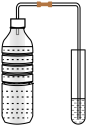
I.为了证明某碳酸饮料中含有CO2,小杨同学用如下图装置进行实验。
【查阅资料1】
①该饮料中存在柠檬酸,柠檬酸易溶于水和酒精,常温稳定,熔点153℃,熔化后沸腾前分解,分解温度约为175℃。
②紫色石蕊溶液遇到酸(如:碳酸、柠檬酸等)会变红色。
(1)打开瓶盖,立即塞上带导管的橡皮塞,将导管另一端伸入装有紫色石蕊溶液的试管中。当观察到试管内_______ ,证明饮料内含有CO2。
(2)小王同学质疑小杨的方案不够严谨,认为也可能是柠檬酸随着气体进入试管,导致紫色石蕊溶液变色。小杨在自己实验的基础上,未增加任何试剂,仅通过一步实验操作进行证明自己的结论正确。该操作和现象是_______ ,证明不是因为柠檬酸引起的紫色石蕊溶液变色。
Ⅱ.铁锈的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定10g铁锈中铁元素的质量,小张同学进行了如下实验。
【查阅资料2】
①草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4•3H2O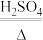 CO2↑+CO↑+4H2O。
CO2↑+CO↑+4H2O。
②浓硫酸具有吸水性。
③NaOH溶液可以吸收CO2。
④碱石灰为NaOH与CaO的混合物,可吸收CO2和H2O。
【设计实验】用如图所示装置进行实验:(草酸晶体在气体发生装置中分解)
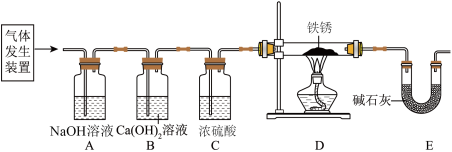
【分析与反思】
(3)B装置中Ca(OH)2的作用_______ 。
(4)实验结束,装置冷却至室温后,小赓同学通过称量_______ (填装置的字母)反应前后的质量变化计算出了10g铁锈中铁元素的质量。(假设铁锈完全反应)
(5)老师指出了【设计实验】中的实验装置存在一个明显缺陷:_______ 。
I.为了证明某碳酸饮料中含有CO2,小杨同学用如下图装置进行实验。

【查阅资料1】
①该饮料中存在柠檬酸,柠檬酸易溶于水和酒精,常温稳定,熔点153℃,熔化后沸腾前分解,分解温度约为175℃。
②紫色石蕊溶液遇到酸(如:碳酸、柠檬酸等)会变红色。
(1)打开瓶盖,立即塞上带导管的橡皮塞,将导管另一端伸入装有紫色石蕊溶液的试管中。当观察到试管内
(2)小王同学质疑小杨的方案不够严谨,认为也可能是柠檬酸随着气体进入试管,导致紫色石蕊溶液变色。小杨在自己实验的基础上,未增加任何试剂,仅通过一步实验操作进行证明自己的结论正确。该操作和现象是
Ⅱ.铁锈的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定10g铁锈中铁元素的质量,小张同学进行了如下实验。
【查阅资料2】
①草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4•3H2O
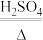 CO2↑+CO↑+4H2O。
CO2↑+CO↑+4H2O。②浓硫酸具有吸水性。
③NaOH溶液可以吸收CO2。
④碱石灰为NaOH与CaO的混合物,可吸收CO2和H2O。
【设计实验】用如图所示装置进行实验:(草酸晶体在气体发生装置中分解)

【分析与反思】
(3)B装置中Ca(OH)2的作用
(4)实验结束,装置冷却至室温后,小赓同学通过称量
(5)老师指出了【设计实验】中的实验装置存在一个明显缺陷:
您最近一年使用:0次
解题方法
5 . 实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体(CuSO4·5H2O),经历下列过程(已知Fe3+在pH=5时沉淀完全,Fe2+能被H2O2、Cl2、硝酸等物质氧化为Fe3+):

(1)写出步骤②发生的化学反应方程式___________ 。
(2)能否使用Cl2或硝酸代替H2O2,并说明理由___________ 。

(1)写出步骤②发生的化学反应方程式
(2)能否使用Cl2或硝酸代替H2O2,并说明理由
您最近一年使用:0次
解题方法
6 . 草酸(乙二酸)存在于自然界的植物中,草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。回答下列问题:
查阅资料:①已知H2C2O4能使澄清石灰水反应变浑浊;②无水氯化钙吸收水分;③浓氢氧化钠能吸收二氧化碳。

(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。
①装置C中可观察到的现象是______ ;
②由此可知草酸晶体分解的产物中有CO2,装置B的主要作用是______ ;
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。

①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、______ 、G、H、D、I;
②装置H反应管中盛有的物质是______ ;
③能证明草酸晶体分解产物中有CO的现象是______ ;
(3)设计实验证明:草酸是一种酸性物质______ 。
查阅资料:①已知H2C2O4能使澄清石灰水反应变浑浊;②无水氯化钙吸收水分;③浓氢氧化钠能吸收二氧化碳。

(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。
①装置C中可观察到的现象是
②由此可知草酸晶体分解的产物中有CO2,装置B的主要作用是
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。

①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、
②装置H反应管中盛有的物质是
③能证明草酸晶体分解产物中有CO的现象是
(3)设计实验证明:草酸是一种酸性物质
您最近一年使用:0次
7 . “化学链燃烧”是指燃料不直接与空气接触,而是以载氧体在两个反应器之间的循环来实现燃料较低温度下燃烧的过程。某“化学链燃烧”的过程如下:

A.空气反应器中发生的反应为: |
| B.X中氮气的含量比空气中高 |
| C.与直接燃烧相比,“化学链燃烧”有利于二氧化碳的捕集 |
| D.等质量的甲烷直接燃烧比“化学链燃烧”消耗氧气多 |
您最近一年使用:0次
2023-09-28更新
|
1558次组卷
|
31卷引用:福建省厦门市2023-2024学年九年级上学期化学用语教学质量监测试题
福建省厦门市2023-2024学年九年级上学期化学用语教学质量监测试题2023年江苏省无锡市中考化学真题(已下线)课题2 如何正确书写化学方程式(知识清单+练习)-【安老师大讲堂】2023-2024学九年级化学上册同步课堂精讲练(人教版)(已下线)第4章 认识化学变化(A卷)-2023-2024学年九年级化学上册同步测试优选卷(沪教版)(已下线)5.2如何正确书写化学方程式-【易备课】2023-2024学年九年级化学上册同步精品讲义(人教版)江苏省苏州市姑苏区胥江实验中学2023-2024学年九年级上学期12月月考化学卷江苏省苏州市工业园区金鸡湖中学2023-2024学年九年级上学期12月月考化学试题江苏省无锡市锡山区仓下中学、二泉中学2023-2024学年九年级上学期12月月考化学试题(已下线)专题04 物质的组成和结构-【寒假自学课】2024年九年级化学寒假提升学与练(人教版)江苏省南京市鼓楼区南京师范大学附属中学树人学校2023-2024学年九年级上学期12月份化学测试卷江苏省淮安市淮安区开明中学2023-2024学年九年级上学期月测2化学试题(已下线)寒假作业02 空气 氧气-【寒假分层作业】2024年九年级化学寒假培优练(人教版) 湖北省 武汉市光谷实验中学2023—2024学年上学期12月适应性测试 物理化学试卷(已下线)九年级化学开学模拟考(福建专用,人教版1-8单元)-2023-2024学年初中下学期开学摸底考试卷安徽省宿州市灵璧县第六初级中学2023-2024学年九年级上学期素质检测三化学试题江苏省扬州市邗江区2023-2024学年九年级上学期期末化学试题江苏省扬州市邗江区梅苑双语学校2023-2024学年九年级上学期10月月考化学试卷(已下线)黄金卷03(全国通用)-【赢在中考·黄金8卷】备战2024年中考化学模拟卷(全国通用)(已下线)黄金卷(无锡专用)-【赢在中考·黄金8卷】备战2024年中考化学模拟卷(江苏专用)(已下线)2024年中考风向标-江苏-图形、图像与流程分析海南省海口市安定县山高中学2023-2024学年九年级上学期期末化学试卷2024年江苏省天一中学、格致中学一模联考化学试卷(已下线)专题05 工业流程题(题型专练)-备战2024年中考化学一轮复习考点帮(沪教版·全国)福建省莆田市荔城区中山中学、金石中学等四校2023-2024学年九年级下学期3月联考化学试题2024年广东省茂名市滨海新区中考一模化学试题(已下线)专题03? 教材基础实验(七大题型)-2024年中考化学二轮热点题型归纳与变式演练(江苏通用)(已下线)易错类型04 质量守恒定律 化学方程式 微观模型“六大”易错点-备战2024年中考化学考试易错题(全国通用)(已下线)重难点05 燃烧 燃料 能源-2024年中考化学【热点·重点·难点】专练(全国通用)(已下线)专题十 燃料及其利用【五大题型】-备战2024年中考化学二轮轮复习举一反三系列(全国通用)2024年江苏省常州市田家炳初级中学中考一模化学试卷 2024年山东省青岛莱西市中考一模化学试题
8 .  是一种高效的杀菌消毒剂,也常用来漂白织物等。用下列装置探究
是一种高效的杀菌消毒剂,也常用来漂白织物等。用下列装置探究 的制备。资料:晶体以
的制备。资料:晶体以 的形式存在,不稳定可发生如下反应:
的形式存在,不稳定可发生如下反应: 完成下列填空:
完成下列填空:

(1)仪器a的名称为_____ ,装置②的作用是_____ 。
(2)检查装置气密性的方法是_____ 。
(3)关闭 ,从分液漏斗中加入一定量浓硫酸,装置③中生成
,从分液漏斗中加入一定量浓硫酸,装置③中生成 的化学方程式为
的化学方程式为 ,该反应中化合价发生改变的元素有
,该反应中化合价发生改变的元素有_____ 。
(4)实验完成后,为防止装置中残留的有毒气体污染空气,可以进行的操作是:打开止水夹
_____ 。
(5)装置③采用冰水浴的目的是_____ 。
(6)为测定所得固体中 的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为ag,灼烧恒重后,得到固体bg。则晶体中
的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为ag,灼烧恒重后,得到固体bg。则晶体中 的质量分数是
的质量分数是_____ 。
 是一种高效的杀菌消毒剂,也常用来漂白织物等。用下列装置探究
是一种高效的杀菌消毒剂,也常用来漂白织物等。用下列装置探究 的制备。资料:晶体以
的制备。资料:晶体以 的形式存在,不稳定可发生如下反应:
的形式存在,不稳定可发生如下反应: 完成下列填空:
完成下列填空:
(1)仪器a的名称为
(2)检查装置气密性的方法是
(3)关闭
 ,从分液漏斗中加入一定量浓硫酸,装置③中生成
,从分液漏斗中加入一定量浓硫酸,装置③中生成 的化学方程式为
的化学方程式为 ,该反应中化合价发生改变的元素有
,该反应中化合价发生改变的元素有(4)实验完成后,为防止装置中残留的有毒气体污染空气,可以进行的操作是:打开止水夹

(5)装置③采用冰水浴的目的是
(6)为测定所得固体中
 的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为ag,灼烧恒重后,得到固体bg。则晶体中
的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为ag,灼烧恒重后,得到固体bg。则晶体中 的质量分数是
的质量分数是
您最近一年使用:0次
名校
解题方法
9 . 某白色固体甲的主要成分为 ,可能含有
,可能含有 、
、 、
、 和
和 中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:
中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:

(1)写出生成白色固体丙的化学方程式_______ 。
(2)向无色溶液D中加入过量稀盐酸的目的是_______ 。
(3)分析上述实验可知,白色固体甲中一定没有的物质是_______ 。
(4)若用上述实验中的A、B、C、D四种溶液鉴别稀 和
和 溶液,能达到鉴别目的的是
溶液,能达到鉴别目的的是_______ 。
 ,可能含有
,可能含有 、
、 、
、 和
和 中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:
中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:
(1)写出生成白色固体丙的化学方程式
(2)向无色溶液D中加入过量稀盐酸的目的是
(3)分析上述实验可知,白色固体甲中一定没有的物质是
(4)若用上述实验中的A、B、C、D四种溶液鉴别稀
 和
和 溶液,能达到鉴别目的的是
溶液,能达到鉴别目的的是
您最近一年使用:0次
2023-07-08更新
|
290次组卷
|
2卷引用:广东省云浮市郁南县东坝镇初级中学2023年金钥匙科技竞赛(初三学生CESL活动)初赛模拟化学试题(六)
解题方法
10 . 某实验学校初三兴趣小组利用如下图所示装置(部分固定装置已略去)制备氮化钙,并探究其化学式(实验式)。

(1)按上图连接好实验装置,检查装置气密性的方法是_______ 。
(2)反应过程中末端导管必须插入试管A的水中,目的是_______ 。
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后,_______ ;④拆除装置,取出产物。
(4)没有U形管的可能后果是:_______ 。
(5)数据记录如下:
计算得到化学式(实验式)CaxN2,其中x=_______ 。
(6)若通入的N2中混有少量O2,则(5)中计算得到的x_______ (填“偏大”或“偏小”或“不变”)。

(1)按上图连接好实验装置,检查装置气密性的方法是
(2)反应过程中末端导管必须插入试管A的水中,目的是
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后,
(4)没有U形管的可能后果是:
(5)数据记录如下:
| 空硬质玻璃管质量m0/g | 硬质玻璃管与钙的质量m1/g | 硬质玻璃管与产物的质量m2/g |
| 114.8 | 120.8 | 122.2 |
(6)若通入的N2中混有少量O2,则(5)中计算得到的x
您最近一年使用:0次



