解题方法
1 . 某品牌威化饼干的配料如图所示,研究性学习小组对其部分成分进行相关探究。
①饼干制作烘焙过程中,配料中的碳酸氢钠全部受热分解转化为碳酸钠,而碳酸钠不分解。
②碱石灰是固体氢氧化钠和氧化钙的混合物。
【实验准备】
称取质量为m的饼干样品放入烧杯中,加入适量蒸馏水,充分溶解后过滤,将滤液通过半透膜渗析(除去蛋白质等有机物),得到待检液,将待检液平均分为甲、乙两等份。
任务一:定性验证饼干样品中的有关成分
【实验验证】
(1)请完善下面的表格:
【交流讨论】
(2)小组有同学认为可以把步骤I中的稀硝酸改为稀盐酸。经讨论后,大家一致认为不可行,理由是________________________ 。
任务二:定量测定饼干样品中碳酸钠的质量分数
【实验探究】小组同学用待检液乙进行如下实验。主要步骤:①检查装置气密性后装入药品;②通入一段时间N2;③称量装置C的质量为m1;④滴加稀硫酸充分反应;⑤再通入一段时间N2;⑥称量装置C的质量为m2。
(3)装置C中发生反应的化学方程式为__________ 。
【实验结论】
(4)该饼干样品中碳酸钠的质量分数为________ (用m、m1、m2表示)。

①饼干制作烘焙过程中,配料中的碳酸氢钠全部受热分解转化为碳酸钠,而碳酸钠不分解。
②碱石灰是固体氢氧化钠和氧化钙的混合物。
【实验准备】
称取质量为m的饼干样品放入烧杯中,加入适量蒸馏水,充分溶解后过滤,将滤液通过半透膜渗析(除去蛋白质等有机物),得到待检液,将待检液平均分为甲、乙两等份。
任务一:定性验证饼干样品中的有关成分
【实验验证】
(1)请完善下面的表格:
| 实验步骤 | 实验现象 | 实验结论 |
| Ⅰ.取少许待检液甲于试管中,滴入过量稀硝酸 | 有 | 饼干中含有碳酸钠 |
| Ⅱ.向步骤①反应后溶液中滴入少量硝酸银溶液 | 有白色沉淀产生 | 饼干中含有 |
【交流讨论】
(2)小组有同学认为可以把步骤I中的稀硝酸改为稀盐酸。经讨论后,大家一致认为不可行,理由是
任务二:定量测定饼干样品中碳酸钠的质量分数
【实验探究】小组同学用待检液乙进行如下实验。主要步骤:①检查装置气密性后装入药品;②通入一段时间N2;③称量装置C的质量为m1;④滴加稀硫酸充分反应;⑤再通入一段时间N2;⑥称量装置C的质量为m2。
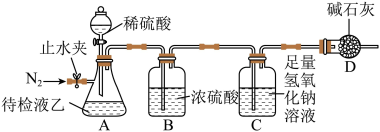
(3)装置C中发生反应的化学方程式为
【实验结论】
(4)该饼干样品中碳酸钠的质量分数为
您最近一年使用:0次
2 . 某溶液可能含有HCl、CuCl2、CuSO4中的一种或几种,为了探究其组成,向一定质量的该溶液中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。下列说法正确的是
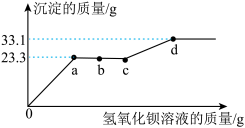
| A.d点后,溶液的pH保持不变 |
| B.b点对应的溶液中有三种溶质 |
| C.c点到d点的过程中,溶液中溶质总质量在减少 |
| D.原溶液含有HCl、CuCl2和CuSO4 |
您最近一年使用:0次
名校
解题方法
3 . 我国早在商代时期就开始使用铜器,到春秋战国时期,开始生产和使用铁器。
(1)铁锅用于烹饪食物主要是利用铁具有良好的______ 性。
(2)下列文物中不属于金属制品的是______(填字母序号)。
(3)《本草纲目拾遗》中记载:“舶上铁日久起销(锈)…刮下之销末,名铁线粉”。铁丝“日久起销”的原因是铁与空气中的______ (填化学式)同时接触而导致。
(4)我国古代曾用“湿法炼铜”和“火法炼铜”,其原理分别为:
①湿法炼铜:Fe+CuSO4=Cu+FeSO4
②火法炼铜:Cu2S+O2 2Cu+SO2
2Cu+SO2
上述两种方案中较优的是______ (填数字序号),理由是______ 。
(5)将一定量的铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液。下列判断正确的是______(填字母序号)。
(6)某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量的稀盐酸反应产生2g氢气,则该金属粉末的组成情况有_______ 种。
(1)铁锅用于烹饪食物主要是利用铁具有良好的
(2)下列文物中不属于金属制品的是______(填字母序号)。
A.鎏金骑士铜贮贝器 | B.鸡形陶壶 |
C.牛虎铜案 | D.滇王金印 |
(3)《本草纲目拾遗》中记载:“舶上铁日久起销(锈)…刮下之销末,名铁线粉”。铁丝“日久起销”的原因是铁与空气中的
(4)我国古代曾用“湿法炼铜”和“火法炼铜”,其原理分别为:
①湿法炼铜:Fe+CuSO4=Cu+FeSO4
②火法炼铜:Cu2S+O2
 2Cu+SO2
2Cu+SO2上述两种方案中较优的是
(5)将一定量的铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液。下列判断正确的是______(填字母序号)。
| A.滤液中一定有Zn(NO3)2 |
| B.滤渣的质量一定大于所加入固体的质量 |
| C.向滤渣中加入稀硫酸,有气泡产生,则滤渣中一定有Zn,一定不含Ag |
| D.若滤液为蓝色、则滤液中一定含有硝酸锌和硝酸铜,一定役有硝酸银 |
(6)某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量的稀盐酸反应产生2g氢气,则该金属粉末的组成情况有
您最近一年使用:0次
4 . 纯碱工业始于18世纪,我国化学家侯德榜为纯碱工业技术的发展作出了杰出的贡献。某化学兴趣小组对纯碱的性质及用途开展项目式学习。
任务一:探究纯碱的性质——Na2CO3溶液呈碱性
【查阅资料】
①溶液呈碱性,是因为溶液中存在较多的OH-。
②Na2CO3在水中全部解离出Na+和CO 。
。
③CaCl2溶液呈中性,Ca2+、Cl-对溶液的酸碱性没有影响。
【提出猜想】
(1)猜想一:H2O单独起作用,产生较多的OH-,使溶液呈碱性
猜想二:___________ 。
猜想三:CO 与H2O作用,产生较多的OH-,使溶液呈碱性
与H2O作用,产生较多的OH-,使溶液呈碱性
【实验探究】
(2)完成下列表格
【实验分析】
(3)②中产生白色沉淀的化学方程式为___________ 。
【拓展延伸】
(4)同学们和老师交流得知,Na2CO3溶液中含有的阴离子为HCO 、OH-和
、OH-和___________ 。
任务二:探究纯碱的用途一一用于生产洗涤剂
【查阅资料】Na2CO3可用于生产洗涤剂,Na2CO3呈碱性,可清洗油污,溶液碱性越强,去污效果越好。
【实验探究】兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,并测定在不同温度下溶液的pH,记录数据如表:
【解释与结论】
(5)实验①②③对比,可得出的结论是___________ 。
(6)要证明溶液的溶质质量分数变化与pH变化关系,可选择的3个实验编号是___________ 。
任务一:探究纯碱的性质——Na2CO3溶液呈碱性
【查阅资料】
①溶液呈碱性,是因为溶液中存在较多的OH-。
②Na2CO3在水中全部解离出Na+和CO
 。
。③CaCl2溶液呈中性,Ca2+、Cl-对溶液的酸碱性没有影响。
【提出猜想】
(1)猜想一:H2O单独起作用,产生较多的OH-,使溶液呈碱性
猜想二:
猜想三:CO
 与H2O作用,产生较多的OH-,使溶液呈碱性
与H2O作用,产生较多的OH-,使溶液呈碱性【实验探究】
(2)完成下列表格
| 实验操作 | 实验现象 | 实验结论 |
| I.向试管中加入一定量的蒸馏水,滴入2滴酚酞溶液 | 溶液无明显变化 | 猜想一不成立 |
| Ⅱ.向试管中加入一定量的NaCl溶液,滴入2滴酚酞溶液 | 溶液无明显变化 | 猜想二不成立 |
| Ⅲ.①向试管中加入一定量的Na2CO3溶液,滴入2滴酚酞溶液 ②向①所得溶液中逐滴加入CaCl2溶液至过量 | ① ②有白色沉淀产生 | 猜想三成立 |
【实验分析】
(3)②中产生白色沉淀的化学方程式为
【拓展延伸】
(4)同学们和老师交流得知,Na2CO3溶液中含有的阴离子为HCO
 、OH-和
、OH-和任务二:探究纯碱的用途一一用于生产洗涤剂
【查阅资料】Na2CO3可用于生产洗涤剂,Na2CO3呈碱性,可清洗油污,溶液碱性越强,去污效果越好。
【实验探究】兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,并测定在不同温度下溶液的pH,记录数据如表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 溶质质量分数/% | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
| 溶液温度/℃ | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 70 |
| 溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
(5)实验①②③对比,可得出的结论是
(6)要证明溶液的溶质质量分数变化与pH变化关系,可选择的3个实验编号是
您最近一年使用:0次
名校
解题方法
5 . 2024年5月1日,我国完全自主设计建造的首艘弹射型航母“福建舰”开展首次航行试验。___________ 性。
(2)建造航母用到钛合金,钛合金放到海水中数年,取出后仍光亮如初,体现钛合金具有非常好的___________ 性能。钛的氧化物TiO2能与焦炭、氯气发生如下反应: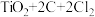

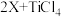 ,其中X的化学式为
,其中X的化学式为___________ 。
(3)航母飞行甲板钢板表面镀有镍等金属。镍(Ni)的金属活动性介于铁和锡之间,化合物中镍元素通常显+2价。
①写出Ni与CuSO4溶液反应的化学方程式___________ ;
②为验证Fe、Ni、Cu三种金属的活动性顺序,下列选用的药品不可行的是___________ (填标号);
A.FeCl2溶液、Ni、Cu B.Fe、NiCl2溶液、Cu C.FeCl2溶液、Ni、CuCl2溶液
③由氧化镍制备高纯度的镍,有以下两种方案:
方案一:
方案二: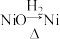
你认为上述两种方案中较优的是___________ (写出选择的方案并说明理由)。
(4)现有不纯的铁粉样品2g,杂质可能含有镁、铝、锌中的一种或几种。向该样品中加入溶质质量分数为9.8%的稀硫酸,恰好完全反应,产生0.2g氢气。下列说法正确的是___________(填标号)。

(2)建造航母用到钛合金,钛合金放到海水中数年,取出后仍光亮如初,体现钛合金具有非常好的
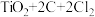

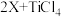 ,其中X的化学式为
,其中X的化学式为(3)航母飞行甲板钢板表面镀有镍等金属。镍(Ni)的金属活动性介于铁和锡之间,化合物中镍元素通常显+2价。
①写出Ni与CuSO4溶液反应的化学方程式
②为验证Fe、Ni、Cu三种金属的活动性顺序,下列选用的药品不可行的是
A.FeCl2溶液、Ni、Cu B.Fe、NiCl2溶液、Cu C.FeCl2溶液、Ni、CuCl2溶液
③由氧化镍制备高纯度的镍,有以下两种方案:
方案一:

方案二:
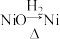
你认为上述两种方案中较优的是
(4)现有不纯的铁粉样品2g,杂质可能含有镁、铝、锌中的一种或几种。向该样品中加入溶质质量分数为9.8%的稀硫酸,恰好完全反应,产生0.2g氢气。下列说法正确的是___________(填标号)。
| A.反应消耗的稀硫酸质量为100g |
| B.样品中一定含有铝 |
| C.样品的组成有6种情况 |
| D.反应后所得溶液中溶质质量为11.6g |
您最近一年使用:0次
解题方法
6 . 钙的化合物的转化关系如图所示(图中“→”表示一种物质可以转化为另一种物质)。下列说法中不正确的是
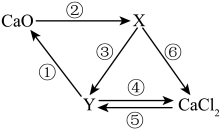
| A.X的俗名是消石灰 |
| B.Y的物质类别属于盐 |
| C.图中涉及化合反应、分解反应、置换反应、复分解反应 |
| D.反应④的过程中能看到产生气泡 |
您最近一年使用:0次
7 . 海水晒盐得到的粗盐中常含有泥沙及少量可溶性CaCl2、Na2SO4杂质,化学兴趣小组为获得精盐进行如图实验。下列相关说法正确的是
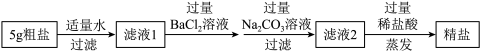
| A.实验室进行蒸发操作时,要等到蒸发皿中的水分蒸干时才能停止加热 |
| B.可加入过量K2CO3溶液代替Na2CO3溶液 |
| C.可调换“过量BaCl2溶液”与“过量Na2CO3溶液”的加入顺序 |
| D.若称得精盐的质量为4.5g,则该粗盐样品中氯化钠的质量分数一定小于90% |
您最近一年使用:0次
解题方法
8 . 《天工开物》是我国古代科技发展的智慧结晶。书中记载了有关金属铜及铜合金的工艺:“凡铜供世用,出山与出炉只有赤铜。以炉甘石或倭铅参和,转色为黄铜;以砒霜等药制炼为白铜;矾、硝等药制炼为青铜……。”
(1)青铜是金属冶铸史上最早的合金,如图所示的青铜鬲流行于商代至春秋,鬲是中国古代的一种炊具。青铜制成的鬲能做炊具是利用了金属的_______ 性。_______ (写一点)。为了鉴别黄铜和黄金,将真假黄金分别放入稀硫酸中,黄金表面没有明显变化,而观察到黄铜表面有气泡产生,其反应的化学方程式为_______ 。
(3)人类发现铁和铜的时期相差不大,但出土文物中铁制品很少,原因是铁制品容易与空气中_______ 的反应而生锈,生活中常采用_______ (写一种)的方法防止铁制品锈蚀。
(4)“倭铅”是锌的古称。
①化学兴趣小组将一定量的锌粉加入含有FeCl2和CuCl2的废液中,充分反应后过滤,得到滤液和滤渣,向滤渣中滴加稀盐酸,有气泡产生,则滤液中一定含有的溶质是_______ (填化学式)。
②实验室有一定质量含锌的两种金属混合物,加入过量的稀盐酸,充分反应,测得生成H2的质量为0.2g,将反应后的溶液蒸发,得到11.1g固体。则金属混合物中的另一种金属可能是_______ (填标号)。
A.Mg B.Al C.Fe D.Cu
(1)青铜是金属冶铸史上最早的合金,如图所示的青铜鬲流行于商代至春秋,鬲是中国古代的一种炊具。青铜制成的鬲能做炊具是利用了金属的

(3)人类发现铁和铜的时期相差不大,但出土文物中铁制品很少,原因是铁制品容易与空气中
(4)“倭铅”是锌的古称。
①化学兴趣小组将一定量的锌粉加入含有FeCl2和CuCl2的废液中,充分反应后过滤,得到滤液和滤渣,向滤渣中滴加稀盐酸,有气泡产生,则滤液中一定含有的溶质是
②实验室有一定质量含锌的两种金属混合物,加入过量的稀盐酸,充分反应,测得生成H2的质量为0.2g,将反应后的溶液蒸发,得到11.1g固体。则金属混合物中的另一种金属可能是
A.Mg B.Al C.Fe D.Cu
您最近一年使用:0次
9 . 海水是重要的自然资源,回答下列问题。
(1)用化学用语填空:
①保持水化学性质的最小粒子_______ ;
②构成氯化钠的粒子_______ ;
③氦气_______ 。
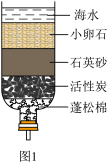
(2)地下水经上述自制净水器净化后为_____ (选填“硬水”或“软水”)。
(3)生活中将硬水转化为软水的方法是_____ 。
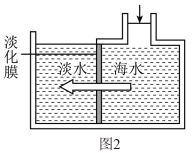
(4)采用膜分离技术可将净化后的海水进行淡化,如图2所示。通过对淡化膜右侧的海水加压,水分子透过淡化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水组成的变化进行分析,正确的说法是 。
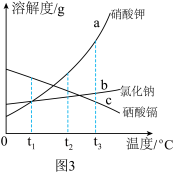
(5)海水中某些元素组成的物质的溶解度曲线如图3所示。将t3℃时等质量的三种物质的饱和溶液分别降温到t1℃,对所得溶液的分析正确的是 。
(1)用化学用语填空:
①保持水化学性质的最小粒子
②构成氯化钠的粒子
③氦气
(2)地下水经上述自制净水器净化后为
(3)生活中将硬水转化为软水的方法是
(4)采用膜分离技术可将净化后的海水进行淡化,如图2所示。通过对淡化膜右侧的海水加压,水分子透过淡化膜进入左侧淡水池,而海水中的各种离子不能透过淡化膜,从而得到淡水。对加压后右侧海水组成的变化进行分析,正确的说法是 。
| A.溶质质量减少 | B.溶剂质量减少 | C.溶质质量分数减小 |
(5)海水中某些元素组成的物质的溶解度曲线如图3所示。将t3℃时等质量的三种物质的饱和溶液分别降温到t1℃,对所得溶液的分析正确的是 。
| A.t1℃物质的溶解度:c>a=b |
| B.溶剂质量:c>a>b |
| C.溶液质量:c>b>a |
| D.溶质质量:a=b>c |
您最近一年使用:0次
名校
解题方法
10 . 实验兴趣小组的同学进行了如图所示的溶解实验(物质x为不含结晶水的固体)。下列说法不正确的是
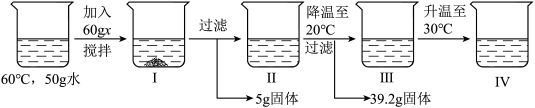
A.溶液I、II均为 的饱和溶液 的饱和溶液 |
B.60℃时, 的溶解度为55g 的溶解度为55g |
| C.溶液III、IV的溶质质量分数相同 |
D.采用降温的方式,可将接近饱和的 溶液转化为饱和溶液 溶液转化为饱和溶液 |
您最近一年使用:0次



