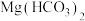1 . CH3OH、C2H5OH、C4H10O组成的混合物中,氧元素的质量分数为y,则碳元素的质量分数为_____________ 。
您最近一年使用:0次
2 . 下列图像中有关量的变化与对应实验叙述一致的是
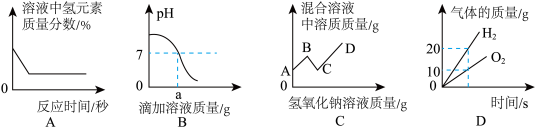
| A.向一定质量的过氧化氢溶液中加入少量的二氧化锰 |
| B.向a克10%的氢氧化钠溶液逐渐滴加a克10%盐酸 |
| C.将氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中 |
| D.电解水实验中,生成的氢气和氧气之间的质量关系 |
您最近一年使用:0次
2024-07-09更新
|
31次组卷
|
3卷引用:2024年新疆乌鲁木齐市第十三中学中考一模化学试卷
2024年新疆乌鲁木齐市第十三中学中考一模化学试卷2024年新疆乌鲁木齐市第十三中学九年级中考物理化学模拟试卷-初中化学(已下线)专题09 酸、碱、盐-【好题汇编】5年(2020-2024)中考1年模拟化学真题分类汇编(新疆专用)
解题方法
3 . 金属材料的应用推动了社会的发展。新型材料的研制,已成为现代高新技术的重要物质基础。
(1)镁和铝可熔炼成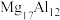 镁合金,熔炼过程只能在真空中,不能在空气中进行的原因是
镁合金,熔炼过程只能在真空中,不能在空气中进行的原因是____________ (写其中一个化学方程式)。
(2)某锌粉含有铜、镁中的一种杂质,取该样品6.5g与足量稀盐酸充分反应,生成氢气0.21g,该锌粉中含有的杂质是______ 。另取一定量该样品加入硫酸铜溶液,充分反应后过滤,得到滤渣和滤液。向滤渣中滴入稀硫酸,有气泡产生,则滤液中一定含有的溶质是______ (填化学式)。
(3)生活中应用最广泛的金属为铁,下列物质在常温下能与铁发生反应的是______。
(1)镁和铝可熔炼成
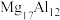 镁合金,熔炼过程只能在真空中,不能在空气中进行的原因是
镁合金,熔炼过程只能在真空中,不能在空气中进行的原因是(2)某锌粉含有铜、镁中的一种杂质,取该样品6.5g与足量稀盐酸充分反应,生成氢气0.21g,该锌粉中含有的杂质是
(3)生活中应用最广泛的金属为铁,下列物质在常温下能与铁发生反应的是______。
A. | B. 溶液 溶液 | C.稀盐酸 | D.AgCl |
您最近一年使用:0次
解题方法
4 . 在古代,地下水代替江河,聚拢着人气和城乡的繁荣。现在仍有一些区域和生产领域再使用地下水。化学兴趣小组的同学对某乡镇地下水的使用情况、硬度及合理利用等内容进行项目式学习。
任务一:调查地下水的使用情况
【问卷调查】调查显示该地域部分家庭通过打井使用地下水,主要用于饮用和农作物的浇灌。
任务二:探究井水的硬度
【实验探究】
(1)取适量蒸馏水和井水分别倒入两个烧杯中,向两个烧杯中加入等量的______ ,搅拌。蒸馏水中泡沫较多,井水中泡沫较少,浮渣较多,说明井水硬度比较大。
【咨询老师】该小组的同学通过咨询知道,当地井水中含有较多的 、
、 、
、 ;离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢,水垢中主要含有
;离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢,水垢中主要含有 和
和 ,还可能含有其他物质。为确定水垢的成分,同学们继续探究。
,还可能含有其他物质。为确定水垢的成分,同学们继续探究。
【查阅资料】有关物质在水中的溶解性表(室温):
【推断预测】
(2)根据以上溶解性表推测水垢中还可能含有 或
或______ 。
【进行实验】
(3)
【实验结论】
(4)同学们通过以上实验,确定了水垢中主要除了含有 和
和 ,还含有
,还含有______
【拓展延伸】
(5)定量研究是确定物质成分的一种方法。现有一包白色固体,可能是 或
或 、
、 的混合物。取10g该固体,加入足量稀盐酸,充分反应后测得生成的气体质量为4.8g,说明白色固体含有
的混合物。取10g该固体,加入足量稀盐酸,充分反应后测得生成的气体质量为4.8g,说明白色固体含有______ 物质(填“一种”或“两种”)。
任务三:井水的合理利用
【小组交流】
(6)①有些井水硬度比较高,常年饮用,易患结石,所以饮用井水前应将其______ ,既可降低硬度还可杀灭水中的细菌。
②同学们认为适当开发地下水可缓解缺水问题,但过度开采会导致地面沉降。为了更好的保护水资源,请写出一条家庭节约用水的措施:______ (填一条即可)。
③实验室为了确保实验结果准确,想将井水加工成净化程度较高的水,可以采用______ 的方法。
【项目总结】通过以上学习,同学们认识到水是人类宝贵的自然资源,应该合理利用。
任务一:调查地下水的使用情况
【问卷调查】调查显示该地域部分家庭通过打井使用地下水,主要用于饮用和农作物的浇灌。
任务二:探究井水的硬度
【实验探究】
(1)取适量蒸馏水和井水分别倒入两个烧杯中,向两个烧杯中加入等量的
【咨询老师】该小组的同学通过咨询知道,当地井水中含有较多的
 、
、 、
、 ;离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢,水垢中主要含有
;离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢,水垢中主要含有 和
和 ,还可能含有其他物质。为确定水垢的成分,同学们继续探究。
,还可能含有其他物质。为确定水垢的成分,同学们继续探究。【查阅资料】有关物质在水中的溶解性表(室温):
物质 |
|
|
|
|
|
|
溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
(2)根据以上溶解性表推测水垢中还可能含有
 或
或【进行实验】
(3)
实验设计 | 实验现象 |
在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,静置一段时间后,取上层清液于两支试管中,分别编号为A和B。向试管A中通入 | 无白色沉淀 |
由溶解性表可知,向试管B中加入 | 产生白色沉淀 |
【实验结论】
(4)同学们通过以上实验,确定了水垢中主要除了含有
 和
和 ,还含有
,还含有【拓展延伸】
(5)定量研究是确定物质成分的一种方法。现有一包白色固体,可能是
 或
或 、
、 的混合物。取10g该固体,加入足量稀盐酸,充分反应后测得生成的气体质量为4.8g,说明白色固体含有
的混合物。取10g该固体,加入足量稀盐酸,充分反应后测得生成的气体质量为4.8g,说明白色固体含有任务三:井水的合理利用
【小组交流】
(6)①有些井水硬度比较高,常年饮用,易患结石,所以饮用井水前应将其
②同学们认为适当开发地下水可缓解缺水问题,但过度开采会导致地面沉降。为了更好的保护水资源,请写出一条家庭节约用水的措施:
③实验室为了确保实验结果准确,想将井水加工成净化程度较高的水,可以采用
【项目总结】通过以上学习,同学们认识到水是人类宝贵的自然资源,应该合理利用。
您最近一年使用:0次
2024·新疆·模拟预测
解题方法
5 . 铜是使用最早、应用广泛的金属。
(一)对古代铜制品认识
(1)玖玖同学到兴化博物馆参观,发现了一把如图所示的战国青铜剑。该文物能保存至今的原因可能是___________ (选填序号)。
(2)《吕氏春秋·别类篇》载有“金柔锡柔,合两柔则刚”(注:此处“金”指铜),表明我们的祖先已认识到铜合金的硬度比纯铜___________ (填“大”或“小”)。
(二)碱式碳酸铜的热分解实验
某碱式碳酸铜成分可表示为Cua(OH)b(CO3)c,兴趣小组为探究其性质和组成,用如图装置控制一定温度使34.6g样品充分分解,观察到固体变成黑色。___________ ,再加样品。
(4)D装置的作用是___________ 。
(5)停止加热后仍需继续通N2,可防止倒吸和___________ 。
(6)测得实验前后各装置的质量变化如表所示。
①分析数据,样品中氢元素质量为___________ ;碳元素质量为___________ ;铜元素质量为___________ 。(写出计算过程)
②该碱式碳酸铜的化学式为___________ 。
(一)对古代铜制品认识
(1)玖玖同学到兴化博物馆参观,发现了一把如图所示的战国青铜剑。该文物能保存至今的原因可能是

(2)《吕氏春秋·别类篇》载有“金柔锡柔,合两柔则刚”(注:此处“金”指铜),表明我们的祖先已认识到铜合金的硬度比纯铜
(二)碱式碳酸铜的热分解实验
某碱式碳酸铜成分可表示为Cua(OH)b(CO3)c,兴趣小组为探究其性质和组成,用如图装置控制一定温度使34.6g样品充分分解,观察到固体变成黑色。

(4)D装置的作用是
(5)停止加热后仍需继续通N2,可防止倒吸和
(6)测得实验前后各装置的质量变化如表所示。
| 温度/°C | 装置A | 装置B | 装置C |
| 实验前/g | 234.6 | 200.0 | 200.0 |
| 试验后/g | 224.0 | 201.8 | 208.8 |
②该碱式碳酸铜的化学式为
您最近一年使用:0次
2024·新疆·模拟预测
解题方法
6 . 填空
(1)市场上常见的苏打水有苏打气泡水和无汽苏打水两种。它们的主要成分中都含有碳酸氢钠,俗称_____ 。苏打气泡水中含有大量二氧化碳,瓶盖一打开就有大量气泡产生,所以叫气泡水。无汽苏打水则不含二氧化碳,但小明认为他喝入体内也会产生二氧化碳,主要原因是_____ (用化学方程式表示)。
某化学兴趣小组同学对碳酸氢钠产生了兴趣,于是对其性质进行探究。
【查阅资料】
①碳酸氢钠的溶解度如下:
②碳酸氢钠固体在潮湿的空气中久置或受热(50°C以上)分解均生成Na2CO3、H2O和CO2.
③很多浓酸稀释过程中都伴随着放热过程。
探究1:NaHCO3溶液与盐酸反应的热效应
室温下(20°C),边搅拌边向盛有0.5gNaHCO3固体的烧杯中加入10mL水,测得温度为18.5℃,恢复至室温后,向烧杯中加入过量10mL质量分数为20%的盐酸(20°C),搅拌,测得温度为20.8℃。
(2)实验中配制的NaHCO3溶液_____ (填“是”或“不是”)饱和溶液。
(3)由上述实验可知:NaHCO3固体溶于水_____ (填“放热”或“吸热”)。有同学认为由上述实验得出NaHCO3溶液与盐酸反应放热的结论并不可靠,理由是_____ 。
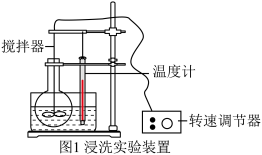
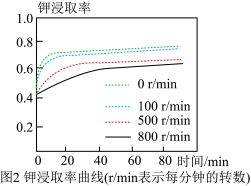
探究2:对碳酸钠、碳酸氢钠和稀盐酸的反应进行探究,实验装置如图1所示。
(4)由图像中信息得到结论:相同条件下,_____ 和稀盐酸反应产生二氧化碳较慢。请结合上表中的信息,分析得到这一结论的理由:_____ 。
探究3:久置的NaHCO3样品中NaHCO3含量的测定:
将一瓶在潮湿空气中久置的NaHCO3样品(假设只有NaHCO3和Na2CO3)混合均匀后,称取20.0g混合物,加热至恒重,称其质量为16.9g。
(5)计算样品中NaHCO3的质量分数_____ 。若上述测定过程中加热未至恒重,则测得NaHCO3的质量分数将_____ (填“偏大”、“偏小”或“无影响”)。
(1)市场上常见的苏打水有苏打气泡水和无汽苏打水两种。它们的主要成分中都含有碳酸氢钠,俗称
某化学兴趣小组同学对碳酸氢钠产生了兴趣,于是对其性质进行探究。
【查阅资料】
①碳酸氢钠的溶解度如下:
| 温度 | 10℃ | 20℃ | 30℃ | 40℃ |
| 溶解度 | 8.1g | 9.6g | 11.1g | 12.7g |
③很多浓酸稀释过程中都伴随着放热过程。
探究1:NaHCO3溶液与盐酸反应的热效应
室温下(20°C),边搅拌边向盛有0.5gNaHCO3固体的烧杯中加入10mL水,测得温度为18.5℃,恢复至室温后,向烧杯中加入过量10mL质量分数为20%的盐酸(20°C),搅拌,测得温度为20.8℃。
(2)实验中配制的NaHCO3溶液
(3)由上述实验可知:NaHCO3固体溶于水
探究2:对碳酸钠、碳酸氢钠和稀盐酸的反应进行探究,实验装置如图1所示。

| 滴入酚酞溶液 | 滴入稀盐酸,溶液颜色变化 | |
| 碳酸钠溶液 | 红色 | 红色→浅红色→无色 |
| 碳酸氢钠溶液 | 浅红色 | 浅红色→无色 |
(4)由图像中信息得到结论:相同条件下,
探究3:久置的NaHCO3样品中NaHCO3含量的测定:
将一瓶在潮湿空气中久置的NaHCO3样品(假设只有NaHCO3和Na2CO3)混合均匀后,称取20.0g混合物,加热至恒重,称其质量为16.9g。
(5)计算样品中NaHCO3的质量分数
您最近一年使用:0次
解题方法
7 . 《礼记》等文献中记载古人用草木灰制取氢氧化钾,用作纺织品漂洗剂等。某化学兴趣小组对草木灰的有关性质、成分、用途进行了如下探究。
【资料】
(a)草木灰是作物秸秆、枯枝等燃烧后的剩余灰烬,其中富含可溶性钾盐。
(b) 不溶于水,能与酸反应;
不溶于水,能与酸反应; 既不溶于水,也不能与酸反应。
既不溶于水,也不能与酸反应。
(1)任务一 探究草木灰的酸碱性________ (填写实验操作),得到滤液(草木灰水)。________ 转,浸取时间为________ 分钟,比较适宜。
③取少量上述草木灰水于试管中,滴加无色酚酞溶液,观察到溶液变为________ 色,证明草木灰水呈碱性。
(2)任务二 探究草木灰的成分
【猜想】草木灰中可能含 ,
, 中的一种或两种。
中的一种或两种。
【实验探究】
【反思评价】有同学认为步骤Ⅱ的实验结论不一定正确,理由是________ (用化学方程式表示)。
【实验改进与结论】
小组同学向步骤Ⅱ中得到的白色沉淀中滴加足量稀硝酸,观察到的现象是________ ,证明草木灰中含有碳酸钾,不含硫酸钾。
(3)任务三 模拟草木灰古法制碱
古人用草木灰制碱:将草木灰与氢氧化钙悬浊液混合生成氢氧化钾。
【资料】常温下 饱和溶液的pH为12.7,测得任务一中得到的草木灰水pH为11.3。
饱和溶液的pH为12.7,测得任务一中得到的草木灰水pH为11.3。
【实验模拟】同学们模拟古人制碱的原理,向盛有草木灰水的烧杯中,分3次加入氢氧化钙悬浊液,充分反应后,静置,分别测其溶液的pH变化后的数据如表。小组同学通过分析表中实验数据认为可以证明草木灰与氢氧化钙悬浊液混合后生成了氢氧化钾,依据是________ 。
【处理废液】向上述实验中的碱性废液中注入稀硫酸,搅拌,将pH调至约等于________ 后排放。
【资料】
(a)草木灰是作物秸秆、枯枝等燃烧后的剩余灰烬,其中富含可溶性钾盐。
(b)
 不溶于水,能与酸反应;
不溶于水,能与酸反应; 既不溶于水,也不能与酸反应。
既不溶于水,也不能与酸反应。(1)任务一 探究草木灰的酸碱性
③取少量上述草木灰水于试管中,滴加无色酚酞溶液,观察到溶液变为
(2)任务二 探究草木灰的成分
【猜想】草木灰中可能含
 ,
, 中的一种或两种。
中的一种或两种。【实验探究】
| 项目 | 实验步骤 | 实验现象 | 实验结论 |
| 方案 | Ⅰ.取少量草木灰水于试管中,滴加足量 | 有气泡产生 | 草木灰中含有碳酸钾 |
| Ⅱ.另取少量草木灰水于试管中,滴加足量氯化钡溶液 | 产生白色沉淀 | 草木灰中含有硫酸钾 |
【实验改进与结论】
小组同学向步骤Ⅱ中得到的白色沉淀中滴加足量稀硝酸,观察到的现象是
(3)任务三 模拟草木灰古法制碱
古人用草木灰制碱:将草木灰与氢氧化钙悬浊液混合生成氢氧化钾。
【资料】常温下
 饱和溶液的pH为12.7,测得任务一中得到的草木灰水pH为11.3。
饱和溶液的pH为12.7,测得任务一中得到的草木灰水pH为11.3。【实验模拟】同学们模拟古人制碱的原理,向盛有草木灰水的烧杯中,分3次加入氢氧化钙悬浊液,充分反应后,静置,分别测其溶液的pH变化后的数据如表。小组同学通过分析表中实验数据认为可以证明草木灰与氢氧化钙悬浊液混合后生成了氢氧化钾,依据是
| 次数 | 第1次 | 第2次 | 第3次 |
| pH | 12.2 | 13.2 | 14.0 |
您最近一年使用:0次
2024-05-26更新
|
149次组卷
|
4卷引用:2024年新疆乌鲁木齐5月检测中考物理、化学试卷-初中化学
2024年新疆乌鲁木齐5月检测中考物理、化学试卷-初中化学2024年新疆和田地区中考三模考试化学试题(已下线)2024年新疆中考化学真题变式题(非选择题14-16)(已下线)专题11 实验探究题-【好题汇编】5年(2020-2024)中考1年模拟化学真题分类汇编(新疆专用)
解题方法
8 . 我国青海湖地区素有“夏天晒盐,冬天捞碱”之说。已知氯化钠和碳酸钠的溶解度曲线如下图所示,下列说法正确的是
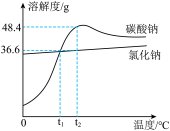
| A.碳酸钠的溶解度比氯化钠的溶解度大 |
B.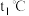 时,氯化钠饱和溶液的溶质质量分数为36.6% 时,氯化钠饱和溶液的溶质质量分数为36.6% |
C. 时,分别将质量均为20g的碳酸钠、氯化钠固体加入50g水中充分溶解,均可得到不饱和溶液 时,分别将质量均为20g的碳酸钠、氯化钠固体加入50g水中充分溶解,均可得到不饱和溶液 |
| D.夏天晒盐的原理是氯化钠的溶解度受温度影响小,夏天温度高,水分蒸发快,氯化钠易结晶析出 |
您最近一年使用:0次
解题方法
9 . 某学习小组定期用营养液浇灌教室内养殖的绿萝。在观察绿萝生长状况时,决定研究重金属对植物生长的影响。
【查阅资料】I.重金属原义是指比重大于5的金属,包括金、银、铜、钡等;
Ⅱ.重金属因为难以被生物分解或排出而积累在生物体内,造成慢性中毒;
Ⅲ.BaCl2为白色晶体,可溶于水,是一种具有毒性的盐。
该小组首先研究了CuSO4对植物生长的影响。
任务一:配制CuSO4溶液。
(1)每次施用的浇灌液均为100mL,配液方案如下:(本研究所用溶液很稀,密度均近似看作1g/cm3)
为了获得严谨的结论,合理设计盆4的配液方案:ω=___________ ,b=___________ 。
(2)该小组还研究了BaCl2对植物生长的影响。研究结束后该小组将未用完的BaCl2溶液和CuSO4溶液直接混合,准备做无害化处理。混合后产生大量白色沉淀,反应的化学方程式为___________ 。
任务二:
探究无害化处理,过滤后所得蓝色滤液中含有的溶质成分。
(3)猜想一:只有CuCl2 猜想二:CuCl2和BaCl2 猜想三:___________
【探究过程】
(4)确定蓝色滤液的成分,试验方案如下表,将表中内容补充完整:
【拓展延伸】
(5)CuSO4是农药波尔多液的配制原料之一,不能用铁质容器盛放波尔多液的原因是______ 。
【查阅资料】I.重金属原义是指比重大于5的金属,包括金、银、铜、钡等;
Ⅱ.重金属因为难以被生物分解或排出而积累在生物体内,造成慢性中毒;
Ⅲ.BaCl2为白色晶体,可溶于水,是一种具有毒性的盐。
该小组首先研究了CuSO4对植物生长的影响。
任务一:配制CuSO4溶液。
(1)每次施用的浇灌液均为100mL,配液方案如下:(本研究所用溶液很稀,密度均近似看作1g/cm3)
| 编号 | 浇灌液中CuSO4的浓度/% | 总体积/mL | 5% CuSO4溶液的用量/mL | 水的用量/mL |
| 盆1 | 5 | 100 | 100 | 0 |
| 盆2 | 3 | 100 | 60 | 40 |
| 盆3 | 1 | 100 | 20 | 80 |
| 盆4 | ω | 100 | 0 | b |
(2)该小组还研究了BaCl2对植物生长的影响。研究结束后该小组将未用完的BaCl2溶液和CuSO4溶液直接混合,准备做无害化处理。混合后产生大量白色沉淀,反应的化学方程式为
任务二:
探究无害化处理,过滤后所得蓝色滤液中含有的溶质成分。
(3)猜想一:只有CuCl2 猜想二:CuCl2和BaCl2 猜想三:
【探究过程】
(4)确定蓝色滤液的成分,试验方案如下表,将表中内容补充完整:
| 实验操作 | 实验现象 | 实验结论 | |
| ① | 取少量滤液于试管中, | 无明显现象 | 猜想二不成立 |
| ② | 猜想三成立 |
【拓展延伸】
(5)CuSO4是农药波尔多液的配制原料之一,不能用铁质容器盛放波尔多液的原因是
您最近一年使用:0次
名校
解题方法
10 . “侯氏制碱法”生产纯碱的主要反应是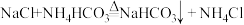 。如图是三种固体物质的溶解度曲线。下列说法正确的是
。如图是三种固体物质的溶解度曲线。下列说法正确的是
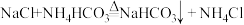 。如图是三种固体物质的溶解度曲线。下列说法正确的是
。如图是三种固体物质的溶解度曲线。下列说法正确的是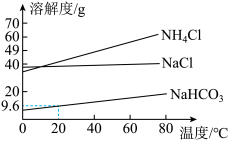
| A.20℃时,NaHCO3饱和溶液一定比NH4Cl饱和溶液的溶质质量分数大 |
| B.20℃时,100g水中加入5.85gNaCl固体和7.9gNH4HCO3固体,一定有晶体析出 |
| C.该反应成功的关键是20℃时NaHCO3在水中的溶解度要比NH4Cl、NaCl小的多 |
| D.若固体NH4Cl中含有少量NaCl,可用蒸发结晶的方法提纯NH4Cl |
您最近一年使用:0次
2024-04-12更新
|
132次组卷
|
12卷引用:2022年新疆乌鲁木齐市第四十四中学中考一模化学试题
2022年新疆乌鲁木齐市第四十四中学中考一模化学试题2022年江苏省苏州市昆山、太仓、常熟、张家港市联考中考模拟化学试题2022年江苏省昆山、太仓、常熟、张家港市中考适应性考试化学试题2022年江苏省常州市中考适应性练习(三模)化学试题(已下线)专题06 溶液和溶解度-5年(2018-2022)中考1年模拟化学分项汇编(江苏苏州专用)2023年江苏省苏州市立达中学校中考一模化学试题2023年江苏省海安市海陵中学中考一模化学试题2023年江苏省扬州市邗江区梅玲中学中考二模化学试题江苏省高邮市高邮镇2022-2023学年九年级下学期4月月考化学试题(已下线)【金榜卷】2024年化学中考一模全真模拟卷A(南通专用)江苏省南通市部分学校2023-2024学年九年级下学期3月月考化学试卷(已下线)押南通卷第8-10题 单项选择题-备战2024年中考化学临考题号押题(南通专用)