1 . 干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质。某研究小组对一只干燥管里的碱石灰样品的成分进行实验探究。
猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠;
猜想Ⅱ:已经部分变质,可能情况未知;
猜想Ⅲ:完全变质,且只含有碳酸钙和碳酸钠。
【实验探究】
①取样品,加入几滴清水,试管外壁不发烫;
②取样品,加入足量清水和几滴酚酞溶液,充分搅拌并过滤,得到白色沉淀a和红色滤液b;在红色滤液b和白色沉淀a中分别加入足量稀盐酸,都有气泡产生。
(1)请写出白色沉淀a中加稀盐酸产生气泡的方程式______ 。
【分析过程】
(2)根据实验①说明猜想______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)不成立。
(3)根据实验②,甲同学认为猜想Ⅲ成立,乙同学不同意,他认为碱石灰样品中不一定含有碳酸钙,可能是加水时两种物质反应生成的碳酸钙(请用方程式解释)______ 。
(4)为进一步确定猜想,他们设计了以下实验方案:
【实验结论】甲、乙同学完成设计的实验方案后,证明了猜想Ⅱ成立。
【实验反思】
(5)根据上述实验,下列说法正确的是______(填序号)。

猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠;
猜想Ⅱ:已经部分变质,可能情况未知;
猜想Ⅲ:完全变质,且只含有碳酸钙和碳酸钠。
【实验探究】
①取样品,加入几滴清水,试管外壁不发烫;
②取样品,加入足量清水和几滴酚酞溶液,充分搅拌并过滤,得到白色沉淀a和红色滤液b;在红色滤液b和白色沉淀a中分别加入足量稀盐酸,都有气泡产生。
(1)请写出白色沉淀a中加稀盐酸产生气泡的方程式
【分析过程】
(2)根据实验①说明猜想
(3)根据实验②,甲同学认为猜想Ⅲ成立,乙同学不同意,他认为碱石灰样品中不一定含有碳酸钙,可能是加水时两种物质反应生成的碳酸钙(请用方程式解释)
(4)为进一步确定猜想,他们设计了以下实验方案:
| 实验方案 | 实验现象 | 分析 |
| 另取红色滤液b,加入过量的 | 若产生白色沉淀,溶液仍然呈红色 | 滤液中含有 |
【实验结论】甲、乙同学完成设计的实验方案后,证明了猜想Ⅱ成立。
【实验反思】
(5)根据上述实验,下列说法正确的是______(填序号)。
| A.上述实验可以证明该碱石灰固体中有氢氧化钠 |
| B.若在上述红色滤液中加入少量稀盐酸,可能无气泡产生 |
| C.上述实验证明了原碱石灰样品中一定不含Ca(OH)2 |
| D.根据实验可知,碱石灰样品是部分变质,变质后的固体成分有2种可能性 |
您最近一年使用:0次
名校
解题方法
2 . 下列是相关物质的转化图,(“→”表示反应一步实现,部分物质和反应条件已略去)。下列说法错误的是
Cu Cu(NO3)2
Cu(NO3)2 Mg(NO3)2
Mg(NO3)2 MgSO4
MgSO4 Mg(OH)2
Mg(OH)2
Cu
 Cu(NO3)2
Cu(NO3)2 Mg(NO3)2
Mg(NO3)2 MgSO4
MgSO4 Mg(OH)2
Mg(OH)2| A.反应①可以是置换反应 |
| B.反应②可以证明Mg活动性强于Cu |
| C.反应③不能一步实现 |
| D.反应④可能是MgSO4+Cu(OH)2=Mg(OH)2↓+CuSO4 |
您最近一年使用:0次
3 . 已知:Al(OH)3沉淀可溶于NaOH溶液,现向100gHCl和AlCl3的混合溶液中分5次加入100gNaOH溶液,产生沉淀的质量与所加NaOH溶液的质量关系如下表所示.回答下列问题:
(1)第1次加入NaOH溶液不产生沉淀的原因是______ (用化学方程式表示)。
(2)所用NaOH溶液的溶质质量分数是多少?(写出计算过程)
(3)当沉淀质量达到最大值时,若将混合溶液过滤,则滤液中NaCl的质量分数是多少?(结果精确到 )。
)。
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
NaOH溶液质量 | 20 | 20 | 20 | 20 | 20 |
沉淀质量 | 0 | 2.6 | 5.2 | 7.8 | 0 |
(1)第1次加入NaOH溶液不产生沉淀的原因是
(2)所用NaOH溶液的溶质质量分数是多少?(写出计算过程)
(3)当沉淀质量达到最大值时,若将混合溶液过滤,则滤液中NaCl的质量分数是多少?(结果精确到
 )。
)。
您最近一年使用:0次
4 . 干燥剂“碱石灰”是氧化钙和氢氧化钠的混合物,在空气中容易变质。某研究小组对一只干燥管里的碱石灰样品的成分进行实验探究。

【提出猜想】
猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠;
猜想Ⅱ:已经部分变质,可能情况未知;
猜想Ⅲ:完全变质,且只含有碳酸钙和碳酸钠;
【实验探究】
(1)取样品,加入几滴清水,试管外壁不发烫;
(2)取样品,加入足量清水和几滴酚酞溶液,充分搅拌并过滤,得到白色沉淀和红色滤液;
【分析过程】
根据实验(1)说明猜想______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)不成立。根据实验(2),甲同学认为猜想Ⅲ成立,乙同学不同意,他认为碱石灰样品中不一定含有碳酸钙,可能是实验(2)中新生成的,他的理由是______ (请写化学方程式)。
为进一步确定猜想,他们设计了以下实验方案:
【实验结论】甲、乙同学完成设计的实验方案后,证明了猜想Ⅱ成立。
【实验反思】根据上述实验,下列说法正确的是______ (填序号)。
A.过滤后得到的红色滤液中的溶质只有 3 种可能的组合
B.表格中的方案①,若通入的 CO2适量,溶液可能由红色变成无色
C.实验证明了原碱石灰样品中一定不含 CaCO3
D.根据实验可知,碱石灰样品的变质情况有 2 种可能性

【提出猜想】
猜想Ⅰ:没有变质,只含有氧化钙和氢氧化钠;
猜想Ⅱ:已经部分变质,可能情况未知;
猜想Ⅲ:完全变质,且只含有碳酸钙和碳酸钠;
【实验探究】
(1)取样品,加入几滴清水,试管外壁不发烫;
(2)取样品,加入足量清水和几滴酚酞溶液,充分搅拌并过滤,得到白色沉淀和红色滤液;
【分析过程】
根据实验(1)说明猜想
为进一步确定猜想,他们设计了以下实验方案:
| 实验方案 | 实验现象 | 分析 |
| ①取红色滤液,通入一 定量的 CO2气体 | 若产生 | 滤液中含有 Ca(OH)2 |
| ②取红色滤液,加入过量 的 | 若产生白色沉淀,溶液仍然呈红色 | 滤液中含有 |
| 若产生白色沉淀,溶液呈无色 | 滤液中只含 Na2CO3 |
【实验反思】根据上述实验,下列说法正确的是
A.过滤后得到的红色滤液中的溶质只有 3 种可能的组合
B.表格中的方案①,若通入的 CO2适量,溶液可能由红色变成无色
C.实验证明了原碱石灰样品中一定不含 CaCO3
D.根据实验可知,碱石灰样品的变质情况有 2 种可能性
您最近一年使用:0次
解题方法
5 . 草酸亚铁(FeC2O4)是生产锂电池的原料,在加热条件下能发生分解。某兴趣小组为探究其分解产物设计了如下图实验。在装置A中加入14.4g草酸亚铁,加热至固体质量不再变化,生成气体和黑色固体。实验过程中持续通入干燥的N2确保装置中无O2存在(部分装置略去)。

探究一:草酸亚铁受热分解的气体产物
【猜想假设】甲同学认为气体产物可能为CO2、CO中的一种或两种。
【实验分析】
(1)判断气体产物是否有CO2,应观察装置______ (填“B”或“E”)中的澄清石灰水是否变浑浊。
(2)随着实验进行,甲同学观察到B、E中澄清石灰水均变浑浊,D中有红色固体生成,写出D装置玻璃管中发生反应的化学方程式______ 。
【得出结论】
(3)气体产物成分为_______ (填化学式)。
探究二:草酸亚铁晶体受热分解的固体产物
【查阅资料】铁粉、FeO、Fe3O4均为黑色固体。
(4)为判断生成的黑色固体成分,乙同学将该固体分为两等份,向其中一份滴加稀盐酸,若观察到___ 现象,可以判断不含铁粉。
【猜想假设】根据元素组成和颜色,对黑色固体成分提出以下猜想:猜想1:FeO;猜想2:Fe3O4;猜想3:FeO和Fe3O4的混合物
【实验探究】
(5)丙同学称量另一份黑色固体的质量为3.6g,通过计算证明猜想______ 成立(填数字)。
【得出结论】
(6)FeC2O4受热分解的化学方程式为_____ 。

探究一:草酸亚铁受热分解的气体产物
【猜想假设】甲同学认为气体产物可能为CO2、CO中的一种或两种。
【实验分析】
(1)判断气体产物是否有CO2,应观察装置
(2)随着实验进行,甲同学观察到B、E中澄清石灰水均变浑浊,D中有红色固体生成,写出D装置玻璃管中发生反应的化学方程式
【得出结论】
(3)气体产物成分为
探究二:草酸亚铁晶体受热分解的固体产物
【查阅资料】铁粉、FeO、Fe3O4均为黑色固体。
(4)为判断生成的黑色固体成分,乙同学将该固体分为两等份,向其中一份滴加稀盐酸,若观察到
【猜想假设】根据元素组成和颜色,对黑色固体成分提出以下猜想:猜想1:FeO;猜想2:Fe3O4;猜想3:FeO和Fe3O4的混合物
【实验探究】
(5)丙同学称量另一份黑色固体的质量为3.6g,通过计算证明猜想
【得出结论】
(6)FeC2O4受热分解的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 重庆一中某化学小组在鱼塘旁发现一包久置的高纯过氯化钙(杂质忽略不计),为研究其性质及变质情况,取样完成了如下探究实验。
【查阅资料】过氧化钙(CaO2)是一种供氧剂,常用于鱼类养殖。
过氧化钙与水反应的化学方程式为: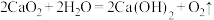
【提出猜想】小鹏对久置的过氧化钙样品的变质情况提出了如下猜想:
猜想①:完全变质,只有CaCO3
猜想②:已变质,但具体情况待确定
猜想③:未变质,只有CaO2
(1)请用化学方程式解释变质生成CaCO3的原因_______ 。
【定性实验】
步骤一:取过氧化钙样品于烧杯,加入足量稀盐酸,有气泡产生。
步骤二:取过氧化钙样品于烧杯,加入足量水和几滴酚酞,缓慢产生气泡,充分反应得到红色澄清溶液。
(2)根据步骤一的现象,小鹏认为原样品中一定有CaCO3,小理不同意该说法,原因是_______ 。
(3)根据步骤二的现象,小鹏认为猜想_______ (填序号)不成立。
【定量实验】为进一步探究样品变质情况,小蔚设计了如下实验:
步骤三:取质量为X的过氧化钙样品于烧杯,加入足量水,充分搅拌后再加入过量碳酸钠溶液,反应完全后过滤、洗涤、干燥,称得沉淀质量为50g。
步骤四:取质量为Y的过氧化钙样品于锥形瓶,加入足量水,充分反应后测得产生气体(其密度为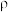 g/mL)的体积为VmL。
g/mL)的体积为VmL。
(4)步骤三中为检验沉淀是否洗净,可取最后一次洗涤液于试管加入_______(填序号)。
(5)步骤四中Y的取值范围是______ (用含V、 的式子表示)。
的式子表示)。
【实验结论】猜想②成立
【实验反思】
(6)下列关于上述实验的说法不正确的是______(填序号)
【查阅资料】过氧化钙(CaO2)是一种供氧剂,常用于鱼类养殖。
过氧化钙与水反应的化学方程式为:
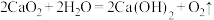
【提出猜想】小鹏对久置的过氧化钙样品的变质情况提出了如下猜想:
猜想①:完全变质,只有CaCO3
猜想②:已变质,但具体情况待确定
猜想③:未变质,只有CaO2
(1)请用化学方程式解释变质生成CaCO3的原因
【定性实验】
步骤一:取过氧化钙样品于烧杯,加入足量稀盐酸,有气泡产生。
步骤二:取过氧化钙样品于烧杯,加入足量水和几滴酚酞,缓慢产生气泡,充分反应得到红色澄清溶液。
(2)根据步骤一的现象,小鹏认为原样品中一定有CaCO3,小理不同意该说法,原因是
(3)根据步骤二的现象,小鹏认为猜想
【定量实验】为进一步探究样品变质情况,小蔚设计了如下实验:
步骤三:取质量为X的过氧化钙样品于烧杯,加入足量水,充分搅拌后再加入过量碳酸钠溶液,反应完全后过滤、洗涤、干燥,称得沉淀质量为50g。
步骤四:取质量为Y的过氧化钙样品于锥形瓶,加入足量水,充分反应后测得产生气体(其密度为
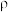 g/mL)的体积为VmL。
g/mL)的体积为VmL。(4)步骤三中为检验沉淀是否洗净,可取最后一次洗涤液于试管加入_______(填序号)。
| A.Fe2O3 | B.NH4Cl溶液 | C.Ba(NO3)2溶液 | D.稀硫酸 |
 的式子表示)。
的式子表示)。【实验结论】猜想②成立
【实验反思】
(6)下列关于上述实验的说法不正确的是______(填序号)
| A.步骤一可以省略不做 |
| B.步骤二中溶液呈红色,则原样品中一定有Ca(OH)2 |
| C.若步骤三中36g<X<37g,则样品已变质且为CaO2和Ca(OH)2的混合物 |
| D.步骤四可以省略不做 |
您最近一年使用:0次
名校
解题方法
7 . 硫代硫酸钠(Na2S2O3)有抗过敏作用,临床上常用于治疗皮肤瘙痒,荨麻疹等。某硫代硫酸钠的样品中混有少量硫酸钠,现取16g该样品,加入适量稀硫酸,发生反应的化学方程式为: 。充分反应后,得到只含有一种溶质的不饱和溶液,其溶质质量分数为10%.同时生成3.2g硫。计算:
。充分反应后,得到只含有一种溶质的不饱和溶液,其溶质质量分数为10%.同时生成3.2g硫。计算:
(1)硫代硫酸钠中钠、硫元素质量比为_______ 。
(2)该样品中硫代硫酸钠的质量为_______ 。
(3)所用稀硫酸的溶质质量分数(计算结果精确到0.1%)。
 。充分反应后,得到只含有一种溶质的不饱和溶液,其溶质质量分数为10%.同时生成3.2g硫。计算:
。充分反应后,得到只含有一种溶质的不饱和溶液,其溶质质量分数为10%.同时生成3.2g硫。计算:(1)硫代硫酸钠中钠、硫元素质量比为
(2)该样品中硫代硫酸钠的质量为
(3)所用稀硫酸的溶质质量分数(计算结果精确到0.1%)。
您最近一年使用:0次
解题方法
8 . 食盐、苏打、食醋和生石灰是生活中常见的物质,实验小组进行了如下实验探究。
【活动一】
(1)选用上述物质中的_____ 做食品干燥剂(填化学式)。
【活动二】
(2)实验小组通过如图1所示的两组实验(其中A、B一组,C、D一组)鉴别氯化钠溶液和碳酸钠溶液。
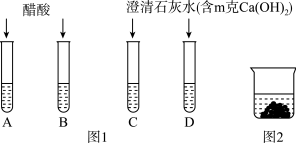
实验现象:试管B内产生气泡,试管D变浑浊,则试管D内反应的化学方程式为_____ 。
【活动三】
(3)实验小组将试管B和试管D反应后的上层清液倒在烧杯中,发现有白色沉淀生成如图2,实验小组对烧杯内上层废液的成分产生了探究兴趣。
【提出问题】废液中含有哪些溶质?
【查阅资料】①常温下醋酸盐可溶于水
②
【猜想与假设】猜想①:CH3COONa、NaOH
猜想②:CH3COONa、NaOH、Na2CO3
猜想③:_____
【进行实验】取废液少许于试管中,再向其中加入足量的氯化钡溶液,实验现象为_____ 。
【得出结论】猜想②正确。
【反思交流】
(4)实验小组利用活动二结束后试管A中的废液除去某水垢(主要成分为氢氧化镁),其反应的化学方程式为_____ 。
(5)实验小组想确定活动二试管C中是否发生了化学反应,现将活动二结束后试管C的溶液分成两等份。第一份溶液中加入过量的纯碱溶液得到a克沉淀,第二份溶液中加入过量硝酸镁溶液得到b克沉淀,当m=_____ (用a、b表示并化简)时说明进行活动二时C试管内没有发生化学反应。
【活动一】
(1)选用上述物质中的
【活动二】
(2)实验小组通过如图1所示的两组实验(其中A、B一组,C、D一组)鉴别氯化钠溶液和碳酸钠溶液。

实验现象:试管B内产生气泡,试管D变浑浊,则试管D内反应的化学方程式为
【活动三】
(3)实验小组将试管B和试管D反应后的上层清液倒在烧杯中,发现有白色沉淀生成如图2,实验小组对烧杯内上层废液的成分产生了探究兴趣。
【提出问题】废液中含有哪些溶质?
【查阅资料】①常温下醋酸盐可溶于水
②

【猜想与假设】猜想①:CH3COONa、NaOH
猜想②:CH3COONa、NaOH、Na2CO3
猜想③:
【进行实验】取废液少许于试管中,再向其中加入足量的氯化钡溶液,实验现象为
【得出结论】猜想②正确。
【反思交流】
(4)实验小组利用活动二结束后试管A中的废液除去某水垢(主要成分为氢氧化镁),其反应的化学方程式为
(5)实验小组想确定活动二试管C中是否发生了化学反应,现将活动二结束后试管C的溶液分成两等份。第一份溶液中加入过量的纯碱溶液得到a克沉淀,第二份溶液中加入过量硝酸镁溶液得到b克沉淀,当m=
您最近一年使用:0次
9 . 实验室现有一包白色固体,可能由Na2CO3、Na2SO4、CuSO4和NaCl中的一种或几种组成,为探究其成分做了如下实验并记录实验现象:
①取该白色固体样品溶于水,得到无色溶液;
②取适量上述溶液加入过量的BaCl2溶液,出现白色沉淀,再过滤;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀全部消失并有气泡产生。
则下列分析中正确的是
①取该白色固体样品溶于水,得到无色溶液;
②取适量上述溶液加入过量的BaCl2溶液,出现白色沉淀,再过滤;
③向步骤②所得沉淀中加入过量的稀HNO3,沉淀全部消失并有气泡产生。
则下列分析中正确的是
| A.原固体中一定含有Na2CO3,可能含有CuSO4和NaCl |
| B.原固体中一定不含Na2SO4和CuSO4,可能含有NaCl |
| C.原固体中一定含有Na2CO3和Na2SO4,一定不含CuSO4 |
| D.若在步骤②所得滤液中滴人AgNO3溶液,出现白色沉淀,则原固体中一定含有NaCl |
您最近一年使用:0次
2023-04-24更新
|
441次组卷
|
7卷引用:重庆市九龙坡区实验外国语学校2019-2020学年九年级下学期第一次月考化学试题
名校
10 . 下列图像能正确反映其对应操作中各量变化关系的是
A.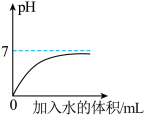 向pH为1的硫酸加水稀释 向pH为1的硫酸加水稀释 |
B.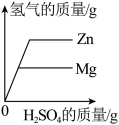 分别向等质量的镁和锌中加入等浓度的稀硫酸至过量 分别向等质量的镁和锌中加入等浓度的稀硫酸至过量 |
C.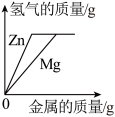 分别向等体积、等浓度的两杯稀盐酸中加入镁和铁至过量 分别向等体积、等浓度的两杯稀盐酸中加入镁和铁至过量 |
D.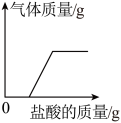 部分变质的NaOH溶液中滴加足量的稀盐酸 部分变质的NaOH溶液中滴加足量的稀盐酸 |
您最近一年使用:0次



