名校
1 . 化学是一门以实验为基础的科学。
(1)根据下列装置图回答:________ 。
②实验室用高锰酸钾制取并收集一瓶干燥的氧气,应选用的装置为________ (填序号),反应的化学方程式为________ 。
③实验室用石灰石和稀盐酸制取二氧化碳,并将生成的二氧化碳通入紫色石蕊溶液中,观察到溶液由紫色变成________ 色。
(2)下列选项中,由实验及现象推出相应结论正确的是________ (填序号)。
(1)根据下列装置图回答:
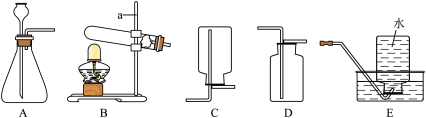
②实验室用高锰酸钾制取并收集一瓶干燥的氧气,应选用的装置为
③实验室用石灰石和稀盐酸制取二氧化碳,并将生成的二氧化碳通入紫色石蕊溶液中,观察到溶液由紫色变成
(2)下列选项中,由实验及现象推出相应结论正确的是
| 选项 | A | B | C |
| 实验 |
|
|
|
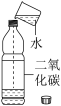
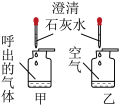
| 现象 | 有气泡冒出,触摸试管外壁,感觉放热 | 旋紧瓶塞,振荡,软塑料瓶变瘪 | 甲瓶中出现白色浑浊乙瓶中无明显现象 |
| 结论 | 化学反应在生成新物质的同时,伴随着能量变化 | 二氧化碳能与水反应 | 人体呼出的气体中二氧化碳的含量高于空气中二氧化碳的含量 |
您最近一年使用:0次
2 . 氢能是绿色的低碳能源。下图是“制氢、储氢、释氢、用氢”的示意图。
查询资料:沸点: -196℃
-196℃  -252℃
-252℃________ 极产生。
(2)步骤②属于的基本反应类型是________ 反应。
(3)步骤③是新能源汽车氢氧燃料电池的反应原理,反应的化学方程式为________ 。
(4)在释氢过程中,可利用________ 不同将氢气和氮气分离。
(5)氢气作为能源,越来越受到人们关注,是因为________。
查询资料:沸点:
 -196℃
-196℃  -252℃
-252℃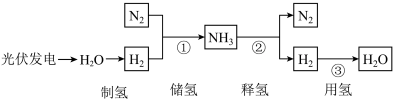
(2)步骤②属于的基本反应类型是
(3)步骤③是新能源汽车氢氧燃料电池的反应原理,反应的化学方程式为
(4)在释氢过程中,可利用
(5)氢气作为能源,越来越受到人们关注,是因为________。
| A.本身无毒 | B.来源广 | C.热值高 | D.产物无污染 |
您最近一年使用:0次
名校
3 . 白铅矿(主要成分是 )是炼铅的主要原料。为探究其性质,小鲁同学取
)是炼铅的主要原料。为探究其性质,小鲁同学取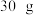 白铅矿(杂质不溶于水且不参与反应)于烧杯中,加入
白铅矿(杂质不溶于水且不参与反应)于烧杯中,加入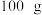 稀硝酸,恰好完全反应,烧杯中残留
稀硝酸,恰好完全反应,烧杯中残留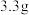 固体。再继续向烧杯中滴加某未知浓度的
固体。再继续向烧杯中滴加某未知浓度的 溶液,烧杯内固体质量随加入
溶液,烧杯内固体质量随加入 溶液的质量变化关系如图所示,A点时消耗了
溶液的质量变化关系如图所示,A点时消耗了 氢氧化钠溶液。
氢氧化钠溶液。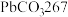 ;
; ;
;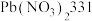 ;
;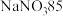 )
)
提示:①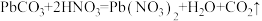 ;②
;②
求:
(1) 中氧元素与碳元素的质量比为
中氧元素与碳元素的质量比为________ 。
(2)所取白铅矿中 的质量为
的质量为________ 。
(3)A点对应的反应后溶液的溶质质量分数是多少?(写出计算过程,结果保留1位小数)
 )是炼铅的主要原料。为探究其性质,小鲁同学取
)是炼铅的主要原料。为探究其性质,小鲁同学取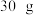 白铅矿(杂质不溶于水且不参与反应)于烧杯中,加入
白铅矿(杂质不溶于水且不参与反应)于烧杯中,加入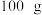 稀硝酸,恰好完全反应,烧杯中残留
稀硝酸,恰好完全反应,烧杯中残留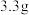 固体。再继续向烧杯中滴加某未知浓度的
固体。再继续向烧杯中滴加某未知浓度的 溶液,烧杯内固体质量随加入
溶液,烧杯内固体质量随加入 溶液的质量变化关系如图所示,A点时消耗了
溶液的质量变化关系如图所示,A点时消耗了 氢氧化钠溶液。
氢氧化钠溶液。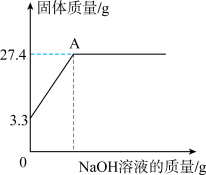
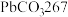 ;
; ;
;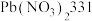 ;
;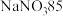 )
)提示:①
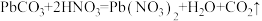 ;②
;②
求:
(1)
 中氧元素与碳元素的质量比为
中氧元素与碳元素的质量比为(2)所取白铅矿中
 的质量为
的质量为(3)A点对应的反应后溶液的溶质质量分数是多少?(写出计算过程,结果保留1位小数)
您最近一年使用:0次
4 . 学习了酸碱盐之后,化学兴趣小组的同学开展了利用紫甘蓝制作酸碱指示剂的项目式学习。
【查阅资料】
①紫甘蓝汁液的变色范围如表:
②饱和 溶液的
溶液的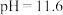
【活动一】制取试剂
利用紫甘蓝自制酸碱指示剂的步骤依次为:研碎→酒精浸泡→过滤→装瓶。
(1)提取紫甘蓝的汁液,需用酒精浸泡而不用水的原因是________ 。
【活动二】应用试剂
同学们用自制的紫甘蓝汁液验证中和反应:取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,观察到溶液由无色变为黄色;再逐滴加入稀盐酸,溶液从上至下依次呈现不同的颜色,宛若彩虹,非常美丽。
【提出问题】为什么在反应过程中溶液中的紫甘蓝汁液会呈现多彩的颜色呢?
【进行猜想】可能是反应过程中,溶液中各部位的酸碱度(pH)不同。
【实验探究】
(2)为验证猜想,同学们设计如下实验方案:另取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,逐滴加入盐酸,边滴加边振荡,观察溶液的颜色变化,同时测量________ 。
【得出结论】猜想正确
【交流反思】
(3)氢氧化钠溶液与稀盐酸反应的化学方程式为________ 。
(4)取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,再逐滴加入稀盐酸充分振荡,溶液最终变成________ 色,说明氢氧化钠与盐酸发生了中和反应。
【活动三】拓展延伸
老师向滴有紫甘蓝汁液的稀盐酸和 的混合溶液中,逐滴加入饱和
的混合溶液中,逐滴加入饱和 溶液,反应所得沉淀或气体的质量变化如图所示。
溶液,反应所得沉淀或气体的质量变化如图所示。 溶液质量为
溶液质量为 时,所得溶液中除指示剂外还含有的溶质是
时,所得溶液中除指示剂外还含有的溶质是________ (填化学式)。
(6)加入饱和 溶液质量由0至bg的过程中,溶液颜色的变化情况是
溶液质量由0至bg的过程中,溶液颜色的变化情况是________ 。
【查阅资料】
①紫甘蓝汁液的变色范围如表:
 | 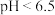 | 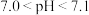 | 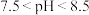 | 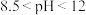 | 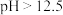 |
| 紫甘蓝汁液 | 粉红色 | 紫色 | 蓝色 | 绿色 | 黄色 |
 溶液的
溶液的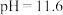
【活动一】制取试剂
利用紫甘蓝自制酸碱指示剂的步骤依次为:研碎→酒精浸泡→过滤→装瓶。
(1)提取紫甘蓝的汁液,需用酒精浸泡而不用水的原因是
【活动二】应用试剂
同学们用自制的紫甘蓝汁液验证中和反应:取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,观察到溶液由无色变为黄色;再逐滴加入稀盐酸,溶液从上至下依次呈现不同的颜色,宛若彩虹,非常美丽。
【提出问题】为什么在反应过程中溶液中的紫甘蓝汁液会呈现多彩的颜色呢?
【进行猜想】可能是反应过程中,溶液中各部位的酸碱度(pH)不同。
【实验探究】
(2)为验证猜想,同学们设计如下实验方案:另取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,逐滴加入盐酸,边滴加边振荡,观察溶液的颜色变化,同时测量
【得出结论】猜想正确
【交流反思】
(3)氢氧化钠溶液与稀盐酸反应的化学方程式为
(4)取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,再逐滴加入稀盐酸充分振荡,溶液最终变成
【活动三】拓展延伸
老师向滴有紫甘蓝汁液的稀盐酸和
 的混合溶液中,逐滴加入饱和
的混合溶液中,逐滴加入饱和 溶液,反应所得沉淀或气体的质量变化如图所示。
溶液,反应所得沉淀或气体的质量变化如图所示。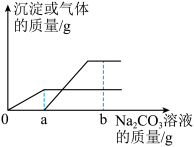
 溶液质量为
溶液质量为 时,所得溶液中除指示剂外还含有的溶质是
时,所得溶液中除指示剂外还含有的溶质是(6)加入饱和
 溶液质量由0至bg的过程中,溶液颜色的变化情况是
溶液质量由0至bg的过程中,溶液颜色的变化情况是
您最近一年使用:0次
5 . 煤化工废水中含有较多 和少量
和少量 、
、 ,三种物质的溶解度曲线如图所示。
,三种物质的溶解度曲线如图所示。 :
:
①采取的结晶方法是_______ (填“降温结晶”或“蒸发结晶”)。
②用6%的 溶液(密度约为
溶液(密度约为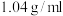 )配制
)配制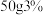 的
的 溶液,主要涉及以下操作:a.计算;b.
溶液,主要涉及以下操作:a.计算;b._______ ;c.混匀;d.装瓶。
(2) ℃时,某
℃时,某 溶液中溶质和溶剂的质量比为2:3,则该溶液是
溶液中溶质和溶剂的质量比为2:3,则该溶液是_______ (填“饱和”或“不饱和”)溶液。
(3) ℃时,将等质量的饱和
℃时,将等质量的饱和 溶液和
溶液和 溶液分别降温至
溶液分别降温至 ℃,以下对所得溶液的分析正确的是_______(填字母)。
℃,以下对所得溶液的分析正确的是_______(填字母)。
 和少量
和少量 、
、 ,三种物质的溶解度曲线如图所示。
,三种物质的溶解度曲线如图所示。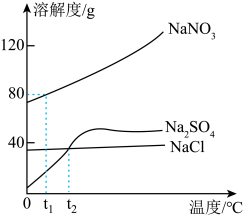
 :
:①采取的结晶方法是
②用6%的
 溶液(密度约为
溶液(密度约为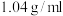 )配制
)配制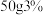 的
的 溶液,主要涉及以下操作:a.计算;b.
溶液,主要涉及以下操作:a.计算;b.(2)
 ℃时,某
℃时,某 溶液中溶质和溶剂的质量比为2:3,则该溶液是
溶液中溶质和溶剂的质量比为2:3,则该溶液是(3)
 ℃时,将等质量的饱和
℃时,将等质量的饱和 溶液和
溶液和 溶液分别降温至
溶液分别降温至 ℃,以下对所得溶液的分析正确的是_______(填字母)。
℃,以下对所得溶液的分析正确的是_______(填字母)。A.溶剂质量的大小关系是 |
B.溶液质量的大小关系是 |
C.溶质质量分数的大小关系是 |
您最近一年使用:0次
6 . 农业对于人类社会的生存和发展具有重要意义,农业生产与化学息息相关。
(1)大棚建造时使用钢管作框架结构,钢属于_______ (填“金属材料”或“合成材料”)。
(2)“杂交水稻之父”袁隆平培育出的某种水稻中富含硒,这里的“硒”指的是_______(填序号)。
(3)农药波尔多液可防治果树、马铃薯等作物的真菌病害,利用石灰浆和硫酸铜溶液制波尔多液时发生的化学方程式是_______ 。
(4)农业生产强调绿色发展,下列做法中不利于保护生态环境的是______(填序号)。
(1)大棚建造时使用钢管作框架结构,钢属于
(2)“杂交水稻之父”袁隆平培育出的某种水稻中富含硒,这里的“硒”指的是_______(填序号)。
| A.硒原子 | B.硒元素 | C.硒单质 |
(4)农业生产强调绿色发展,下列做法中不利于保护生态环境的是______(填序号)。
| A.秸秆露天焚烧 | B.过度使用化肥、农药 | C.将大水漫灌改为喷灌和滴灌 |
您最近一年使用:0次
名校
解题方法
7 . 自来水消毒常用氯气、漂白粉【主要成分是次氯酸钙 】。请用化学用语填空:
】。请用化学用语填空:
(1)2个钙离子_______ 。
(2)标出次氯酸钙中氯元素的化合价_______ 。
(3)钙元素是人体所需的_______ (填“常量”或“微量”)元素。
(4)根据次氯酸钙的化学式,写出次氯酸的化学式_______ 。
 】。请用化学用语填空:
】。请用化学用语填空:(1)2个钙离子
(2)标出次氯酸钙中氯元素的化合价
(3)钙元素是人体所需的
(4)根据次氯酸钙的化学式,写出次氯酸的化学式
您最近一年使用:0次
名校
解题方法
8 . 实验是化学学习的重要手段。下列实验方案设计不合理的是
| 选项 | 实验目的 | 实验方案 |
| A | 比较铝和锌的金属活动性强弱 | 将铝片和锌粒分别放入硫酸铜溶液中,观察现象 |
| B | 除去氯化钙溶液中少量的盐酸 | 加过量的碳酸钙,过滤 |
| C | 鉴别碳酸钙和氧化钙 | 取少量样品,分别加入少量水,感受温度变化 |
| D | 检验氢氧化钠溶液中是否变质 | 取少量样品,加入足量盐酸,观察是否产生气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 推理和归纳是化学学习常用的思维方法。下列推理正确的是
| A.有机物中一定含碳元素,所以含碳元素的化合物一定是有机物 |
| B.置换反应都有单质生成,则有单质生成的反应一定是置换反应 |
| C.化学变化常常伴随有能量变化,所以有能量变化的一定是化学变化 |
| D.单质是由一种元素组成的纯净物,则一种元素组成的纯净物一定是单质 |
您最近一年使用:0次
10 . 已知白磷的着火点是40℃,红磷的着火点是240℃。如图实验,三支试管里面充满氮气,初始温度25℃,升温至60℃后,用注射器同时向②③试管中迅速注入足量氧气。下列说法错误的是
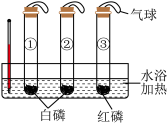
| A.只有②中有燃烧现象 |
| B.由①②现象说明可燃物达到着火点未必燃烧 |
| C.若继续水浴升温,则③中一定会燃烧 |
| D.气球有平衡气压的作用 |
您最近一年使用:0次