解题方法
1 . 某研究性小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后,得到了肯定的答案,邀请你对此展开研究。
②加热条件下,氢气还原氧化铜的化学式为
探究过程如下:
I.称量已装入相关药品的装置C、D的质量,分别为m1、m2;
Ⅱ.连接装置A、B、C,将足量的锌和稀硫酸分别装入锥形瓶和长颈漏斗中,反应一段时间后,再连接装置D,点燃酒精灯;
Ⅲ.待玻璃管内黑色固体完全变为红色时,熄灭酒精灯,直到玻璃管冷却;
IV.再次称量装置C、D的质量,分别为m3、m4。
请回答下列问题:
(1)装置B的作用是___________ 。
(2)装置A中反应的化学方程式为___________ ,稀硫酸不能用稀盐酸代替,其理由是___________ 。
(3)依据实验所得数据计算,水的组成中氢元素和氧元素的质量比为___________ 。(用m1~m4的字母表示)。
(4)误差分析。按上述实验步骤(假设生成的水完全被D装置吸收)测得水的组成中氢元素和氧元素的质量比为___________ (填“偏大”“偏小”或“准确”),理由是___________ 。如果有误差,改进措施是___________ 。

②加热条件下,氢气还原氧化铜的化学式为

探究过程如下:
I.称量已装入相关药品的装置C、D的质量,分别为m1、m2;
Ⅱ.连接装置A、B、C,将足量的锌和稀硫酸分别装入锥形瓶和长颈漏斗中,反应一段时间后,再连接装置D,点燃酒精灯;
Ⅲ.待玻璃管内黑色固体完全变为红色时,熄灭酒精灯,直到玻璃管冷却;
IV.再次称量装置C、D的质量,分别为m3、m4。
请回答下列问题:
(1)装置B的作用是
(2)装置A中反应的化学方程式为
(3)依据实验所得数据计算,水的组成中氢元素和氧元素的质量比为
(4)误差分析。按上述实验步骤(假设生成的水完全被D装置吸收)测得水的组成中氢元素和氧元素的质量比为
您最近一年使用:0次
2 . 物质在溶解时速率会受到哪些因素的影响?以硫酸铜为例进行如下探究。
【提出假设】
(1)假设一:温度因素;温度越高,硫酸铜晶体溶解速率越快。
假设二:搅拌因素;搅拌能加快硫酸铜晶体溶解速率。
假设三:颗粒大小因素;______ 。
【进行实验】
(2)设计实验验证假设二。
【反思评价】
(3)在上述因素中,能改变物质溶解度的因素是______ 。
(4)用分子观点解释温度的影响______ 。
(5)在本实验中搅拌能加快晶体溶解速率的原因______ 。
(6)要使试管里的固体加速溶解,常采用的方法是______ 。
【提出假设】
(1)假设一:温度因素;温度越高,硫酸铜晶体溶解速率越快。
假设二:搅拌因素;搅拌能加快硫酸铜晶体溶解速率。
假设三:颗粒大小因素;
【进行实验】
(2)设计实验验证假设二。
| 实验操作 | 实验现象 | 实验结论 |
| 在2个大小相同的烧杯中,分别注入温度相同的100mL水,再同时向烧杯中各加入一药匙颗粒大小相同的硫酸铜晶体,用玻璃棒搅拌其中一个烧杯 | 在搅拌的情况下,硫酸铜晶体溶解得 | 假设二正确 |
【反思评价】
(3)在上述因素中,能改变物质溶解度的因素是
(4)用分子观点解释温度的影响
(5)在本实验中搅拌能加快晶体溶解速率的原因
(6)要使试管里的固体加速溶解,常采用的方法是
您最近一年使用:0次
3 . 学习化学的一个重要途径是科学探究,请完成以下探究活动。
【探究活动一】
某学校初中甲、乙两个化学兴趣小组的同学在老师的指导下,完成下列实验活动。请你一起参与探究并回答问题。
两组同学按相同的方案首先向氯化钡溶液、氢氧化钡溶液中分别滴加硫酸钠溶液和碳酸钠溶液。______ 。
(2)同学们认为试管①、②和试管③、④中发生反应的微观实质是分别相同的,请你写出试管③、④中发生反应而减少的微观粒子符号;______ 。
实验后同学们将4支试管中的所有物质倒入一个烧杯中,充分混合后过滤得滤渣和滤液(废液)。同学们对废液产生兴趣,打算对其溶质成分进行探究,然后再进行处理。
(3)甲组同学取少量废液于试管中,加入足量稀硫酸,看到溶液中产生气泡,则废液中一定含有的溶质是______ (填化学式)。现要求将甲组废液处理呈中性再排放,请你写出一个可行的实验方案______ 。
(4)乙组同学也取少量废液于试管中,加足量稀硫酸,看到有白色沉淀产生,则乙组废液中一定没有的离子是______ (填符号),写出废液中与足量稀硫酸反应产生白色沉淀的物质化学式______ 。
【探究活动二】
 是一种重要的化工原料,某工厂以一种镁矿石(主要成分为
是一种重要的化工原料,某工厂以一种镁矿石(主要成分为 和
和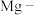
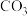 ,还含有少量
,还含有少量 ,其它成分忽略)为原料制备
,其它成分忽略)为原料制备 的主要流程如图:
的主要流程如图:
① 既不溶于水也不溶于稀硫酸;
既不溶于水也不溶于稀硫酸;
②部分阳离子以氢氧化物形式沉淀时溶液的 见下表。
见下表。
请回答下列问题:
(5) 溶于稀硫酸的化学方程式为
溶于稀硫酸的化学方程式为______ 。
(6)为了让镁矿石与稀硫酸充分反应,提高原料利用率,可采取的措施为______(填字母)。
(7)选用 调节
调节 使
使 转化为沉淀,而不选用
转化为沉淀,而不选用 的原因是
的原因是______ 。
(8)加氧化镁调节后溶液的 范围是
范围是______ (用不等式表示)。
【探究活动一】
某学校初中甲、乙两个化学兴趣小组的同学在老师的指导下,完成下列实验活动。请你一起参与探究并回答问题。
两组同学按相同的方案首先向氯化钡溶液、氢氧化钡溶液中分别滴加硫酸钠溶液和碳酸钠溶液。

(2)同学们认为试管①、②和试管③、④中发生反应的微观实质是分别相同的,请你写出试管③、④中发生反应而减少的微观粒子符号;
实验后同学们将4支试管中的所有物质倒入一个烧杯中,充分混合后过滤得滤渣和滤液(废液)。同学们对废液产生兴趣,打算对其溶质成分进行探究,然后再进行处理。
(3)甲组同学取少量废液于试管中,加入足量稀硫酸,看到溶液中产生气泡,则废液中一定含有的溶质是
(4)乙组同学也取少量废液于试管中,加足量稀硫酸,看到有白色沉淀产生,则乙组废液中一定没有的离子是
【探究活动二】
 是一种重要的化工原料,某工厂以一种镁矿石(主要成分为
是一种重要的化工原料,某工厂以一种镁矿石(主要成分为 和
和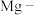
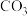 ,还含有少量
,还含有少量 ,其它成分忽略)为原料制备
,其它成分忽略)为原料制备 的主要流程如图:
的主要流程如图:
①
 既不溶于水也不溶于稀硫酸;
既不溶于水也不溶于稀硫酸;②部分阳离子以氢氧化物形式沉淀时溶液的
 见下表。
见下表。| 阳离子 |  |  |  |
开始沉淀时的 | 9.1 | 7.6 | 1.9 |
沉淀完全时的 | 11.1 | 9.7 | 3.2 |
(5)
 溶于稀硫酸的化学方程式为
溶于稀硫酸的化学方程式为(6)为了让镁矿石与稀硫酸充分反应,提高原料利用率,可采取的措施为______(填字母)。
| A.将镁矿石粉碎 | B.降低反应温度 | C.用稀硫酸多次浸泡 |
(7)选用
 调节
调节 使
使 转化为沉淀,而不选用
转化为沉淀,而不选用 的原因是
的原因是(8)加氧化镁调节后溶液的
 范围是
范围是
您最近一年使用:0次
4 . 某学校初中甲、乙两个化学兴趣小组的同学在老师的指导下,完成下列实验活动。请你一起参与探究并回答问题。
【探究活动一】
两组同学按相同的方案首先向氯化钡溶液、氢氧化钡溶液中分别滴加硫酸钠溶液和碳酸钠溶液。________ 。
(2)试管①中发生反应的化学方程式为:________ 。
(3)同学们认为试管①、②和试管③、④中发生反应的微观实质是分别相同的,请你写出试管③、④中发生反应而减少的微观粒子符号:________ 。
【探究活动二】
实验后同学们将四支试管中的所有物质倒入一个烧杯中,充分混合后过滤得滤渣和滤液(废液)。同学们对废液产生兴趣,打算对其溶质成分进行探究,然后再进行处理。
(4)甲组同学取少量废液于试管中,加入足量稀硫酸,看到溶液中产生气泡,则废液中一定含有的溶质是________ (填化学式)。现要求将甲组废液处理呈中性再排放,请你写出一个可行的实验方案________ 。
(5)乙组同学也取少量废液于试管中,加足量稀硫酸,看到有白色沉淀产生,则乙组废液中一定没有的离子是________ (填符号)。
【探究活动一】
两组同学按相同的方案首先向氯化钡溶液、氢氧化钡溶液中分别滴加硫酸钠溶液和碳酸钠溶液。

(2)试管①中发生反应的化学方程式为:
(3)同学们认为试管①、②和试管③、④中发生反应的微观实质是分别相同的,请你写出试管③、④中发生反应而减少的微观粒子符号:
【探究活动二】
实验后同学们将四支试管中的所有物质倒入一个烧杯中,充分混合后过滤得滤渣和滤液(废液)。同学们对废液产生兴趣,打算对其溶质成分进行探究,然后再进行处理。
(4)甲组同学取少量废液于试管中,加入足量稀硫酸,看到溶液中产生气泡,则废液中一定含有的溶质是
(5)乙组同学也取少量废液于试管中,加足量稀硫酸,看到有白色沉淀产生,则乙组废液中一定没有的离子是
您最近一年使用:0次
解题方法
5 . 小明同学想在实验室用NaOH溶液与CO2气体制取Na2CO3溶液。但是经过检验,发现很难得到纯净的Na2CO3溶液,在老师的帮助下查阅了相关资料,制定了计划。
【查阅资料】
①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象。
②NaHCO3溶液煮沸时不会发生分解反应;NaHCO3溶液与CaCl2溶液不反应。
③ 。
。
【制取步骤】
①量取两份50mL相同浓度的NaOH溶液备用。
②用一份50mLNaOH溶液吸收过量的CO2气体,至CO2气体不再溶解。
③小心煮沸②溶液1~2分钟。
④在得到的③溶液中加入另一份50mLNaOH溶液,使其充分混合。
【实验探究】
(1)步骤③的作用是________ ,步骤③和步骤④能否颠倒?_______ ,理由是______ 。
(2)若实验中溶液的体积控制的不准确,则制得的Na2CO3溶液中可能含有的杂质是_______ 。
(3)为检验制得的溶液是否为纯净的Na2CO3溶液,请你与小明一起完成下列实验探究:
【结论】所制得的不是纯净的Na2CO3溶液。
【评价与反思】
(4)小芳同学认为可以用过量的Ca(OH)2溶液替代CaCl2溶液进行以上实验,你认为是否可行?___________ ,原因是___________ 。
【查阅资料】
①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象。
②NaHCO3溶液煮沸时不会发生分解反应;NaHCO3溶液与CaCl2溶液不反应。
③
 。
。【制取步骤】
①量取两份50mL相同浓度的NaOH溶液备用。
②用一份50mLNaOH溶液吸收过量的CO2气体,至CO2气体不再溶解。
③小心煮沸②溶液1~2分钟。
④在得到的③溶液中加入另一份50mLNaOH溶液,使其充分混合。
【实验探究】
(1)步骤③的作用是
(2)若实验中溶液的体积控制的不准确,则制得的Na2CO3溶液中可能含有的杂质是
(3)为检验制得的溶液是否为纯净的Na2CO3溶液,请你与小明一起完成下列实验探究:
| 实验步骤 | 实验现象 | 实验结论 | |
| 取少量制得的溶液于试管中,加入过量的显中性的CaCl2溶液 | 溶液中含有Na2CO3 | ||
| 将上步实验所得混合物进行过滤,将滤液分成两份 | 取其中一份加入足量的 | 无气泡产生 | 制得的溶液中不含 |
| 取另一份加入 | 制得的溶液中含有NaOH | ||
【结论】所制得的不是纯净的Na2CO3溶液。
【评价与反思】
(4)小芳同学认为可以用过量的Ca(OH)2溶液替代CaCl2溶液进行以上实验,你认为是否可行?
您最近一年使用:0次
7日内更新
|
33次组卷
|
3卷引用:2024年黑龙江省绥化市九年级中考三模物理·化学试题-初中化学
解题方法
6 . 小明同学在学习完酸、碱、盐的化学性质之后,进行了如图所示的实验,请你来参与他的探究过程,并回答下列问题。___________ 。做乙图所示实验时,看到的现象是___________ 。
(2)实验后,小明将甲、乙、丙中的无色溶液均倒入洁净的废液缸,发现废液明显变浑浊且呈红色。废液变浑浊,是因为倾倒前丙中的溶液含有NaOH和___________ (填化学式)。
(3)【提出问题】使废液变成红色的物质是什么?
【作出猜想】
猜想一:只有Na2CO3
猜想二:只有NaOH
猜想三:NaOH和Ca(OH)2
猜想四:NaOH和___________
以上猜想中,你认为不合理的是猜想___________ 。
【查阅资料】CaCl2溶液呈中性。
【验证猜想】
(4)静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,有白色沉淀生成。静置后发现试管中的上层清液仍为红色,由此证明了猜想___________ 成立。

(2)实验后,小明将甲、乙、丙中的无色溶液均倒入洁净的废液缸,发现废液明显变浑浊且呈红色。废液变浑浊,是因为倾倒前丙中的溶液含有NaOH和
(3)【提出问题】使废液变成红色的物质是什么?
【作出猜想】
猜想一:只有Na2CO3
猜想二:只有NaOH
猜想三:NaOH和Ca(OH)2
猜想四:NaOH和
以上猜想中,你认为不合理的是猜想
【查阅资料】CaCl2溶液呈中性。
【验证猜想】
(4)静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,有白色沉淀生成。静置后发现试管中的上层清液仍为红色,由此证明了猜想
您最近一年使用:0次
名校
解题方法
7 . 同学们对“二氧化碳溶于水是否与水反应”进行实验探究,请参与探究并回答下列问题。
【探究思路】
(1)判断物质间是否发生化学反应的根本依据是_______ ,观察到的可以作为判断依据的实验现象有颜色变化、放出气体、生成沉淀等并伴有吸热、放热、发光等能量变化。
(2)CO2溶于水无明显现象,_______ (填“能”或“不能”)用观察的方法判断是否发生反应。
(3)设计“探究物质间是否反应”的实验方案的依据是:生成物和反应物的性质差异。
【提出猜想】猜想一:二氧化碳溶于水不与水反应;猜想二:二氧化碳溶于水且与水反应。
【实验设计】用四朵石蕊溶液染成紫色的干燥纸花设计如下实验:(已知稀醋酸可使紫色石蕊变红)
i.“实验设计②”的具体内容是_______ 。
ii.“实验设计③”的目的是_______ 。
【进行实验】进行实验探究,观察记录实验现象。
【实验结论】猜想二成立,支持猜想二成立的实验现象是_______ 。
【反思交流】实验探究“无明显实验现象时是否发生化学反应”的核心思路有_______ (填字母)。
A.设计对比实验 B.控制实验条件 C.获取事实证据 D.逻辑推理判断
【探究思路】
(1)判断物质间是否发生化学反应的根本依据是
(2)CO2溶于水无明显现象,
(3)设计“探究物质间是否反应”的实验方案的依据是:生成物和反应物的性质差异。
【提出猜想】猜想一:二氧化碳溶于水不与水反应;猜想二:二氧化碳溶于水且与水反应。
【实验设计】用四朵石蕊溶液染成紫色的干燥纸花设计如下实验:(已知稀醋酸可使紫色石蕊变红)
| 序号 | 实验设计 |
| ① | 向第一朵纸花喷稀醋酸 |
| ② | ________。 |
| ③ | 将第三朵纸花直接放入盛有二氧化碳的集气瓶中 |
| ④ | 将第四朵纸花喷水后放入盛有二氧化碳的集气瓶中 |
ii.“实验设计③”的目的是
【进行实验】进行实验探究,观察记录实验现象。
【实验结论】猜想二成立,支持猜想二成立的实验现象是
【反思交流】实验探究“无明显实验现象时是否发生化学反应”的核心思路有
A.设计对比实验 B.控制实验条件 C.获取事实证据 D.逻辑推理判断
您最近一年使用:0次
7日内更新
|
18次组卷
|
2卷引用:黑龙江省哈尔滨市第四十七中学2023-2024学年下学期5月份调查问卷九年级理化综合试题-初中化学
8 . 为探究酸的化学性质,某化学兴趣小组的同学利用盐酸进行了如下实验,请回答下列问题:_______ 。
(2)A试管中的实验现象为银白色固体表面产生气泡,固体减少,放热,_______ 。
(3)将C、D试管反应后的溶液倒入同一烧杯中,实验现象如图所示,由该实验现象可知,C试管反应后溶液中的溶质为_______ (写名称),同学们将烧杯中的物质过滤,对所得滤液中离子成分进行探究:
【猜想与假设】悦彤同学的猜想: 、
、 ;一诺同学的猜想:
;一诺同学的猜想: 、
、 、
、 ;婷婷同学的猜想:
;婷婷同学的猜想: 、
、 、
、 、
、 ;浚琪同学的猜想:
;浚琪同学的猜想:_______ 。
【进行讨论】经过讨论,同学们一致认为_______ 同学的猜想不正确。
【设计实验】
悦彤同学为了证明自己的猜想,设计了如下实验,请完成实验报告:
【评价与交流】芃芃同学经过思考认为悦彤的实验设计不正确,她觉得只用一种试剂就能鉴别出溶液中的离子成分,她选取的试剂是下列中的_______ (填序号),最终得出一诺的猜想成立。
A.硫酸钠溶液 B.稀硫酸 C.氯化钙溶液
【归纳与总结】同学们经过上述实验,总结出酸的一些化学性质,酸能与活泼金属、_______ 反应。(填物质类别)
【拓展与提升】为了达到无公害排放,小崔实验小组的同学向C、D反应后的100g滤液中,加入50g 14.2%的 溶液,恰好完全反应,过滤,蒸发结晶得到23.4g NaCl,(假设各步操作都很严谨)。则100g滤液中
溶液,恰好完全反应,过滤,蒸发结晶得到23.4g NaCl,(假设各步操作都很严谨)。则100g滤液中 的质量分数为
的质量分数为_______ 。

(2)A试管中的实验现象为银白色固体表面产生气泡,固体减少,放热,
(3)将C、D试管反应后的溶液倒入同一烧杯中,实验现象如图所示,由该实验现象可知,C试管反应后溶液中的溶质为

【猜想与假设】悦彤同学的猜想:
 、
、 ;一诺同学的猜想:
;一诺同学的猜想: 、
、 、
、 ;婷婷同学的猜想:
;婷婷同学的猜想: 、
、 、
、 、
、 ;浚琪同学的猜想:
;浚琪同学的猜想:【进行讨论】经过讨论,同学们一致认为
【设计实验】
悦彤同学为了证明自己的猜想,设计了如下实验,请完成实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| 溶液中产生白色沉淀 | 自己的猜想成立 |
A.硫酸钠溶液 B.稀硫酸 C.氯化钙溶液
【归纳与总结】同学们经过上述实验,总结出酸的一些化学性质,酸能与活泼金属、
【拓展与提升】为了达到无公害排放,小崔实验小组的同学向C、D反应后的100g滤液中,加入50g 14.2%的
 溶液,恰好完全反应,过滤,蒸发结晶得到23.4g NaCl,(假设各步操作都很严谨)。则100g滤液中
溶液,恰好完全反应,过滤,蒸发结晶得到23.4g NaCl,(假设各步操作都很严谨)。则100g滤液中 的质量分数为
的质量分数为
您最近一年使用:0次
解题方法
9 . 化学小组为验证某些酸碱盐之间能否发生反应:做了如下实验:
【查阅资料】
①碳酸钠溶液显碱性,硝酸钡、硝酸钠、硫酸钠溶液均为中性。
②碱性溶液中含有大量 。
。
③碳酸钡、硫酸钡均是不溶于水的白色沉淀,且硫酸钡不溶于酸。
【探究一】如图所示,分别向三支盛有稀硫酸的试管中滴加不同溶液,边滴加边震荡。
(1)试管①中没有观察到明显现象,试管②中有气泡产生,试管③中出现白色沉淀,写出试管③中反应的化学方程式________ 。
【实验结论】试管①中未反应,试管②和试管③中一定发生了复分解反应。
【反思与交流】
同学们不同意试管①中未反应的结论,于是向其中滴入几滴酚酞试剂,观察到溶液为红色。证明这两个试管中发生了复分解反应。
(2)小明同学根据“试管①中溶液呈红色”,认为硫酸与氢氧化钠发生了化学反应,小明的理由是:________ 。
【废液处理】
实验后,小亮同学将上述三支试管的“废液”全部倒入一洁净的大烧杯中,充分混合后静置,发现烧杯底部有白色沉淀,上层清液呈红色。
【讨论与交流】
(3)静置后的上层清液中一定含有的的离子有(填离子符号)________ 。
【探究二】
(4)小宾同学为进一步确定上层清液中可能含有的溶质成分,进行了如下实验:
【得出结论】
(5)根据实验现象,上层清液中的溶质含有 、
、 、
、________ (除酚酞外)。
(6)若酸碱盐之间发生反应,则一定有________ 生成。
(7)判断上层清液中含有 、
、 的理由是:
的理由是:________ 。
【查阅资料】
①碳酸钠溶液显碱性,硝酸钡、硝酸钠、硫酸钠溶液均为中性。
②碱性溶液中含有大量
 。
。③碳酸钡、硫酸钡均是不溶于水的白色沉淀,且硫酸钡不溶于酸。
【探究一】如图所示,分别向三支盛有稀硫酸的试管中滴加不同溶液,边滴加边震荡。
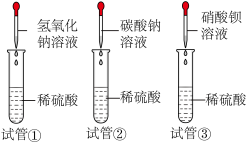
(1)试管①中没有观察到明显现象,试管②中有气泡产生,试管③中出现白色沉淀,写出试管③中反应的化学方程式
【实验结论】试管①中未反应,试管②和试管③中一定发生了复分解反应。
【反思与交流】
同学们不同意试管①中未反应的结论,于是向其中滴入几滴酚酞试剂,观察到溶液为红色。证明这两个试管中发生了复分解反应。
(2)小明同学根据“试管①中溶液呈红色”,认为硫酸与氢氧化钠发生了化学反应,小明的理由是:
【废液处理】
实验后,小亮同学将上述三支试管的“废液”全部倒入一洁净的大烧杯中,充分混合后静置,发现烧杯底部有白色沉淀,上层清液呈红色。
【讨论与交流】
(3)静置后的上层清液中一定含有的的离子有(填离子符号)
【探究二】
(4)小宾同学为进一步确定上层清液中可能含有的溶质成分,进行了如下实验:
| 实验操作 | 实验现象 |
| 取少量上层清液:加入稍过量的硝酸钡溶液,振荡 | 产生白色沉淀,溶液为红色 |
| 再向试管中加入过量的 | 白色沉淀部分溶解,有气泡产生,溶液为无色 |
【得出结论】
(5)根据实验现象,上层清液中的溶质含有
 、
、 、
、(6)若酸碱盐之间发生反应,则一定有
(7)判断上层清液中含有
 、
、 的理由是:
的理由是:
您最近一年使用:0次
解题方法
10 . 化学课外小组进行以下两个实验活动。
探究一
配制500g溶质质量分数为0.9%生理盐水,操作步骤如图。
(2)如图⑤称量过程中,若指针左偏,你应该采取的操是________ 。
(3)用量筒量取水时,若仰视读数,则配制该溶液溶质质量分数将________ (填“偏大”、“偏小”或“不变”)。
探究二
某蛋糕包装中常使用一种防腐剂,其标签如图所示,同学们对这包久置的“防腐剂”固体样品很好奇,设计实验进行探究。
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、 、CaO、
、CaO、 和
和 。
。
【实验探究1】
(4)甲同学的方案:
【反思与评价】
(5)甲同学实验中步骤(1)的结论不合理,正确结论应是________ 。
(6)甲同学实验中步骤(2)的结论不合理,理由是________ 。
(7)甲同学实验中步骤(3)中反应的化学方程式是________ 。
【实验探究2】
乙、丙同学设计如下实验方案继续验证:________ ,仍有一种物质不能确定,该物质是________ 。
丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中 质量为1.0g,滤渣C质量为1.0g。
质量为1.0g,滤渣C质量为1.0g。
【实验结论】
(9)综合上述实验及所给数据,久置固体的成分是________ 。
探究一
配制500g溶质质量分数为0.9%生理盐水,操作步骤如图。

| A.④⑤①②③ | B.①②③④⑤ | C.①②④③⑤ | D.③④①②⑤ |
(2)如图⑤称量过程中,若指针左偏,你应该采取的操是
(3)用量筒量取水时,若仰视读数,则配制该溶液溶质质量分数将
探究二
某蛋糕包装中常使用一种防腐剂,其标签如图所示,同学们对这包久置的“防腐剂”固体样品很好奇,设计实验进行探究。
| 品名:防腐剂 成分:铁粉:生石灰等 |
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、
 、CaO、
、CaO、 和
和 。
。【实验探究1】
(4)甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁 | 固体中一定含有氧化钙和氢氧化钙 |
| (2)另取少量固体于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有 |
| (3)将步骤(2)中产生的气体通入澄清的石灰水中 | 固体中一定含有 |
【反思与评价】
(5)甲同学实验中步骤(1)的结论不合理,正确结论应是
(6)甲同学实验中步骤(2)的结论不合理,理由是
(7)甲同学实验中步骤(3)中反应的化学方程式是
【实验探究2】
乙、丙同学设计如下实验方案继续验证:

丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中
 质量为1.0g,滤渣C质量为1.0g。
质量为1.0g,滤渣C质量为1.0g。【实验结论】
(9)综合上述实验及所给数据,久置固体的成分是
您最近一年使用:0次



