2024·云南·模拟预测
解题方法
1 . 醋酸钙[Ca(Ac)2]是国家允许使用的补钙制剂之一、以蛋壳为原料回收膜并制备醋酸钙的一种工艺流程如图。___________ 。
(2)CO2与CH4一定条件下化合可生成甲醛(HCHO),则此反应中CO2与CH4的最佳质量比是______ 。
(3)在反应Ⅰ中制备石灰乳,而不是制备澄清石灰水的目的是___________ 。写出熟石灰的一种用途___________ 。
(4)在反应Ⅱ中醋酸过量的目的是___________ 。
(5)膜分离时,盐酸不能过量的主要原因是___________ 。

(2)CO2与CH4一定条件下化合可生成甲醛(HCHO),则此反应中CO2与CH4的最佳质量比是
(3)在反应Ⅰ中制备石灰乳,而不是制备澄清石灰水的目的是
(4)在反应Ⅱ中醋酸过量的目的是
(5)膜分离时,盐酸不能过量的主要原因是
您最近一年使用:0次
2 . 回答下列问题:
(1)请用化学用语回答问题:
①氦气______ ;②3个镁离子______ ;③相对分子质量最小的氧化物______ 。
(2)硫酸生产过程中会产生大量有害的二氧化硫废气和烟尘,为了变废为宝,某硫酸厂的环保车间设计了如图所示的工艺流程,采用物质循环利用的方法将二氧化硫转化为无毒的气体。请分析流程,解决下列问题:
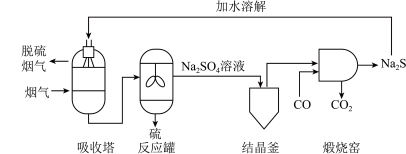
①反应罐中分离物质采用的操作方法为_______ 。
②写出煅烧窑中高温条件下发生反应的化学方程式_______ 。
③整个流程中,可以循环使用的物质是______ (填化学式)。
(1)请用化学用语回答问题:
①氦气
(2)硫酸生产过程中会产生大量有害的二氧化硫废气和烟尘,为了变废为宝,某硫酸厂的环保车间设计了如图所示的工艺流程,采用物质循环利用的方法将二氧化硫转化为无毒的气体。请分析流程,解决下列问题:

①反应罐中分离物质采用的操作方法为
②写出煅烧窑中高温条件下发生反应的化学方程式
③整个流程中,可以循环使用的物质是
您最近一年使用:0次
真题
解题方法
3 . 新能源的开发和利用促进了能源结构向多元、清洁和低碳转变。
(1)目前,人类利用的能量大多来自化石燃料,如石油、天然气和______ 。在有石油的地方,一般都有天然气存在,天然气的主要成分是甲烷,其化学式为______ 。
(2)做饭时,天然气燃烧不充分,锅底易出现黑色物质,此时可调______ (填“小”或“大”)燃气灶的进风口,使燃料充分燃烧,节约能源。
(3)我国研制出一种新型催化剂,在这种催化剂作用下,二氧化碳可以转化为汽油,主要转化过程如图所示(部分生成物已略去)。______ 不变。
②过程I中反应生成的另外一种物质为生活中常见的氧化物,该反应的化学方程式为______ 。
(4)随着科学技术的发展,氢能源的开发利用已取得很大进展。氢气作为燃料的优点是______ (答一点即可)。
(1)目前,人类利用的能量大多来自化石燃料,如石油、天然气和
(2)做饭时,天然气燃烧不充分,锅底易出现黑色物质,此时可调
(3)我国研制出一种新型催化剂,在这种催化剂作用下,二氧化碳可以转化为汽油,主要转化过程如图所示(部分生成物已略去)。
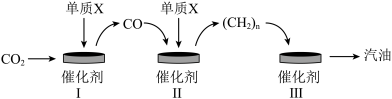
②过程I中反应生成的另外一种物质为生活中常见的氧化物,该反应的化学方程式为
(4)随着科学技术的发展,氢能源的开发利用已取得很大进展。氢气作为燃料的优点是
您最近一年使用:0次
解题方法
4 . 燃煤电厂常利用NaOH溶液处理烟气,实现“碳捕集”,其主要转化流程如图:________ 。
(2)写出烟气通入氢氧化钠溶液中所发生反应的化学方程式:________________ 。
(3)写出干冰的一种用途________________ 。
(4)上述流程中可循环使用的物质有溶液X和________ 。
(5)用化学用语填空:
①硫元素________ ;
②3个氧原子________ 。
(6)写出下列符号中数字的含义:
“Mg2+”中“2+”表示________ 。

(2)写出烟气通入氢氧化钠溶液中所发生反应的化学方程式:
(3)写出干冰的一种用途
(4)上述流程中可循环使用的物质有溶液X和
(5)用化学用语填空:
①硫元素
②3个氧原子
(6)写出下列符号中数字的含义:
“Mg2+”中“2+”表示
您最近一年使用:0次
2024·云南·模拟预测
解题方法
5 . 能源问题一直受到社会高度关注。
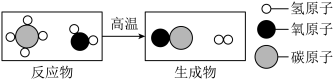
(1)天然气重整可以得到合成气,其反应的微观示意图如下:___________ 。
(2)氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为:
6ZnFe2O4 6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O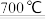 3ZnFe2O4+H2↑
3ZnFe2O4+H2↑
①制氢过程中,ZnFe2O4的作用是___________ 。
②该循环制氢中不断消耗的物质是___________ (填化学式) 。
Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得,该合金在一定条件下完全吸氢生成氢化物MgH2和另一种合金。
③熔炼制备Mg2Cu合金时,通入氩气的目的是___________ 。
④氢化物MgH2与水反应生成一种碱,并释放出H2。其化学反应方程式为___________ 。
(1)天然气重整可以得到合成气,其反应的微观示意图如下:
(2)氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为:
6ZnFe2O4
 6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O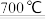 3ZnFe2O4+H2↑
3ZnFe2O4+H2↑①制氢过程中,ZnFe2O4的作用是
②该循环制氢中不断消耗的物质是
Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得,该合金在一定条件下完全吸氢生成氢化物MgH2和另一种合金。
③熔炼制备Mg2Cu合金时,通入氩气的目的是
④氢化物MgH2与水反应生成一种碱,并释放出H2。其化学反应方程式为
您最近一年使用:0次
2024·云南·模拟预测
解题方法
6 . 利用空气制取氮肥的流程如图所示:________ 。(填“物理变化”或“化学变化”)。
(2)反应Ⅱ的化学方程式为____________ ,基本反应类型是_________ 。(填“化合反应”或“分解反应”)。
(3)Ⅲ中催化剂的作用是_________ 。
(4)写出反应Ⅳ的化学方程式__________ 。

(2)反应Ⅱ的化学方程式为
(3)Ⅲ中催化剂的作用是
(4)写出反应Ⅳ的化学方程式
您最近一年使用:0次
2024·云南·模拟预测
解题方法
7 . 金属材料广泛应用于生产、生活中。
(1)下列用品中,主要利用金属导热性的是__________ (填字母)。
A 金饰品 B 铁锅 C 铜导线
(2)铁制容器不能用来盛放农药波尔多液(波尔多液的主要成分是硫酸铜和氢氧化钙),用化学方程式表示其原因____________ 。
(3)向含有氯化铜、氯化亚铁和稀盐酸的混合溶液中加入过量镁粉,充分反应后过滤滤液中含有的溶质是____________ (写化学式)。
(4)铁矿石有多种,如赤铁矿(主要成分Fe2O3)和磁铁矿(主要成分Fe3O4)等。写出赤铁矿石中的主要成分与一氧化碳反应的化学方程式___________ 。
(5)某钢铁厂每天需消耗3500t含Fe2O380%的赤铁矿石,理论上可日产含Fe 98%的生铁_________ t。
(1)下列用品中,主要利用金属导热性的是
A 金饰品 B 铁锅 C 铜导线
(2)铁制容器不能用来盛放农药波尔多液(波尔多液的主要成分是硫酸铜和氢氧化钙),用化学方程式表示其原因
(3)向含有氯化铜、氯化亚铁和稀盐酸的混合溶液中加入过量镁粉,充分反应后过滤滤液中含有的溶质是
(4)铁矿石有多种,如赤铁矿(主要成分Fe2O3)和磁铁矿(主要成分Fe3O4)等。写出赤铁矿石中的主要成分与一氧化碳反应的化学方程式
(5)某钢铁厂每天需消耗3500t含Fe2O380%的赤铁矿石,理论上可日产含Fe 98%的生铁
您最近一年使用:0次
2024·云南·模拟预测
解题方法
8 . 用适当的化学符号填空
(1)镁元素____________ ;
(2)三个氢原子____________ ;
(3)四个二氧化硫分子___________ ;
(4)氢氧根离子____________ ;
(5)氧化铁中铁元素的化合价为正三价_____________ 。
(6)符号“3Ca2+”中的“3”表示________ ,“2+”表示________ 。
(1)镁元素
(2)三个氢原子
(3)四个二氧化硫分子
(4)氢氧根离子
(5)氧化铁中铁元素的化合价为正三价
(6)符号“3Ca2+”中的“3”表示
您最近一年使用:0次
2024·云南·模拟预测
9 . 水的生活、生产和化学实验中起着十分重要的作用。自来水厂净化水的过程为取水→沉降→过滤→吸附→消毒。在净水过程中常用高铁酸钾(K2FeO4)作絮凝剂。
(1)制备K2FeO4的化学方程式为2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,则X的化学式为___________ 。
(2)自来水厂的净水过程中,过滤是为了除去水中的___________ 杂质。
(3)欲证明一瓶无色透明液体是纯水,可靠的实验方法是___________(选填字母)。
(4)请根据如图实验操作,并结合溶解度曲线回答下列问题(其中甲、乙、丙均不含结晶水)___________ ;试管内所盛饱和溶液的溶质为对应溶解度曲线中的___________ (选填“甲”“乙”或“丙”)。
②如果要配制相同浓度的甲、乙饱和溶液,需要把温度控制在___________ ℃。
③t3℃时,将等质量的甲、乙、丙的饱和溶液(没有剩余固体)都降温到t1℃,溶液中溶质的质量分数由小到大的顺序为___________ 。
(1)制备K2FeO4的化学方程式为2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,则X的化学式为
(2)自来水厂的净水过程中,过滤是为了除去水中的
(3)欲证明一瓶无色透明液体是纯水,可靠的实验方法是___________(选填字母)。
| A.1.01×105Pa时沸点为100℃ | B.测得其pH=7 | C.电解时得到H2与O2的体积比为2:1 |
(4)请根据如图实验操作,并结合溶解度曲线回答下列问题(其中甲、乙、丙均不含结晶水)

②如果要配制相同浓度的甲、乙饱和溶液,需要把温度控制在
③t3℃时,将等质量的甲、乙、丙的饱和溶液(没有剩余固体)都降温到t1℃,溶液中溶质的质量分数由小到大的顺序为
您最近一年使用:0次
10 . 化学与生产生活密切相关。
(1)请从下列物质中选择相应的序号填在横线上:
a.氩气 b.硝酸铵 c.氧化钙 d.碳酸氢钠
①常用作食品干燥剂的是___________ 。
②可用于填充霓虹灯的是___________ 。
③溶于水吸热的物质是___________ 。
④烘焙糕点所用发酵粉主要成分___________ 。
(2)洗涤剂去油污是因为洗涤剂具有___________ 作用。
(3)豆浆已成为众多家庭的饮品,下表是豆浆中部分营养成分的平均质量分数。请据表回答:
①豆浆中含有人体所需的微量元素是___________ ,青少年因缺___________ 而导致佝偻病。
②豆浆所含的营养素中不能供给人体能量,但可以起到调节新陈代谢作用的是___________ (填字母)。
a.蛋白质 b.油脂 c.糖类 d.维生素
(1)请从下列物质中选择相应的序号填在横线上:
a.氩气 b.硝酸铵 c.氧化钙 d.碳酸氢钠
①常用作食品干燥剂的是
②可用于填充霓虹灯的是
③溶于水吸热的物质是
④烘焙糕点所用发酵粉主要成分
(2)洗涤剂去油污是因为洗涤剂具有
(3)豆浆已成为众多家庭的饮品,下表是豆浆中部分营养成分的平均质量分数。请据表回答:
| 成分 | 蛋白质 | 油脂 | 糖类 | 钙 | 铁 | 维生素 |
| 质量分数/% | 1.8 | 0.7 | 1.1 | 0.01 | 0.0005 | 0.015 |
②豆浆所含的营养素中不能供给人体能量,但可以起到调节新陈代谢作用的是
a.蛋白质 b.油脂 c.糖类 d.维生素
您最近一年使用:0次



