名校
解题方法
1 . 化学实验室有一瓶失去标签的过氧化氢溶液,为测定这瓶过氧化氢溶液的溶质质量分数,化学小组的同学完成了如下实验。
(1)生成氧气的质量为___________ g。
(2)这瓶过氧化氢溶液的溶质质量分数为多少?
【温馨提示: 】
】

(1)生成氧气的质量为
(2)这瓶过氧化氢溶液的溶质质量分数为多少?
【温馨提示:
 】
】
您最近一年使用:0次
2024·云南·模拟预测
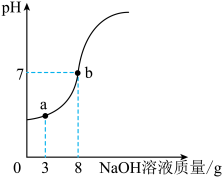
2 . 兴趣小组同学要测定一瓶失去标签的稀硫酸的溶质质量分数。取10g稀硫酸样品,将10%的氢氧化钠溶液逐滴加入到样品中,不断搅拌,测得溶液pH随滴入氢氧化钠溶液量的变化情况如图所示。
(1)该反应的实质是___________ 。
(2)计算该稀硫酸的溶质质量分数。
(1)该反应的实质是
(2)计算该稀硫酸的溶质质量分数。
您最近一年使用:0次
2024·云南·模拟预测
解题方法
3 . 二氧化硫(SO2)是一种食品添加剂。葡萄酒酿造过程中添加SO2可防止其变质,但须严格控制用量,我国《葡萄酒国家标准》中规定SO2的含量≤ 259 mg/L。
(1)SO2作为食品添加剂须严格控制用量的原因是___________ 。
(2)为检测某国产葡萄酒SO2中的含量是否符合国家标准,进行如下实验:
步骤1 取100mL该葡萄酒于锥形瓶中,加入质量分数为10%的H2O2溶液,将SO2完全转化成硫酸。
步骤2 向锥形瓶中滴加指示剂(该指示剂在pH<7的溶液中显紫色,在pH>7的溶液中显绿色),用氢氧化钠溶液中和,测得锥形瓶中硫酸的质量为14.7mg。
通过计算判断该葡萄酒中SO2的含量是否符合国家标准。
(1)SO2作为食品添加剂须严格控制用量的原因是
(2)为检测某国产葡萄酒SO2中的含量是否符合国家标准,进行如下实验:
步骤1 取100mL该葡萄酒于锥形瓶中,加入质量分数为10%的H2O2溶液,将SO2完全转化成硫酸。
步骤2 向锥形瓶中滴加指示剂(该指示剂在pH<7的溶液中显紫色,在pH>7的溶液中显绿色),用氢氧化钠溶液中和,测得锥形瓶中硫酸的质量为14.7mg。
通过计算判断该葡萄酒中SO2的含量是否符合国家标准。
您最近一年使用:0次
解题方法
4 . 向某硫酸钠溶液中加入一定量的氯化钡溶液,两者恰好完全反应。实验数据如下表:
请计算:
(1)产生BaSO4的质量为___ g。
(2)所用硫酸钠溶液中溶质的质量分数。(温馨提示: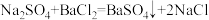 )
)
| 反应前 | 反应后 | ||
| 实验数据 | 硫酸钠溶液的质量/g | 氯化钡溶液的质量/g | 反应后溶液质量/g |
| 100 | 100 | 176.7 | |
(1)产生BaSO4的质量为
(2)所用硫酸钠溶液中溶质的质量分数。(温馨提示:
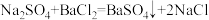 )
)
您最近一年使用:0次
解题方法
5 . 工业生产中会产生有害的SO2气体,常用氢氧化钠溶液来进行尾气处理。化学方程式为:SO2+2NaOH =Na2SO3+H2O。现工厂用100t氢氧化钠溶液吸收工厂尾气中的SO2气体,若恰好完全反应后测得溶液的总质量为106.4t。试计算:
(1)吸收SO2气体的质量为___________ t,
(2)该氢氧化钠溶液的溶质质量分数。
(1)吸收SO2气体的质量为
(2)该氢氧化钠溶液的溶质质量分数。
您最近一年使用:0次
名校
6 . 为确定实验室某过氧化氢溶液中溶质的质量分数,小芳同学利用此过氧化氢溶液与二氧化锰混合进行实验,数据记录如下表所示。
计算:
(1)实验中生成的氧气的质量为___________ g。
(2)该过氧化氢溶液的溶质质量分数。(温馨提示: )
)
| 反应前物质的质量/g | 充分反应后剩余物质的总质量/g | |
| 过氧化氢溶液 | 二氧化锰 | |
| 34 | 0.3 | 32.7 |
(1)实验中生成的氧气的质量为
(2)该过氧化氢溶液的溶质质量分数。(温馨提示:
 )
)
您最近一年使用:0次
解题方法
7 . 某工厂化验室用200g的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸(该产品中其它物质不与NaOH反应),恰好完全反应,得到142g溶质质量分数为10%的Na2SO4溶液。(化学方程式:2NaOH+H2SO4=Na2SO4+2H2O)求:
(1)生成的Na2SO4的质量为____ g。
(2)所用氢氧化钠溶液的溶质质量分数。
(1)生成的Na2SO4的质量为
(2)所用氢氧化钠溶液的溶质质量分数。
您最近一年使用:0次
2024-06-13更新
|
14次组卷
|
2卷引用:2024年云南省昆明市西山区初中学业水平考试第二次模拟考试化学试卷和答案
名校
解题方法
8 . 实验室有一瓶未知浓度的盐酸。为测定该盐酸中溶质的质量分数,化学兴趣小组向36.5g该盐酸中逐滴滴入质量分数为20%的氢氧化钠溶液,所得溶液温度与加入氢氧化钠溶液质量的变化关系如图所示。
(1)氢氧化钠与盐酸反应_______ (填“放出”或“吸收”)热量。
(2)计算该盐酸中溶质的质量分数。(化学方程式:NaOH+HCl=NaCl+H2O)

(1)氢氧化钠与盐酸反应
(2)计算该盐酸中溶质的质量分数。(化学方程式:NaOH+HCl=NaCl+H2O)
您最近一年使用:0次
解题方法
9 . 农业上常用氯化钠溶液来选种。化学兴趣小组从农科站取来36g氯化钠溶液测定其溶质的质量分数。向36g氯化钠溶液中逐滴滴入硝酸银溶液至不再产生白色沉淀,共消耗硝酸银溶液100g,过滤,测得滤液质量为121.65g。计算:
(温馨提示:NaCl+AgNO3=AgCl↓+NaNO3)
(1)产生沉淀的质量为_______ g。
(2)该氯化钠溶液中溶质的质量分数。
(温馨提示:NaCl+AgNO3=AgCl↓+NaNO3)
(1)产生沉淀的质量为
(2)该氯化钠溶液中溶质的质量分数。
您最近一年使用:0次
名校
解题方法
10 . 某兴趣小组从灌装可乐瓶上剪下一块10g的铝片放入烧杯中,再向其中加入90g过量的稀盐酸,反应后得到99.6g的溶液(假设铝片中的杂质均能与酸反应,但没有气体产生)。请计算:
(1)反应生成气体的质量为___________ g。
(2)可乐罐中未氧化的铝的质量分数。(温馨提示:2Al+6HCl=2AlCl3+3H2↑)
(1)反应生成气体的质量为
(2)可乐罐中未氧化的铝的质量分数。(温馨提示:2Al+6HCl=2AlCl3+3H2↑)
您最近一年使用:0次



