1 . 下图“黑面包”实验中,加入浓硫酸和水时,绵白糖变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。小组同学实验探究影响实验效果的因素。
Ⅰ.绵白糖的主要成分是蔗糖。
Ⅱ.实验中涉及的化学反应有:
①蔗糖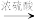 碳+水
碳+水
②C + 2H2SO4 CO2↑+ 2SO2↑+ 2H2O
CO2↑+ 2SO2↑+ 2H2O
③2KMnO4 + 3SO2 + 2H2O=K2SO4 + 2MnO2↓+ 2H2SO4
【进行实验】在100 mL烧杯中进行实验,实验数据记录如下:
说明:用产物高度简单衡量实验效果,高度越高,实验效果越好。
【解释与结论】
(1)绵白糖中一定含有的元素有______ 。
(2)0.5%高锰酸钾溶液的作用是______ 。
(3)根据实验数据推断,在100 mL烧杯中,使用10 g绵白糖进行实验,选择最佳的浓硫酸体积和水的滴数分别是______ 。
(4)实验①~⑤的目的是______ 。
(5)不能得出“绵白糖质量、浓硫酸体积等条件相同时,水滴数越多,效果越好”的结论,依据的实验是______ (填序号)。
【反思与评价】
(6)为进一步证明“烧杯的体积小,实验效果更明显”的结论,需要补做实验:在50 mL和250 mL烧杯中分别加入10 g绵白糖、5 mL浓硫酸、10滴水。下列现象属于50 mL烧杯中的是______(填序号)。

Ⅰ.绵白糖的主要成分是蔗糖。
Ⅱ.实验中涉及的化学反应有:
①蔗糖
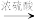 碳+水
碳+水②C + 2H2SO4
 CO2↑+ 2SO2↑+ 2H2O
CO2↑+ 2SO2↑+ 2H2O③2KMnO4 + 3SO2 + 2H2O=K2SO4 + 2MnO2↓+ 2H2SO4
【进行实验】在100 mL烧杯中进行实验,实验数据记录如下:
| 实验 | 绵白糖质量/g | 浓硫酸体积/mL | 水滴数 | 产物高度/cm |
| ① | 10 | 5 | 10 | 4.5 |
| ② | 20 | 5 | 10 | 6.8 |
| ③ | 30 | 5 | 10 | 10.0 |
| ④ | 35 | 5 | 10 | 11.5 |
| ⑤ | 40 | 5 | 10 | 11.5 |
| ⑥ | 10 | 10 | 10 | 9.0 |
| ⑦ | 10 | 15 | 10 | 7.0 |
| ⑧ | 10 | 5 | 20 | 8.0 |
| ⑨ | 10 | 5 | 30 | 6.2 |
| ⑩ | 10 | 5 | 40 | 5.0 |
【解释与结论】
(1)绵白糖中一定含有的元素有
(2)0.5%高锰酸钾溶液的作用是
(3)根据实验数据推断,在100 mL烧杯中,使用10 g绵白糖进行实验,选择最佳的浓硫酸体积和水的滴数分别是
(4)实验①~⑤的目的是
(5)不能得出“绵白糖质量、浓硫酸体积等条件相同时,水滴数越多,效果越好”的结论,依据的实验是
【反思与评价】
(6)为进一步证明“烧杯的体积小,实验效果更明显”的结论,需要补做实验:在50 mL和250 mL烧杯中分别加入10 g绵白糖、5 mL浓硫酸、10滴水。下列现象属于50 mL烧杯中的是______(填序号)。
| A.放出热量 | B.有刺激性气味 | C.产物高度2.3 cm | D.产物高度7.5 cm |
您最近一年使用:0次
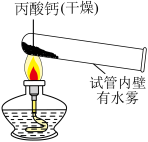
2 . 丙酸钙为白色固体,易溶于水,可作食品防霉剂,国家标准规定了其用于制作面食、糕点时每千克面粉中的最大使用量。小组同学实验探究其性质和防霉的效果。
Ⅰ.探究丙酸钙的性质
【进行实验】用下图装置(夹持仪器已略去)完成实验,记录如下:
【解释与结论】
(1)由①中现象说明丙酸钙一定含有_____ 元素。
(2)查阅资料得知丙酸钙与盐酸反应无气体生成。在实验②中,若要证明①中冷却后的固体里含有碳酸盐,则烧杯中A溶液的溶质是_____ 。
Ⅱ.探究丙酸钙防霉的效果
【进行实验】分别按下列①~⑧的配方蒸制8个馒头,冷却后置于密封袋中,记录如下:
【解释与结论】
(3)第1组,③中X为_____ 。
(4)设计第2组实验的目的是_____ 。
(5)在①-⑧实验中,能证明“有无蔗糖对丙酸钙防霉效果无影响”的所有实验组合是_____ 。
【反思与评价】
(6)结合生活经验,你对日常使用的食品添加剂有什么看法:_____ (一条即可)。
Ⅰ.探究丙酸钙的性质
【进行实验】用下图装置(夹持仪器已略去)完成实验,记录如下:
| 序号 | ① | ② |
| 装置 |
|
|
(1)由①中现象说明丙酸钙一定含有
(2)查阅资料得知丙酸钙与盐酸反应无气体生成。在实验②中,若要证明①中冷却后的固体里含有碳酸盐,则烧杯中A溶液的溶质是
Ⅱ.探究丙酸钙防霉的效果
【进行实验】分别按下列①~⑧的配方蒸制8个馒头,冷却后置于密封袋中,记录如下:
| 组别 | 第1组 | 第2组 | |||||||
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 配方 | 面粉/g | 50 | 50 | 50 | 50 | 50 | 50 | 50 | 50 |
| 酵母/g | 0.75 | 0.75 | X | 0.75 | 0.75 | 0.75 | 0.75 | 0.75 | |
| 蔗糖/g | 0 | 0 | 0 | 0 | 5 | 5 | 5 | 5 | |
| 丙酸钙/g | 0 | 0.06 | 0.10 | 0.15 | 0 | 0.06 | 0.10 | 0.15 | |
| 开始发霉时间 | 第3天 | 第4天 | 第5天 | 第6天 | 第3天 | 第4天 | 第5天 | 第6天 | |
(3)第1组,③中X为
(4)设计第2组实验的目的是
(5)在①-⑧实验中,能证明“有无蔗糖对丙酸钙防霉效果无影响”的所有实验组合是
【反思与评价】
(6)结合生活经验,你对日常使用的食品添加剂有什么看法:
您最近一年使用:0次
解题方法
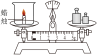
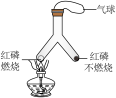
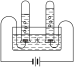
3 . 下列实验方案不能达到实验目的的是
| 实验方案 |
|
|
|
|
| 实验目的 | A.验证质量守恒定律 | B.探究可燃物燃烧需要温度达到着火点 | C.验证CO2的密度比空气大 | D.探究水的组成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
昨日更新
|
27次组卷
|
2卷引用:2024年陕西省延安市初中学业水平考试化学临考冲刺卷(C)D
解题方法
4 . 载人航天器利用 进行
进行 再生,反应如下:
再生,反应如下:
①
②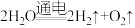
(1)①中,若消耗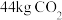 ,计算理论上生成
,计算理论上生成 的质量(写出计算过程及结果)。
的质量(写出计算过程及结果)。
(2)若①中生成的水全部参与②,则消耗的 与生成的
与生成的 的分子个数比为
的分子个数比为______ 。
 进行
进行 再生,反应如下:
再生,反应如下:①

②
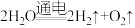
(1)①中,若消耗
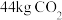 ,计算理论上生成
,计算理论上生成 的质量(写出计算过程及结果)。
的质量(写出计算过程及结果)。(2)若①中生成的水全部参与②,则消耗的
 与生成的
与生成的 的分子个数比为
的分子个数比为
您最近一年使用:0次
解题方法
5 . 甲、乙、丙、丁四种物质在密闭容器内反应前后的质量关系如图所示,下列说法错误的是

| A.X=19 | B.该反应为分解反应 |
| C.丙可能是该反应的催化剂 | D.甲、乙的相对分子质量之比可能为1:16 |
您最近一年使用:0次
2024·山西·三模
名校
解题方法
6 . 中华民族对宇宙奥秘的探索从未间断。迈向深空、挺进深蓝、钻入深地……如今,一项项“上天入海陆上”的重大工程正在加速推进,助力中国经济稳健前行。________ (填名称),煤油在氧气中充分燃烧,生成水和二氧化碳,由此可以推断煤油中一定含有的元素是________ 。
2.图2“挺进深蓝”:福建舰顺利完成海试,对我国海军具有里程碑意义,标志着我国超级航母时代已经开始。航母外壳用特制涂料覆盖,是为了防止钢铁材料与________ 接触而锈蚀,制造航母使用大量的钢铁,工业上用赤铁矿冶炼铁的化学方程式为________ 。
3.图3“钻入深地”:中国石油塔里木油田深地塔科1井钻探深度突破10000米,我国超深油气勘探正式步入万米时代,万米地下的地层温度超过200摄氏度,地层压力超过130兆帕。所用的金刚石钻头使用时要注意避免温度太高,原因是________ (用化学方程式表示),我国深层超深层新增油气储量占比逐年增大,天然气的主要成分甲烷燃烧的现象是________ 。
4.火箭、航母和钻探机这些大国重器的建造与发展离不开电力支撑。新建成投运的大容量钠离子电池储能电站——伏林钠离子电池储能电站每年能发出清洁电能7300万度。钠原子与钠离子的区别是________ (写1点)不同,钠离子的结构示意图为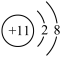 ,则钠离子的核电荷数是
,则钠离子的核电荷数是________ 。

2.图2“挺进深蓝”:福建舰顺利完成海试,对我国海军具有里程碑意义,标志着我国超级航母时代已经开始。航母外壳用特制涂料覆盖,是为了防止钢铁材料与
3.图3“钻入深地”:中国石油塔里木油田深地塔科1井钻探深度突破10000米,我国超深油气勘探正式步入万米时代,万米地下的地层温度超过200摄氏度,地层压力超过130兆帕。所用的金刚石钻头使用时要注意避免温度太高,原因是
4.火箭、航母和钻探机这些大国重器的建造与发展离不开电力支撑。新建成投运的大容量钠离子电池储能电站——伏林钠离子电池储能电站每年能发出清洁电能7300万度。钠原子与钠离子的区别是
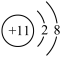 ,则钠离子的核电荷数是
,则钠离子的核电荷数是
您最近一年使用:0次
解题方法
7 . 真空热还原法生产钙的主要转化过程如图:_______ 。
(2)II中反应有两种产物,固体X一定含有氧元素和铝元素,从元素守恒角度说明理由_______ 。

(2)II中反应有两种产物,固体X一定含有氧元素和铝元素,从元素守恒角度说明理由
您最近一年使用:0次
解题方法
8 . 高纯CaCO3广泛应用于医药、生产、生活领域。工业上利用石灰石(含杂质SiO2)制备高纯CaCO3的工艺流程如图:______ 。
(2)上述流程中,除去杂质SiO2,利用其性质是不溶于水、______ 。
(3)高纯CaCO3中的氧元素来自于______(填序号)。

(2)上述流程中,除去杂质SiO2,利用其性质是不溶于水、
(3)高纯CaCO3中的氧元素来自于______(填序号)。
| A.CO2 | B.H2O | C.CaCl2 |
您最近一年使用:0次
解题方法
9 . 氨是重要的工业原料。某化肥厂用氨生产化肥 (NH4)2SO4的工艺流程如下:_______ 。
(2)煅烧炉中,碳酸钙在高温条件下发生分解反应的方程式为_______ 。
(3)加入的X为_______(填字母序号)。

(2)煅烧炉中,碳酸钙在高温条件下发生分解反应的方程式为
(3)加入的X为_______(填字母序号)。
| A.H2SO4 | B.CaSO4 | C.SO2 |
您最近一年使用:0次
解题方法
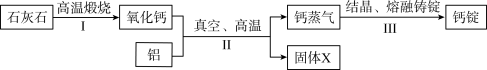
10 . 真空热还原法生产钙的主要转化过程如下:_____ 。
(2)Ⅱ中反应有两种产物,固体X一定含有氧元素和_____ 。
(3)Ⅲ中发生的是_____ (填“物理”或“化学”)变化。
(2)Ⅱ中反应有两种产物,固体X一定含有氧元素和
(3)Ⅲ中发生的是
您最近一年使用:0次