解题方法
1 . 好奇的同学们为了探测鸡蛋壳中碳酸钙的含量,从家里收集了鸡蛋壳清洗干燥后带到学校实验室。取12g 鸡蛋壳样品于烧杯中,加入稀盐酸至不再产生气泡(假设鸡蛋壳中其他成分不与稀盐酸反应,生成气体全部逸出),共加入稀盐酸100g, 此时烧杯内混合物的质量为107.6g。请计算。
(1)生成二氧化碳的质量为______ g;
(2)鸡蛋壳中碳酸钙的质量是______ g;
(3)所用稀盐酸中溶质的质量分数。(写出计算过程)
(1)生成二氧化碳的质量为
(2)鸡蛋壳中碳酸钙的质量是
(3)所用稀盐酸中溶质的质量分数。(写出计算过程)
您最近一年使用:0次
解题方法
2 . 工业生产中会产生有害的SO2气体,常用氢氧化钠溶液来进行尾气处理。化学方程式为:SO2+2NaOH =Na2SO3+H2O。现工厂用100t氢氧化钠溶液吸收工厂尾气中的SO2气体,若恰好完全反应后测得溶液的总质量为106.4t。试计算:
(1)吸收SO2气体的质量为___________ t,
(2)该氢氧化钠溶液的溶质质量分数。
(1)吸收SO2气体的质量为
(2)该氢氧化钠溶液的溶质质量分数。
您最近一年使用:0次
3 . 过氧化镁( )是一种镁精细化工产品,在医疗及环境保护上均有应用。工业上利用碱式碳酸镁[
)是一种镁精细化工产品,在医疗及环境保护上均有应用。工业上利用碱式碳酸镁[ ]制备过氧化镁的过程如图所示。
]制备过氧化镁的过程如图所示。 和
和 常温下比较稳定,加热时容易发生分解;
常温下比较稳定,加热时容易发生分解;
ⅱ、MgO与 反应放出大量的热。
反应放出大量的热。
(1) 中氢、氧原子的个数比为
中氢、氧原子的个数比为______ 。
(2) 煅烧时分解生成三种氧化物,分别为MgO和
煅烧时分解生成三种氧化物,分别为MgO和______ 、______ (填化学式)。
(3)反应2的化学方程式为 。用40gMgO,理论上可制备
。用40gMgO,理论上可制备 的质量是多少?(写出计算过程)
的质量是多少?(写出计算过程)
(4)加入稳定剂的目的是______ 。
 )是一种镁精细化工产品,在医疗及环境保护上均有应用。工业上利用碱式碳酸镁[
)是一种镁精细化工产品,在医疗及环境保护上均有应用。工业上利用碱式碳酸镁[ ]制备过氧化镁的过程如图所示。
]制备过氧化镁的过程如图所示。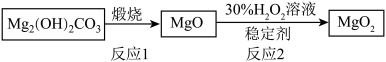
 和
和 常温下比较稳定,加热时容易发生分解;
常温下比较稳定,加热时容易发生分解;ⅱ、MgO与
 反应放出大量的热。
反应放出大量的热。(1)
 中氢、氧原子的个数比为
中氢、氧原子的个数比为(2)
 煅烧时分解生成三种氧化物,分别为MgO和
煅烧时分解生成三种氧化物,分别为MgO和(3)反应2的化学方程式为
 。用40gMgO,理论上可制备
。用40gMgO,理论上可制备 的质量是多少?(写出计算过程)
的质量是多少?(写出计算过程)(4)加入稳定剂的目的是
您最近一年使用:0次
解题方法
4 . 我国化学家侯德榜发明了侯氏制碱法,为世界制碱工业做出了杰出贡献。实际生产的纯碱产品中会混有少量的氯化钠。为测定某纯碱样品中碳酸钠的质量分数,称取22.0g该样品放入烧杯中,加入稀盐酸146.0g,恰好完全反应,称得烧杯内物质的总质量为159.2g。请计算:
(1)生成CO2的质量为______ g。
(2)纯碱样品中碳酸钠的质量分数(写出计算过程,结果精确到0.1%)。
(1)生成CO2的质量为
(2)纯碱样品中碳酸钠的质量分数(写出计算过程,结果精确到0.1%)。
您最近一年使用:0次
2024九年级·江苏无锡·专题练习
解题方法
5 . 阅读下面的科普短文,回答下列问题。
碳在自然界中的循环变化,对于生态环境有极为重要的意义。随着工业生产的高速发展和人们生活水平的提高,排入大气中的CO2越来越多,导致温室效应增强。减少CO2排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的4种主要途径。科学家预测,到2050年,4种途径对全球碳中和的贡献率如图1所示。CO2的吸收是碳封存的首要环节,常选用NaOH、氨水、一乙醇胺等作吸收剂。在研究膜吸收法吸收CO2时,研究人员通过实验比较了一乙醇胺、二乙醇胺、氨基乙酸钾3种吸收剂对烟气中CO2的脱除效果,其结果如图2所示。____ (填“吸收“或“释放”)CO2。
(2)由图1可知,到2050年,对全球碳中和贡献率最大的途径是____ 。
(3)对比图2中三条曲线,得出的结论是:在实验研究的烟气流速范围内,当烟气流速相同时,____ (填物质名称)对烟气中CO2的脱除效果最好。
碳在自然界中的循环变化,对于生态环境有极为重要的意义。随着工业生产的高速发展和人们生活水平的提高,排入大气中的CO2越来越多,导致温室效应增强。减少CO2排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的4种主要途径。科学家预测,到2050年,4种途径对全球碳中和的贡献率如图1所示。CO2的吸收是碳封存的首要环节,常选用NaOH、氨水、一乙醇胺等作吸收剂。在研究膜吸收法吸收CO2时,研究人员通过实验比较了一乙醇胺、二乙醇胺、氨基乙酸钾3种吸收剂对烟气中CO2的脱除效果,其结果如图2所示。
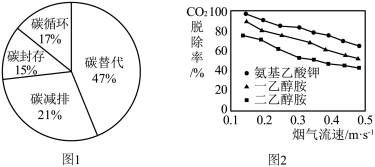
(2)由图1可知,到2050年,对全球碳中和贡献率最大的途径是
(3)对比图2中三条曲线,得出的结论是:在实验研究的烟气流速范围内,当烟气流速相同时,
您最近一年使用:0次
真题
解题方法
6 . 某反应的微观示意图如下、下列说法错误的是
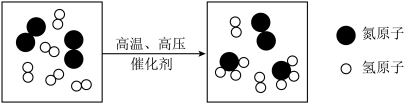
A. 对应物质的化学式是 对应物质的化学式是 | B.该反应前后原子总数不变 |
| C.该反应前后分子总数不变 | D.参加该反应的 与 与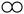 的个数比为 的个数比为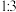 |
您最近一年使用:0次
真题
解题方法
7 . 一定条件下,X、Y、乙、W四种物质在密闭容器中充分反应,测得反应前后各物质质量如下表。
下列说法正确的是
| 物质 | X | Y | Z | W |
| 反应前的质量/g | 6.8 | 1.0 | 93.2 | 0 |
| 反应后的质量/g | 0 | a | 96.8 | 3.2 |
A.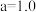 ,Y一定是该反应的催化剂 ,Y一定是该反应的催化剂 | B.该反应一定为化合反应 |
C.X与W相对分子质量之比一定为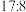 | D.Z与W质量变化之比一定为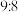 |
您最近一年使用:0次
名校
解题方法
8 . 碳中和指在一定时间内直接或间接产生的二氧化碳或温室气体排放总量,通过植树造林、节能减排等形式,以抵消自身产生的二氧化碳或温室气体排放量,实现正负相抵,达到相对的"零排放"。
(1)化石燃料包括石油、天然气和_______ 。
(2)研究发现“在新型铜-铁基催化下,二氧化碳和水反应可生成甲烷和其他产物”,理论上推测,最终“其他产物”不可能 是_______(填序号)。
(1)化石燃料包括石油、天然气和
(2)研究发现“在新型铜-铁基催化下,二氧化碳和水反应可生成甲烷和其他产物”,理论上推测,最终“其他产物”
| A.四氧化三铁 | B.氧气 | C.肼 |
您最近一年使用:0次
解题方法
9 . 7分)阅读下列短文并回答问题。
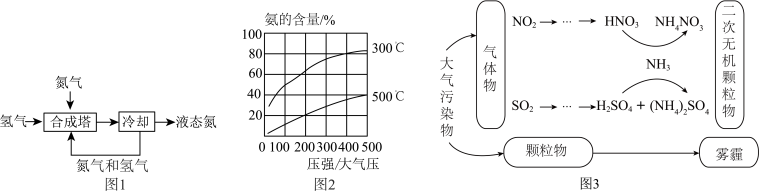
氨气是地球大气中唯一呈碱性的气体,它无色,有强烈的刺激气味,密度小于空气,极易溶于水,在常温下加压即可使其液化,可用于制造硝酸和氨肥,是一种重要的化学物质。氨气主要来自于人工合成,1909年,德国化学家弗里茨·哈伯成功地利用氮气和氢气合成出氨。工业合成氨的流程如图1所示。为了找到合成氨反应合适的催化剂,人们做了6500多次实验,发现铁触媒效果较好。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨,当容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图2所示。1913年,第一座合成氨工厂建立,如今全球合成氨年产量超千万吨,其中大约85%的氨用于生产氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
(1)工业上可用________ 的方法获得合成氨的原料 。
。
(2)从“合成塔”中出来的气体是________ (填“纯净物”或“混合物”)。
(3)可通过甲烷和 在高温下反应得到CO和原料气
在高温下反应得到CO和原料气 ,该反应的化学方程式为
,该反应的化学方程式为________ 。
(4)科学家反复研究合成氨反应催化剂的目的是________ 。
(5)雾霾中二次无机颗粒物主要是硝酸铵和硫酸铵,其形成过程中发生了化合反应,其中一个的所有反应物和生成物都含有同种元素,请写出其化学反应方程式________ 。
(6)相同质量的氨气,生成二次无机颗粒物的质量比为________ 。
(7)为降低氨气的排放,人类可采取的有效措施有哪些?________ (写一条)。
氨气是地球大气中唯一呈碱性的气体,它无色,有强烈的刺激气味,密度小于空气,极易溶于水,在常温下加压即可使其液化,可用于制造硝酸和氨肥,是一种重要的化学物质。氨气主要来自于人工合成,1909年,德国化学家弗里茨·哈伯成功地利用氮气和氢气合成出氨。工业合成氨的流程如图1所示。为了找到合成氨反应合适的催化剂,人们做了6500多次实验,发现铁触媒效果较好。在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨,当容器中氨的含量不再发生变化时(平衡时),测得氨的含量分别与温度和压强的关系如图2所示。1913年,第一座合成氨工厂建立,如今全球合成氨年产量超千万吨,其中大约85%的氨用于生产氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
(1)工业上可用
 。
。(2)从“合成塔”中出来的气体是
(3)可通过甲烷和
 在高温下反应得到CO和原料气
在高温下反应得到CO和原料气 ,该反应的化学方程式为
,该反应的化学方程式为(4)科学家反复研究合成氨反应催化剂的目的是
(5)雾霾中二次无机颗粒物主要是硝酸铵和硫酸铵,其形成过程中发生了化合反应,其中一个的所有反应物和生成物都含有同种元素,请写出其化学反应方程式
(6)相同质量的氨气,生成二次无机颗粒物的质量比为
(7)为降低氨气的排放,人类可采取的有效措施有哪些?
您最近一年使用:0次
真题
解题方法
10 . 碱石灰(CaO、NaOH)常用作气体的干燥剂。化学兴趣小组为测定某种碱石灰中CaO的质量分数,将10g碱石灰加入到80gNa2CO3溶液中,发生反应: 。待碱石灰中CaO完全反应后,测得生成CaCO3固体的质量为10g。
。待碱石灰中CaO完全反应后,测得生成CaCO3固体的质量为10g。
回答下列问题:
(1)除去CaCO3固体后,所得溶液的质量为______ g。
(2)求该碱石灰中CaO的质量分数。(写出计算过程)
 。待碱石灰中CaO完全反应后,测得生成CaCO3固体的质量为10g。
。待碱石灰中CaO完全反应后,测得生成CaCO3固体的质量为10g。回答下列问题:
(1)除去CaCO3固体后,所得溶液的质量为
(2)求该碱石灰中CaO的质量分数。(写出计算过程)
您最近一年使用:0次



