解题方法
1 . 如图所示为实验室中常见气体制备、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学利用其进行下列化学实验。试回答下列问题:

(1)以石灰石和稀盐酸为原料,在实验室中制备并收集纯净、干燥的二氧化碳气体。按照要求设计实验装置,连接仪器、检查装置的气密性,进行实验(少量氯化氢气体可用饱和碳酸氢钠溶液吸收)。
①所选仪器的连接顺序为________ (从左到右填写仪器序号字母)。
②中国已向世界宣布2030年前实现“碳达峰”的国家目标。“碳达峰”是指国家整体二氧化碳气体排放量达到峰值。有研究表明,当前全球每年人为向大气排放二氧化碳约440亿吨,在这些二氧化碳中含碳元素的质量为______ 亿吨。
(2)用锌和稀硫酸为原料制取干燥的氢气,并测定ag某不纯氧化铁样品中Fe2O3的质量分数(假设样品中杂质不挥发,也不参与反应),设计了实验方案,所选仪器按“B→C1→A→C2→C3”的顺序连接(C1、C2、C3为浓硫酸洗气瓶),检查装置的气密性,然后进行实验。(假设发生的化学反应都充分反应:Fe2O3+3H2 2Fe+3H2O)
2Fe+3H2O)
①点燃纯净的氢气,会产生______ 色火焰,该过程将______ 能转化为热能和______ 能。
②在实验过程中,洗气瓶C3的作用是_______ 。实验结束后,若C1质量增加了bg,C2质量增加了cg,则氧化铁样品中Fe2O3的质量为______ (结果用代数式表示)。
③通过测量反应前后仪器A处玻璃管内药品的质量,来测算出该样品中Fe2O3的质量分数。反应前将ag氧化铁样品装入仪器A玻璃管内,充分反应后冷却,测得此时仪器A玻璃管内药品的质量为dg,则该氧化铁样品中Fe2O3的质量分数为_______ ×100%(结果用代数式表示)。若其他操作正确,反应结束后立即停止通氢气,再熄灭酒精灯,这样计算出的氧化铁样品纯度与实际值相比_______ (填“偏大”“偏小”“基本一致”之一)。

(1)以石灰石和稀盐酸为原料,在实验室中制备并收集纯净、干燥的二氧化碳气体。按照要求设计实验装置,连接仪器、检查装置的气密性,进行实验(少量氯化氢气体可用饱和碳酸氢钠溶液吸收)。
①所选仪器的连接顺序为
②中国已向世界宣布2030年前实现“碳达峰”的国家目标。“碳达峰”是指国家整体二氧化碳气体排放量达到峰值。有研究表明,当前全球每年人为向大气排放二氧化碳约440亿吨,在这些二氧化碳中含碳元素的质量为
(2)用锌和稀硫酸为原料制取干燥的氢气,并测定ag某不纯氧化铁样品中Fe2O3的质量分数(假设样品中杂质不挥发,也不参与反应),设计了实验方案,所选仪器按“B→C1→A→C2→C3”的顺序连接(C1、C2、C3为浓硫酸洗气瓶),检查装置的气密性,然后进行实验。(假设发生的化学反应都充分反应:Fe2O3+3H2
 2Fe+3H2O)
2Fe+3H2O)①点燃纯净的氢气,会产生
②在实验过程中,洗气瓶C3的作用是
③通过测量反应前后仪器A处玻璃管内药品的质量,来测算出该样品中Fe2O3的质量分数。反应前将ag氧化铁样品装入仪器A玻璃管内,充分反应后冷却,测得此时仪器A玻璃管内药品的质量为dg,则该氧化铁样品中Fe2O3的质量分数为
您最近一年使用:0次
解题方法
2 . 英国物理学家、化学家波义耳和法国化学家拉瓦锡曾做过貌似相同的两个实验,实验如下图,关于这两个实验的说法正确的是

| A.两个实验均可用于测定空气中氧气的含量 |
| B.两个实验中,曲颈甑内汞的表面都有黑色物质生成 |
| C.拉瓦锡的实验中,玻璃钟罩内汞的液面逐渐上升,达到一定高度后不再变化 |
| D.波义耳的实验中,曲颈甑内物质加热后质量增加的现象不能用质量守恒定律来解释 |
您最近一年使用:0次
3 . 拉瓦锡用定量的方法研究了空气的成分。某兴趣小组利用氧气传感器来检测足量红磷燃烧过程中氧气的含量,如图所示,下列判断正确的是

| A.a点时容器内氮气体积分数为85% |
| B.容器内物质总质量:b点>c点 |
| C.氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 |
| D.此实验测得空气中氧气的质量分数为18% |
您最近一年使用:0次
2023-06-21更新
|
1887次组卷
|
67卷引用:山东省枣庄市市中区2023-2024学年九年级上学期期中化学试题
山东省枣庄市市中区2023-2024学年九年级上学期期中化学试题山东省德州市乐陵市2023-2024学年九年级上学期期中化学试题山东省枣庄市薛城区2023-2024学年九年级上学期学业综合素养监测化学试题山东省滕州市藤东中学2023-2024学年九年级化学上学期期末模拟考试试卷山东省菏泽市东明县2023-2024学年九年级上学期期末化学试题山东省青岛市莱西市济南路中学实验中学等2023-2024学年八年级下学期3月月考化学试题山东省日照市曲阜师范大学附属实验学校2023-2024学年下学期九年级3月月考化学试卷山东省淄博市高青县2023-2024学年八年级下学期4月期中化学试题(已下线)2024年山东省枣庄市台儿庄区中考第二次模拟考试化学试题2023年湖南省衡阳市中考化学真题(已下线)第15讲 化学反应中的质量关系-【暑假自学课】2023年新九年级化学暑假精品课(沪教版)(已下线)专题02 空气(第01期)-学易金卷:2023年中考化学真题分项汇编(全国通用)(已下线)专题02 空气-学易金卷:三年(2021-2023)中考化学真题分项汇编(全国通用)(已下线)专题02 空气 -学易金卷:三年(2021-2023)中考化学真题分项汇编(湖南专用)(已下线)2.1 空气的成分(第一课时)(同步练习)-九年级化学上册同步精品课堂(科粤版2012)(已下线)第6课 空气的组成-【帮课堂】2023-2024学年九年化学上册同步学与练(人教版)(已下线)实验05 空气中氧气含量的测定-【同步实验课】2023-2024学年九年级化学上册教材实验大盘点(人教版)(已下线)第二章 空气、物质的构成【单元测试·考点卷】(11大核心考点)-2023-2024学年九年化学上册单元速记·巧练(科粤版)(已下线)课题1 空气(第1课时)(分层作业)-【上好课】九年级化学上册同步备课系列(人教版)(已下线)第05讲 人类赖以生存的空气(第1课时)(分层练习)-2023-2024学年九年级化学第一学期同步精品课堂(沪教版·上海)(已下线)第一次月考B卷(上海专用,沪教版·上海)-学易金卷:2023-2024学年九年化学上学期第一次月考(已下线)第二单元 我们周围的空气B卷-2023-2024学年九年级化学上册同步测试优选卷(人教版)(已下线)易错05 空气中氧气含量的探究 -2023-2024学年九年级化学上册易混易错微考点(人教版)湖北省恩施州咸丰县民族中学2023-2024学年九年级上学期第一次月考化学试题安徽省宣城市第六中学2023-2024学年九年级上学期10月月考化学试题(已下线)第1章 开启化学之门【考点清单】(讲+练)-2023-2024学年九年级化学上学期期中考点大串讲(沪教版·全国)山西省运城市稷山县2023-2024学年九年级上学期期中化学试题(已下线)课题1 质量守恒定律-2023-2024学年九年级化学同步学习中考真题练(人教版)辽宁省沈阳市和平区南昌初级中学2023-2024学年九年级上学期11月月考化学试题湖南省张家界市永定区2023-2024学年九年级上学期期中化学试题江苏省泰州市靖江外国语、泰州市二附中联考2023-2024学年九年级上学期11月期中化学试题安徽省淮南市洞山中学2023-2024学年九年级上学期第二次月考化学试卷(已下线)XDRzkgshxzw902湖北省武汉市光谷实验中学2023-2024学年九年级上学期11月月考化学试卷黑龙江省哈尔滨市第一一三中学校2023-2024学年八年级上学期11月月考化学试题(已下线)专题02 空气和常见化合物-【寒假自学课】2024年九年级化学寒假提升学与练(人教版)福建省漳州市第三中学2023-2024学年九年级上学期12月月考化学试卷(已下线)专题03 空气 氧气(练习)-2024年中考化学一轮复习讲练测(全国通用)(已下线)专题03 空气 氧气(讲义)-2024年中考化学一轮复习讲练测(全国通用)(已下线)第2单元 我们周围的空气 (B卷 真题通关卷)-2023-2024学年九年级化学上册同步考点解读与专题训练(人教版)(已下线)第二单元 我们周围的空气【过习题】-2023-2024学年九年级化学单元复习过过过(人教版)(已下线)寒假作业02 空气 氧气-【寒假分层作业】2024年九年级化学寒假培优练(沪教版)(已下线)化学(南通卷)-学易金卷:2024年中考第一次模拟考试(已下线)九年级化学开学摸底考(广西专用,人教版1-9单元)-2023-2024学年初中下学期开学摸底考试(已下线)专题01 空气和氧气(考点专练)-备战2024年中考化学考点微专题(广东专用)江苏省苏州市吴江区松陵第一中学2023-2024学年九年级上学期10月考化学试卷湖南省娄底市2023-2024学年九年级上学期期末化学试题山西省晋城市阳城县2023-2024学年九年级上学期期末化学试题(已下线)第2章 身边的化学物质(讲义)-备战2024年中考化学一轮复习考点帮(沪教版·全国)(已下线)第一讲 空气 氧气-备战2024年中考化学一轮复习学·练·考(全国通用)安徽省六安市金安区六安皋城中学2023-2024学年九年级上学期1月期末化学试题(已下线)专题03 空气和氧气-备战2024年中考化学一轮复习考点直击讲义(全国通用)(已下线)2024年中考风向标-全国-空气、氧气安徽省六安市金安区六安皋城中学2023-2024学年九年级下学期3月月考化学试题江苏省南京市江宁区麒麟初级中学2023-2024学年九年级下学期3月练习化学试题(已下线)题型突破03 坐标曲线题-备战2024年中考化学复习题型突破学·练·考(全国通用)(已下线)第1讲 空气中氧气含量的测定 氧气的实验室制取-备战2024年中考化学一轮复习重点实验学·练·考(全国通用)2024口袋书系列 课本回归 专题1 空气2024中考一轮复习考点微专题-专题01空气和氧气-考点专练(已下线)专题02 身边的化学物质(讲练)-2024年中考化学二轮复习讲练测(全国通用)(已下线)专题02 质量守恒定律的应用(7大题型)-2024年中考化学二轮热点题型归纳与变式演练(上海专用)(已下线)易错类型15 坐标曲线“五大”易错点-备战2024年中考化学考试易错题(全国通用)(已下线)专题03 坐标曲线题-2024年中考化学答题技巧与模板构建(已下线)重难点01 空气和氧气-2024年中考化学【热点·重点·难点】专练(全国通用)(已下线)专题三 空气和氧气【六大题型】-备战2024年中考化学二轮轮复习举一反三系列(全国通用)广西岑溪市糯垌中学联考2023-2024学年九年级下学期第四次月考化学试题2024年内蒙古呼伦贝尔市莫旗中考化学一模试题
名校
4 . 在验证质量守恒定律时,某学习小组三位同学分别做了如下实验:(已知:红磷燃烧产生的五氧化二磷会刺激人体呼吸道)

(1)如图A所示,点燃红磷后观察到的现象是剧烈燃烧、产生大量________ 、放出热量,其中小气球的作用是________ 。
(2)上图验证质量守恒定律的实验中,不能达到实验目的是________ (填字母),请你解释不能验证质量守恒的原因是________ 。
(3)另一个学习小组的同学用镁条在空气中燃烧完成验证实验。实验前,同学们预测生成物的质量比镁条的质量大,原因是________ 。而反应后实际测量的结果却是小于镁条的质量,其原因可能是________ (任写一条)。

(1)如图A所示,点燃红磷后观察到的现象是剧烈燃烧、产生大量
(2)上图验证质量守恒定律的实验中,不能达到实验目的是
(3)另一个学习小组的同学用镁条在空气中燃烧完成验证实验。实验前,同学们预测生成物的质量比镁条的质量大,原因是
您最近一年使用:0次
2023-09-02更新
|
475次组卷
|
6卷引用:山东省威海市经济技术开发区皇冠中学2022-2023学年八年级下学期期末化学试题
山东省威海市经济技术开发区皇冠中学2022-2023学年八年级下学期期末化学试题(已下线)随堂检测(鲁教版)第五单元第一节化学反应中的质量守恒A卷2023-2024九化同步课题例题与随堂检测AB卷(鲁教上册)(已下线)第5讲 化学方程式(讲义)-【划重点】2023-2024学年九年级化学上学期期中期末复习精细讲义 (人教版)(已下线)课堂例题(沪教版)第4章第2节化学反应中的质量关系A卷2023-2024九化同步课题例题与随堂检测AB卷(沪教上册)(已下线)第五单元 化学方程式【考题猜想】(23大题型)-2023-2024学年九年级化学上学期期末考点大串讲(人教版)(已下线)第五单元 化学方程式(考点清单)(讲+练)-2023-2024学年九年级化学上学期期末考点大串讲(人教版)
解题方法
5 . 下图是甲、乙两组同学分别设计的质量守恒定律的两个验证实验。请根据图示进行思考回答(假设甲、乙两组药品混合前质量均为 m 前、混合后质量均为m后):
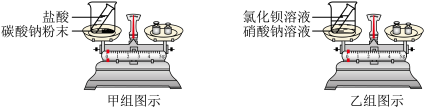
(1)甲组能观察到的实验现象为_________ ,甲组药品混合前、 后质量关系为:m 前>m 后,请解释原因__________ ,该实验若试剂不变,应如何改进此装置_________ ;
(2)乙组药品混合前、后质量关系为:m前=m后,乙组同学认为实验成功,甲组同学认为该实验不能验证质量守恒定律,原因是__________ ;
(3)使用上述实验装置,请你选择另外方案进行实验,既有明显现象又能达到实验目的,所选的药品可以是_______ 和________ (填化学式)。

(1)甲组能观察到的实验现象为
(2)乙组药品混合前、后质量关系为:m前=m后,乙组同学认为实验成功,甲组同学认为该实验不能验证质量守恒定律,原因是
(3)使用上述实验装置,请你选择另外方案进行实验,既有明显现象又能达到实验目的,所选的药品可以是
您最近一年使用:0次
2023-03-19更新
|
71次组卷
|
2卷引用:山东省青岛市第六十五中学2022-2023学年九年级上学期期末化学试题
6 . “化学实验→观察现象→分析推理→得出结论”是化学学习的方法之一。
(1)实验是进行科学探究的重要方式,请根据如图回答问题:

①某兴趣小组的同学设计了如图所示的甲、乙两个实验(托盘天平略)来验证质量守恒定律。小组同学讨论后认为,甲、乙两组实验中只有实验______ 能直接用于验证质量守恒定律,另外一个实验被否定的原因是______ 。
②图丙是某校同学开展的“燃烧的条件”的探究活动,该实验是通过控制温度是否达到可燃物的着火点和控制______ 来探究可燃物燃烧的条件,它采用了______ 的实验方法。
③利用丁图所示方法,把二氧化碳气体慢慢倒入放有燃着蜡烛的烧杯中,下层蜡烛的火焰先熄灭,说明二氧化碳具有______ 的性质。
(2)有A、B、C、D四种物质,已知它们组成中均含有同一种元素,A为单质,B、C为元素组成相同的化合物,D是大理石的主要成分。它们之间有如下转化关系(部分反应物、生成物和反应条件已略去),请回答:

①写出反应④的化学方程式______ 。
②写出C物质的化学式______ ,写出它的一条用途______ 。
③反应①②的基本反应类型相同,都是______ 反应。
④反应③是______ (填“吸热”或“放热”)反应。
⑤已知反应⑤所属的基本反应类型为分解反应,试写出该反应的化学方程式______ 。
(1)实验是进行科学探究的重要方式,请根据如图回答问题:

①某兴趣小组的同学设计了如图所示的甲、乙两个实验(托盘天平略)来验证质量守恒定律。小组同学讨论后认为,甲、乙两组实验中只有实验
②图丙是某校同学开展的“燃烧的条件”的探究活动,该实验是通过控制温度是否达到可燃物的着火点和控制
③利用丁图所示方法,把二氧化碳气体慢慢倒入放有燃着蜡烛的烧杯中,下层蜡烛的火焰先熄灭,说明二氧化碳具有
(2)有A、B、C、D四种物质,已知它们组成中均含有同一种元素,A为单质,B、C为元素组成相同的化合物,D是大理石的主要成分。它们之间有如下转化关系(部分反应物、生成物和反应条件已略去),请回答:

①写出反应④的化学方程式
②写出C物质的化学式
③反应①②的基本反应类型相同,都是
④反应③是
⑤已知反应⑤所属的基本反应类型为分解反应,试写出该反应的化学方程式
您最近一年使用:0次
解题方法
7 . 化学革命是发生在十八世纪末英国和法国的一场深刻的化学学科的变革。英国物理学家、化学家波义耳和法国化学家拉瓦锡曾做过貌似相同的两个实验(见图)。关于这两个实验的说法正确的是


| A.两个实验都可用于测定空气中氧气的含量 |
| B.波义耳的实验比拉瓦锡的更简捷准确 |
| C.波义耳的实验中,金属加热后质量增加,该现象不能用质量守恒定律解释 |
| D.拉瓦锡的实验中,玻璃钟罩内液面逐渐上升,达到一定高度后不再变化 |
您最近一年使用:0次
2021-10-28更新
|
50次组卷
|
2卷引用:山东省青岛市市北区2020-2021学年九年级上学期期中化学试题
8 . 请结合以下图示,回答问题。

(1)如图1所示,电解水的实验中正极与负极产生气体的质量比为____ 。
(2)如图2所示,小明用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种基本反应类型直接生成水(如图中的H2O2、O2),X不能选择下列A、B、C、D4种物质中的____ (填序号)
ACuO BH2CO3 CC2H5OH DCa(OH)2
(3)如图3所示,“→”表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是____ (用“甲、乙、丙”表示)。
(4)如图4所示,某同学用此装置验证质量守恒定律的实验,下列药品不能达到该实验目的的是____ (填序号)。
A 火碱和稀盐酸反应 B 铁和稀盐酸反应
C 铁和硝酸锌溶液反应 D 硫酸和氯化钠溶液

(1)如图1所示,电解水的实验中正极与负极产生气体的质量比为
(2)如图2所示,小明用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种基本反应类型直接生成水(如图中的H2O2、O2),X不能选择下列A、B、C、D4种物质中的
ACuO BH2CO3 CC2H5OH DCa(OH)2
(3)如图3所示,“→”表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是
(4)如图4所示,某同学用此装置验证质量守恒定律的实验,下列药品不能达到该实验目的的是
A 火碱和稀盐酸反应 B 铁和稀盐酸反应
C 铁和硝酸锌溶液反应 D 硫酸和氯化钠溶液
您最近一年使用:0次
9 . 下图是甲、乙两组同学分别设计的质量守恒定律的两个验证实验.请根据图示进行思考回答(假设甲、乙两组药品混合前质量均为m前、混合后质量均为m后):

(1)甲组药品混合前、后质量关系为:m前>m后,请解释原因_________________________ ,该实验若试剂不变,应如何改进此装置________________________ ;
(2)乙组药品混合前、后质量关系为:m前=m后,乙组同学认为实验成功,你同意他的观点吗?_________ (填“同意”或“不同意”);
(3)使用上述实验装置,请你选择另外方案进行实验,既有明显现象又能达到实验目的,所选的药品可以是_________ 和_________ (填化学式).

(1)甲组药品混合前、后质量关系为:m前>m后,请解释原因
(2)乙组药品混合前、后质量关系为:m前=m后,乙组同学认为实验成功,你同意他的观点吗?
(3)使用上述实验装置,请你选择另外方案进行实验,既有明显现象又能达到实验目的,所选的药品可以是
您最近一年使用:0次
2016-11-28更新
|
181次组卷
|
3卷引用:2016届山东省青岛市某中学九年级上学期月考化学试卷
解题方法
10 . 煤燃烧产生的二氧化硫排放到空气中,与大气中的水发生化学反应,生成酸,随雨水降落到地面,便形成酸雨。酸雨能酸化土壤、污染水体、腐蚀建筑物及文物古迹,加速金属制品的锈蚀,已成为全球性灾害。为减少或消除煤炭燃烧产生二氧化硫,人们向煤炭中加入石灰石或生石灰作为固硫剂制成型煤。型煤燃烧后,产生的二氧化硫以硫酸盐形式留在灰渣中,从而达到减少污染的目的。
(1)煤燃烧产生的二氧化硫的原因是煤炭中含有________ 元素。二氧化硫与水反应生成亚硫酸 ,亚硫酸中硫元素的化合价为
,亚硫酸中硫元素的化合价为________ 。
(2)生石灰与二氧化硫反应生成亚硫酸钙,反应的化学方程式为________ 。型煤在燃烧过程中,会将亚硫酸钙转化为硫酸钙,该反应中的另一种反应物是________ 。
(1)煤燃烧产生的二氧化硫的原因是煤炭中含有
 ,亚硫酸中硫元素的化合价为
,亚硫酸中硫元素的化合价为(2)生石灰与二氧化硫反应生成亚硫酸钙,反应的化学方程式为
您最近一年使用:0次



