1 . 化学课堂中,老师演示了“吹气生火”实验,他向包有过氧化钠(Na2O2)粉末的脱脂棉上用导管吹气,脱脂棉燃烧了起来。同学们对该实验产生了浓厚兴趣,进行了如下探究。
探究一:脱脂棉燃烧的原因。
[作出猜想]
(1)根据燃烧条件分析:
①脱脂棉是可燃物;
②吹出的气体可能与过氧化钠反应生成了氧气;
③反应放出热量,满足了温度达到脱脂棉的________ 。
[进行实验]
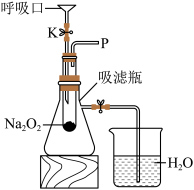
(2)在如图所示装置中,向过氧化钠粉末中不断吹气,观察到过氧化钠粉末由淡黄色逐渐变为白色,在导管口P处放置_______ ,木条复燃,说明试管内生成了氧气。同时还观察到_____ ,说明反应还放出了热量。
探究二:试管内残留白色固体的成分。
[查阅资料]①吹出的气体主要成分有氮气、二氧化碳和水蒸气;② 过氧化钠与氮气不反应。
[作出猜想]
(3)猜想1:CO2参加反应,固体成分是Na2CO3;
猜想2:H2O参加反应,固体成分是NaOH;
猜想3:CO2和H2O均参加反应,固体成分是_____ 。
[实验验证]
(4)实验过程如下:
[实验结论]
(5)过氧化钠与二氧化碳、水蒸气都能反应,猜想3正确。请写出过氧化钠与二氧化碳反应的化学方程式:_____ 。
[拓展延伸]
(6)化工厂存有过氧化钠时,一旦失火,应选用________灭火(填字母序号)。
探究一:脱脂棉燃烧的原因。
[作出猜想]
(1)根据燃烧条件分析:
①脱脂棉是可燃物;
②吹出的气体可能与过氧化钠反应生成了氧气;
③反应放出热量,满足了温度达到脱脂棉的
[进行实验]
(2)在如图所示装置中,向过氧化钠粉末中不断吹气,观察到过氧化钠粉末由淡黄色逐渐变为白色,在导管口P处放置
探究二:试管内残留白色固体的成分。
[查阅资料]①吹出的气体主要成分有氮气、二氧化碳和水蒸气;② 过氧化钠与氮气不反应。
[作出猜想]
(3)猜想1:CO2参加反应,固体成分是Na2CO3;
猜想2:H2O参加反应,固体成分是NaOH;
猜想3:CO2和H2O均参加反应,固体成分是
[实验验证]
(4)实验过程如下:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取残留白色固体于试管中配成溶液, 向其中加入足量的氯化钡溶液,静置 | 产生白色沉淀 | 固体成分含有碳酸钠 |
| ②取适量①的上层清液于试管中,向其 中滴加少量氯化铜溶液 | 产生蓝色沉淀 | 固体成分含有 |
[实验结论]
(5)过氧化钠与二氧化碳、水蒸气都能反应,猜想3正确。请写出过氧化钠与二氧化碳反应的化学方程式:
[拓展延伸]
(6)化工厂存有过氧化钠时,一旦失火,应选用________灭火(填字母序号)。
| A.二氧化碳灭火器 | B.细沙 | C.水基型灭火器 |
您最近一年使用:0次
2 . 质量守恒定律是化学学习中的一条重要规律。
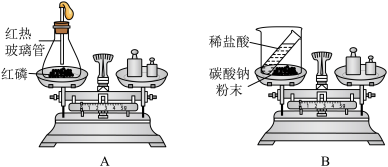
(一)如图是某化学兴趣小组同学探究质量守恒定律时设计的实验,请你跟他们一起探究:
(1)用装置B进行实验时,观察到反应后天平不平衡,天平指针向_______ (填“左”或“右”)偏转。该反应_______ (填“遵守”或“不遵守”)质量守恒定律。
(2)通过对以上两个实验的分析,你认为用有气体参加或生成的化学反应来验证质量守恒定律时,需要在_______ 的容器中进行。
(二)熔喷布是制造口罩的核心材料,纤维直径可以达到1~5微米。某化学兴趣小组为了探究熔喷布的组成元素,设计了如下实验,请你参与并回答相关问题:
【提出问题】熔喷布是由什么元素组成的?
【查阅资料】
①无水硫酸铜(CuSO4)是白色固体,遇水会变为蓝色固体;
②熔喷布易燃,只可能由碳、氢、氧元素中的一种或多种组成。
【进行实验】连接如图所示装置,检查装置的气密性,将α克某熔喷布样品碎片装入玻璃管中,先通入一段时间氧气,再点燃酒精灯。一段时间后,样品完全且充分燃烧,无残留物质。熄灭酒精灯,再持续通一会儿氧气。冷却,称量。计算得出:装置B共增重b克,装置C增重c克。(假设熔喷布样品燃烧生成的物质被B和C完全吸收)

(3)实验开始前将熔喷布样品剪成碎屑的目的是_______ 。
(4)装置B中观察到_______ ,证明生成了水,装置C中的澄清石灰水变浑浊,证明生成了二氧化碳。尾气中检测不到一氧化碳,说明样品充分燃烧。
【得出结论】
(5)由上述实验可知,熔喷布中一定含有的元素是_______ 。若_______ (用含a、b、c的关系式表示),说明该熔喷布不含氧元素。

(一)如图是某化学兴趣小组同学探究质量守恒定律时设计的实验,请你跟他们一起探究:
(1)用装置B进行实验时,观察到反应后天平不平衡,天平指针向
(2)通过对以上两个实验的分析,你认为用有气体参加或生成的化学反应来验证质量守恒定律时,需要在
(二)熔喷布是制造口罩的核心材料,纤维直径可以达到1~5微米。某化学兴趣小组为了探究熔喷布的组成元素,设计了如下实验,请你参与并回答相关问题:
【提出问题】熔喷布是由什么元素组成的?
【查阅资料】
①无水硫酸铜(CuSO4)是白色固体,遇水会变为蓝色固体;
②熔喷布易燃,只可能由碳、氢、氧元素中的一种或多种组成。
【进行实验】连接如图所示装置,检查装置的气密性,将α克某熔喷布样品碎片装入玻璃管中,先通入一段时间氧气,再点燃酒精灯。一段时间后,样品完全且充分燃烧,无残留物质。熄灭酒精灯,再持续通一会儿氧气。冷却,称量。计算得出:装置B共增重b克,装置C增重c克。(假设熔喷布样品燃烧生成的物质被B和C完全吸收)

(3)实验开始前将熔喷布样品剪成碎屑的目的是
(4)装置B中观察到
【得出结论】
(5)由上述实验可知,熔喷布中一定含有的元素是
您最近一年使用:0次
解题方法
3 . 化学规律建立在实验基础之上,质量守恒定律可以用许多化学实验加以验证。
(1)小东同学按照课本上的实验进行验证(如图所示)。一段时间后,可以观察到铁钉表面出现______ ,其反应的化学方程式为______ ,反应前后天平读数不变,但溶液颜色变化不明显。

(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想。
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
【实验分析】从以上现象分析,两个设想都不合适,其中按设想______ (填“一”或“二”)进行的实验能够验证质量守恒定律。
实验1中溶液颜色几乎不变的原因可能是______ (填序号)。
A.铁与饱和硫酸铜溶液不反应
B.铁表面形成了一层氧化膜,阻止了反应的进一步进行
C.生成的铜快速沉积在铁表面,阻止了反应的进一步进行
D.水也参与了该反应,但饱和硫酸铜溶液中水太少
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水,将实验2中的烧杯换成如图所示装置,均能达到实验目的,但该装置中缺少一种物品,请你在装置图中画出______ 。

(1)小东同学按照课本上的实验进行验证(如图所示)。一段时间后,可以观察到铁钉表面出现

(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想。
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
| 实验内容 | 实验现象 | |
| 实验1 | 烧杯中换成饱和硫酸铜溶液 | ①1小时后溶液颜色几乎不变 ②天平读数不变 ③铁钉表面有变化 |
| 实验2 | 铁钉换成锌粒 | ①溶液颜色明显变浅 ②天平读数变小 ③锌粒表面有变化 |
实验1中溶液颜色几乎不变的原因可能是
A.铁与饱和硫酸铜溶液不反应
B.铁表面形成了一层氧化膜,阻止了反应的进一步进行
C.生成的铜快速沉积在铁表面,阻止了反应的进一步进行
D.水也参与了该反应,但饱和硫酸铜溶液中水太少
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水,将实验2中的烧杯换成如图所示装置,均能达到实验目的,但该装置中缺少一种物品,请你在装置图中画出

您最近一年使用:0次
4 . 化学规律建立在实验基础之上,质量守恒定律可以用许多化学实验加以验证。
(1)小东同学按照如图所示实验进行验证。一段时间后,可以观察到铁钉表面出现_____ (填现象),其反应的化学方程式为_____ ,反应前后天平读数不变,但溶液颜色变化不明显。

(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想:
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
【实验分析】
实验1中溶液颜色几乎不变的原因可能是_____ (填序号)。
A 铁与饱和硫酸铜溶液不反应
B 实验中铁严重生锈,表面形成了一层氧化膜,阻止了反应的进一步进行
C 生成的铜快速沉积在铁表面,阻止了反应的进一步进行
D 水与铁发生反应,但饱和硫酸铜溶液中水太少
实验2虽然很快观察到溶液颜色变化,但出现了反应后总质量减小的情况,老师提醒小东,硫酸
铜溶液中含有少量的硫酸,所以总质量减小的原因可能是_____ 。
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水;将实验2中的烧杯换成如图所示装置,均能达到实验目的,但该装置还需的改进方法是_____ 。

(1)小东同学按照如图所示实验进行验证。一段时间后,可以观察到铁钉表面出现

(2)小东想既能验证质量守恒定律,又能更快地观察到溶液颜色的变化,提出了以下设想:
【提出设想】设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
【实验验证】小东将以上实验进行了如下改进:
| 实验内容 | 实验现象 | |
| 实验1 | 烧杯中换成饱和硫酸铜溶液 | ① 1小时后溶液颜色几乎不变 ②天平读数不变 ③铁钉表面有变化 |
| 实验2 | 铁钉换成锌粒 | ①溶液颜色明显变浅 ②天平读数减小 ③锌粒表面有变化 |
实验1中溶液颜色几乎不变的原因可能是
A 铁与饱和硫酸铜溶液不反应
B 实验中铁严重生锈,表面形成了一层氧化膜,阻止了反应的进一步进行
C 生成的铜快速沉积在铁表面,阻止了反应的进一步进行
D 水与铁发生反应,但饱和硫酸铜溶液中水太少
实验2虽然很快观察到溶液颜色变化,但出现了反应后总质量减小的情况,老师提醒小东,硫酸
铜溶液中含有少量的硫酸,所以总质量减小的原因可能是
(3)小东通过反复实验和探究得出:向实验1的饱和硫酸铜溶液中加入等体积的水;将实验2中的烧杯换成如图所示装置,均能达到实验目的,但该装置还需的改进方法是

您最近一年使用:0次



