解题方法
1 . 氢气的开发利用是氢能研究的热点。
一、氢气的发现和制备
(1)1766年,英国科学家卡文迪许用铁与稀盐酸作用,制得了可燃性的H2,同时还得到了浅绿色的氯化亚铁溶液,写出该反应的符号表达式___________ 。
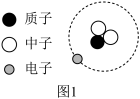
(2)目前制氢的方法主要有电解水制氢。电解水制氢中,使用氚进行核能发电,图1能表示氚的原子结构,氚属于___________ 元素的一种原子,氚原子的相对原子质量约为___________ 。
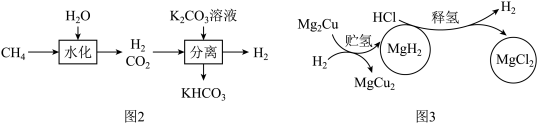
(3)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如图2:
①“分离”时K2CO3溶液吸收CO2生成KHCO3,反应的符号表达式为___________ 。
②甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48:5,则X的化学式为___________ 。
二、氢气的贮存和释放
Mg2Cu可用于化学储氢,其贮氢与释氢过程如图3所示。
(4)贮氢反应需要在高温和隔绝空气的条件下进行,隔绝空气的原因___________ 。
(5)释氢释放的H2比贮氢吸收的H2___________ (选填“多”或“少”)
(6)释放出的氢气可用作氢燃料电池,氢燃料电池工作时将___________ 能转化为电能。
(7)2022年北京冬奥会火炬“飞扬”以氢气为燃料,氢气燃烧的符号表达式为___________ 。
三、氢气在工业生产中的应用
合成氨工艺需要用到氢气,在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨气。
(8)N2是合成氨的重要原料。工业上可从空气中获得N2,利用空气中各成分的___________ 不同将空气成分进行分离。
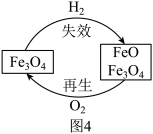
(9)Fe3O4是铁触媒的主要成分。合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图4所示。“再生”过程中铁元素的质量分数___________ (选填“变大”、“不变”或“变小”)。
(10)图5是Fe3O4在失效和再生过程中的质量与时间变化的关系图。

T1~T3时刻,是Fe3O4失效过程,T4~T5时刻,是固体再生过程。
则:A点处,固体中铁元素的质量=___________ g。
B点处,固体中含Fe3O4的质量为46.4g,则M=___________ g。
C点处,Fe3O4和FeO的质量比为___________ 。
一、氢气的发现和制备
(1)1766年,英国科学家卡文迪许用铁与稀盐酸作用,制得了可燃性的H2,同时还得到了浅绿色的氯化亚铁溶液,写出该反应的符号表达式
(2)目前制氢的方法主要有电解水制氢。电解水制氢中,使用氚进行核能发电,图1能表示氚的原子结构,氚属于

(3)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如图2:

①“分离”时K2CO3溶液吸收CO2生成KHCO3,反应的符号表达式为
②甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48:5,则X的化学式为
二、氢气的贮存和释放
Mg2Cu可用于化学储氢,其贮氢与释氢过程如图3所示。
(4)贮氢反应需要在高温和隔绝空气的条件下进行,隔绝空气的原因
(5)释氢释放的H2比贮氢吸收的H2
(6)释放出的氢气可用作氢燃料电池,氢燃料电池工作时将
(7)2022年北京冬奥会火炬“飞扬”以氢气为燃料,氢气燃烧的符号表达式为
三、氢气在工业生产中的应用
合成氨工艺需要用到氢气,在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨气。
(8)N2是合成氨的重要原料。工业上可从空气中获得N2,利用空气中各成分的

(9)Fe3O4是铁触媒的主要成分。合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图4所示。“再生”过程中铁元素的质量分数
(10)图5是Fe3O4在失效和再生过程中的质量与时间变化的关系图。

T1~T3时刻,是Fe3O4失效过程,T4~T5时刻,是固体再生过程。
则:A点处,固体中铁元素的质量=
B点处,固体中含Fe3O4的质量为46.4g,则M=
C点处,Fe3O4和FeO的质量比为
您最近半年使用:0次
名校
2 . A、B、C、D、E、F、G、H 是初中化学常见的物质。其中 A、B、C、D、E 均是由一种元素组成,H 和 G 均由三种元素组成,E 的分子中含有 16 个电子,F 的分子中含有 18 个电子,A 和 F 常温下是液体。它们 之间存在如下图所示的关系(“→”表示一种物质可以通过一个化学反应生成另一种物质,“一”表示相邻两物质可以发生反应,部分反应物和生成物省略)。

(1)E 的化学符号是______ ;
(2)根据以上物质关系,下列说法正确的有______ (填序号)。
①G 可能是白色固体
②B 若在空气中能燃烧,则 B 可能是铁、碳或红磷
③F 一定不是水
④工业上只能通过化学变化得到较为纯净的 E
⑤A 一定是非金属

(1)E 的化学符号是
(2)根据以上物质关系,下列说法正确的有
①G 可能是白色固体
②B 若在空气中能燃烧,则 B 可能是铁、碳或红磷
③F 一定不是水
④工业上只能通过化学变化得到较为纯净的 E
⑤A 一定是非金属
您最近半年使用:0次
2012·辽宁鞍山·中考模拟
解题方法
3 . 比较与分析归纳会使你变得更聪明。请分析下表中信息,回答有关问题:
⑴上述表中X=
⑵ ① 试归纳氟、氯、溴、碘的原子结构规律(答一点即可):
;
② 试归纳氟、氯、溴、碘对应单质的性质变化规律(答一点即可):
;
⑶已知:Cl2和Br2的化学性质相似,Cl2+H2O=HCl+HClO,其中HClO也是一种酸,它与氢氧化钠溶液反应的反应方程式为:HClO+NaOH=NaClO+H2O,试分别写出Br2与水,Br2与NaOH溶液反应的化学方程式:
;
。
| 名称 | 符号 | 原子结构示意图 | 单质的 化学式 | 常温常压下 状态 | 单质与氢气反应 |
| 氟 | F | 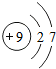 | F2 | 气态 | 黑暗处爆炸 |
| 氯 | Cl | 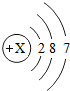 | Cl2 | 气态 | 光照爆炸 |
| 溴 | Br | 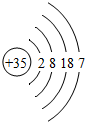 | Br2 | 液态 | 加热反应 |
| 碘 | I | 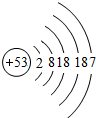 | I2 | 固态 | 持续加热缓慢反应 |
⑵ ① 试归纳氟、氯、溴、碘的原子结构规律(答一点即可):
;
② 试归纳氟、氯、溴、碘对应单质的性质变化规律(答一点即可):
;
⑶已知:Cl2和Br2的化学性质相似,Cl2+H2O=HCl+HClO,其中HClO也是一种酸,它与氢氧化钠溶液反应的反应方程式为:HClO+NaOH=NaClO+H2O,试分别写出Br2与水,Br2与NaOH溶液反应的化学方程式:
;
。
您最近半年使用:0次



