解题方法
1 . 下列实验操作能达到实验目的的是
| 实验目的 | 实验操作 | |
| A | 鉴别NaCl溶液和稀硫酸 | 滴加酚酞溶液 |
| B | 除去CO2中混有的水蒸气 | 将混合气通过NaOH固体 |
| C | 除去O2中混有的水蒸气 | 将混合气通过浓硫酸 |
| D | 检验贝壳中是否含有碳酸盐 | 加适量的稀盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列实验,不能 达到实验目的的是
A.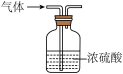 干燥氧气 干燥氧气 | B.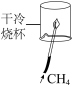 验证甲烷中含有氢元素 验证甲烷中含有氢元素 |
C.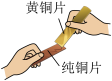 比较黄铜和纯铜的硬度 比较黄铜和纯铜的硬度 | D. 验证质量守恒定律 验证质量守恒定律 |
您最近一年使用:0次
解题方法
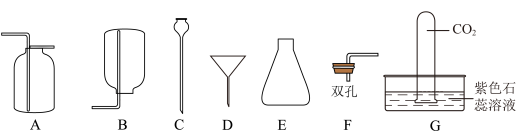
3 . 如图是实验室常用的仪器、装置,请按要求回答下列问题。___________ 。
(2)上述仪器中,制备并收集 时需选用的是
时需选用的是___________ (填字母,从A∼F中选择),实验室用过氧化氢制氧气的化学方程式为___________ 。
(3)下列干燥剂中,可用于干燥 的是___________(填字母)。
的是___________(填字母)。
(4)用G装置探究二氧化碳的性质,观察到的现象是___________ 。
(2)上述仪器中,制备并收集
 时需选用的是
时需选用的是(3)下列干燥剂中,可用于干燥
 的是___________(填字母)。
的是___________(填字母)。| A.碱石灰(氢氧化钠和氧化钙混合物) | B.浓硫酸 | C.氢氧化钠固体 |
(4)用G装置探究二氧化碳的性质,观察到的现象是
您最近一年使用:0次
7日内更新
|
12次组卷
|
3卷引用:2024年陕西省渭南市大荔县初中学业水平考试化学模拟试题
解题方法
4 . 化学探究不仅激发同学们学习化学的兴趣也能提高学习能力,有助于开发同学们的智慧潜力。某化学兴趣小组在老师的指导下,对水蒸气通过灼热的焦炭后得到的混合气体进行了实验探究。
【提出问题】水蒸气通过灼热的焦炭后得到的混合气体含有哪些成分?
【猜想与假设】
猜想一:含有一氧化碳、氢气和水蒸气。
猜想二:含有一氧化碳、二氧化碳、氢气和水蒸气。
猜想三:含有二氧化碳、氢气和水蒸气。
【查阅资料】
①无水硫酸铜遇水由白色变为蓝色。
②碱石灰是固体氢氧化钠和氧化钙的混合物。
③氢气与一氧化碳都具有还原性。
【收集证据】同学们在老师的指导下设计了如图1所示装置(部分夹持仪器已略去),并进行了实验。_______ 。
(2)装置C中的药品为氢氧化钠溶液,其目的为除去二氧化碳气体,防止干扰后面的实验。装置D中应放_______ ,除去混合气体中的水蒸气
(3)反应后装置E玻璃管中_______ 粉末变为黑色,F中无水硫酸铜由白色变为蓝色,G中澄清石灰水变浑浊,说明混合气体中还存在的气体是_______ 。
(4)装置H的作用是_______ 。
【实验结论】
(5)猜想_______ 正确。
【实验反思】
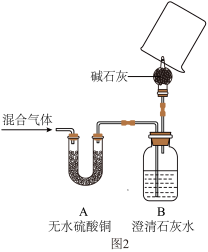
(6)经过讨论,同学们将如图1装置进行了简化。只用如图2所示装置并自选必要试剂就能完成探究(假设每步都完全反应)。实验过程中点燃玻璃尖嘴导出的气体,干燥的凉烧杯内壁能观察到的现象是_______ ,应补充的最后一步实验操作及现象是_______ 。
【提出问题】水蒸气通过灼热的焦炭后得到的混合气体含有哪些成分?
【猜想与假设】
猜想一:含有一氧化碳、氢气和水蒸气。
猜想二:含有一氧化碳、二氧化碳、氢气和水蒸气。
猜想三:含有二氧化碳、氢气和水蒸气。
【查阅资料】
①无水硫酸铜遇水由白色变为蓝色。
②碱石灰是固体氢氧化钠和氧化钙的混合物。
③氢气与一氧化碳都具有还原性。
【收集证据】同学们在老师的指导下设计了如图1所示装置(部分夹持仪器已略去),并进行了实验。
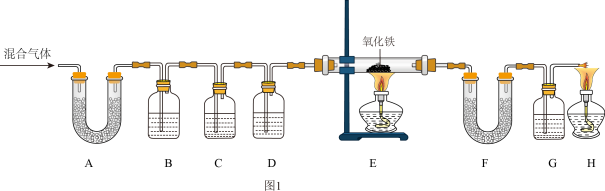
(2)装置C中的药品为氢氧化钠溶液,其目的为除去二氧化碳气体,防止干扰后面的实验。装置D中应放
(3)反应后装置E玻璃管中
(4)装置H的作用是
【实验结论】
(5)猜想
【实验反思】
(6)经过讨论,同学们将如图1装置进行了简化。只用如图2所示装置并自选必要试剂就能完成探究(假设每步都完全反应)。实验过程中点燃玻璃尖嘴导出的气体,干燥的凉烧杯内壁能观察到的现象是
您最近一年使用:0次
5 . 纳米零价铁在环保领域应用广泛。
I.制备纳米铁粉
(1)已知氢气与菱铁矿(主要成分为 )在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式
)在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式_____ 。
Ⅱ.探究所得固体成分
【提出问题】氢气与碳酸亚铁反应后剩余固体的成分是什么?
【做出猜想】
(2)猜想一: 猜想二:
猜想二: 猜想三:
猜想三:_____ 。
【查阅资料】
①氢气具有还原性,能够冶炼金属。
②无水硫酸铜是一种白色固体,遇水会变为蓝色。
【实验探究】某学习小组利用如图1所示装置,对剩余固体成分(杂质不与稀硫酸反应)进行探究,实验操作及现象如下。回答下列问题。_____ 。
(4)向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,甲同学判断猜想一正确,乙同学认为甲的判断不合理,理由是_____ 。
(5)观察到装置B中澄清石灰水变浑浊,D中_____ (填实验现象),E中固体变蓝。
【实验结论】综上所述,猜想三正确。
【反思交流】
(6)若去掉装置E_____ (填“能”或“不能”)证明固体中含有 。
。
Ⅱ.处理水体中的氮、磷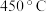 或者
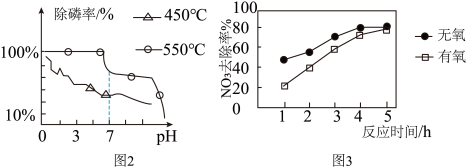
或者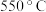 热处理纳米铁粉的除磷率以及
热处理纳米铁粉的除磷率以及 如图2所示。分析:温度为
如图2所示。分析:温度为_____ 时、_____ (填酸性或碱性)条件下处理效果更好。
(8)纳米铁粉能处理水体中的硝态氮。
在酸性条件下,纳米铁粉与 反应生成
反应生成 、
、 和水,该化学反应的化学方程式为
和水,该化学反应的化学方程式为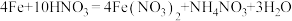 ,反应中化合价改变的元素有
,反应中化合价改变的元素有_____ 。
I.制备纳米铁粉
(1)已知氢气与菱铁矿(主要成分为
 )在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式
)在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式Ⅱ.探究所得固体成分
【提出问题】氢气与碳酸亚铁反应后剩余固体的成分是什么?
【做出猜想】
(2)猜想一:
 猜想二:
猜想二: 猜想三:
猜想三:【查阅资料】
①氢气具有还原性,能够冶炼金属。
②无水硫酸铜是一种白色固体,遇水会变为蓝色。
【实验探究】某学习小组利用如图1所示装置,对剩余固体成分(杂质不与稀硫酸反应)进行探究,实验操作及现象如下。回答下列问题。
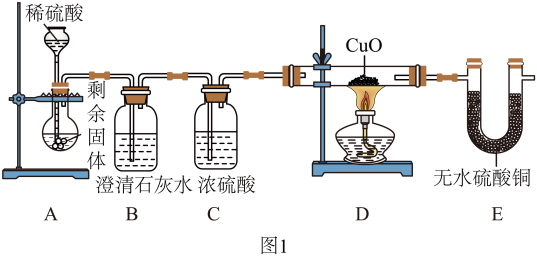
(4)向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,甲同学判断猜想一正确,乙同学认为甲的判断不合理,理由是
(5)观察到装置B中澄清石灰水变浑浊,D中
【实验结论】综上所述,猜想三正确。
【反思交流】
(6)若去掉装置E
 。
。Ⅱ.处理水体中的氮、磷
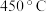 或者
或者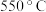 热处理纳米铁粉的除磷率以及
热处理纳米铁粉的除磷率以及 如图2所示。分析:温度为
如图2所示。分析:温度为(8)纳米铁粉能处理水体中的硝态氮。
在酸性条件下,纳米铁粉与
 反应生成
反应生成 、
、 和水,该化学反应的化学方程式为
和水,该化学反应的化学方程式为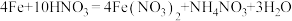 ,反应中化合价改变的元素有
,反应中化合价改变的元素有
您最近一年使用:0次
解题方法
6 . 下列实验方案的设计,合理的是
| A.验证质量守恒定律:比较Ag和CuSO4溶液混合前后的质量关系 |
| B.分离BaCl2和NaCl的混合溶液:加入Na2SO4溶液,过滤,向沉淀中加入稀盐酸 |
| C.除去N2中的O2和水蒸气:将混合气体依次通过浓硫酸和灼热的碳网 |
| D.证明NaOH与稀盐酸能反应:在稀盐酸中加入硫酸铜溶液,再逐滴加入过量的 NaOH溶液 |
您最近一年使用:0次
7 . 实验探究活动:重庆实验外国语学校化学社团学生对CaH2的制备和性质进行探究。
【阅读资料】①用H2与钙加热制得CaH2。
②钙遇水立即发生剧烈反应生成一种碱和一种气体。
③CaH2要密封保存,遇水反应也生成一种碱和一种气体。
【CaH2的制备】设计的制取装置如图所示。_______ 。
(2)制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入紫色石蕊试液后显蓝色,该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是_______ 。
【CaH2的性质探究】
(3)取少量上述装置C中的CaH2样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙,请写出反应时生成碳酸钙的化学方程式_______ 。
(4)社团学生继续对滤液中溶质成分进行探究,对滤液中溶质的成分做出如下猜测:
猜想一:NaOH
猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3
猜想四:NaOH、Ca(OH)2、Na2CO3
经讨论,大家一致认为猜想四不合理,为了进一步验证猜想三,小实同学提出往滤液中滴加少量稀盐酸,若无气泡产生,则猜想三不合理,小外认为该方案不严谨,请用化学方程式解释:_______ 。
【定量分析】
(5)取制得的CaH2样品1g(杂质为未反应完的Ca)加入到足量的溶液Na2CO3中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2g,则该CaH2样品中钙元素的质量分数为_______ 。
【阅读资料】①用H2与钙加热制得CaH2。
②钙遇水立即发生剧烈反应生成一种碱和一种气体。
③CaH2要密封保存,遇水反应也生成一种碱和一种气体。
【CaH2的制备】设计的制取装置如图所示。

(2)制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入紫色石蕊试液后显蓝色,该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是
【CaH2的性质探究】
(3)取少量上述装置C中的CaH2样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙,请写出反应时生成碳酸钙的化学方程式
(4)社团学生继续对滤液中溶质成分进行探究,对滤液中溶质的成分做出如下猜测:
猜想一:NaOH
猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3
猜想四:NaOH、Ca(OH)2、Na2CO3
经讨论,大家一致认为猜想四不合理,为了进一步验证猜想三,小实同学提出往滤液中滴加少量稀盐酸,若无气泡产生,则猜想三不合理,小外认为该方案不严谨,请用化学方程式解释:
【定量分析】
(5)取制得的CaH2样品1g(杂质为未反应完的Ca)加入到足量的溶液Na2CO3中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2g,则该CaH2样品中钙元素的质量分数为
您最近一年使用:0次
解题方法
8 . 化学是一门以实验为基础的科学
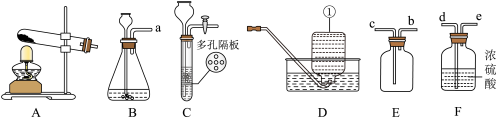
(Ⅰ)气体的制取和性质是初中化学知识的核心之一。请结合下列实验装置回答下列问题。__________ 。
(2)若用过氧化氢溶液制取氧气,反应的化学方程式是__________ ;过氧化氢溶液不适合选C装置的原因:__________ ,制氧气若用高锰酸钾制取并收集较纯净的氧气,应选用的装置是__________ 。
(3)若要制取二氧化碳,在B装置中装有石灰石,从长颈漏斗中应加入__________ (填药品名称)。如果要获得干燥的二氧化碳,还需要用到E、F装置,正确的连接方法是(用导管口代号b、c、d、e表示)a、__________ 。
(4)如图所示,向集满 的试管内倒入约占试管容积三分之一的澄清石灰水,旋紧胶塞,上、下持续振荡一定时间。充分振荡后,试管内压强
的试管内倒入约占试管容积三分之一的澄清石灰水,旋紧胶塞,上、下持续振荡一定时间。充分振荡后,试管内压强__________ 试管外大气压强(选填“>”或“=”或“<”)。__________ (填“高”或“低”)。
(6)图2是探究物质溶解能力差异的实验,高锰酸钾__________ (填“难”或“易”)溶于汽油。
(7)图3是探究质量守恒定律,反应后天平不平衡的原因是__________ 。
(Ⅰ)气体的制取和性质是初中化学知识的核心之一。请结合下列实验装置回答下列问题。
(2)若用过氧化氢溶液制取氧气,反应的化学方程式是
(3)若要制取二氧化碳,在B装置中装有石灰石,从长颈漏斗中应加入
(4)如图所示,向集满
 的试管内倒入约占试管容积三分之一的澄清石灰水,旋紧胶塞,上、下持续振荡一定时间。充分振荡后,试管内压强
的试管内倒入约占试管容积三分之一的澄清石灰水,旋紧胶塞,上、下持续振荡一定时间。充分振荡后,试管内压强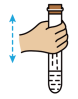
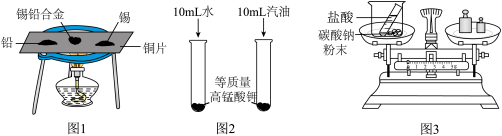
(6)图2是探究物质溶解能力差异的实验,高锰酸钾
(7)图3是探究质量守恒定律,反应后天平不平衡的原因是
您最近一年使用:0次
7日内更新
|
25次组卷
|
2卷引用:2024年江苏省盐城市鹿鸣路初级中学中考三模化学试卷
解题方法
9 . 下列实验方案中,能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 除去氨气中的水蒸气 | 将气体通过足量的浓硫酸 |
| B | 检验酒精中是否含有氧元素 | 点燃,观察是否有水生成 |
| C | 除去MnO2中的KCl | 加入足量的水溶解,过滤、洗涤、干燥 |
| D | 除去氯化钾中的氯酸钾 | 加入适量二氧化锰后,加热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 金属铜在空气中久置会形成一层绿色的“铜锈”,其主要成分是碱式碳酸铜[化学式: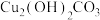 ],已知碱式碳酸铜受热会分解生成三种氧化物,小明设计了以铜锈为原料采用不同途径制备金属铜的转化流程如图(部分反应物、生成物、反应条件已略去),其中B、F为气体。
],已知碱式碳酸铜受热会分解生成三种氧化物,小明设计了以铜锈为原料采用不同途径制备金属铜的转化流程如图(部分反应物、生成物、反应条件已略去),其中B、F为气体。______ 。
(2)若G的浓溶液可做干燥剂,写出④反应的化学方程式________________ 。
(3)该转化关系中属于置换反应的是______ 。(填序号)
(4)F物质的一种用途是______ 。
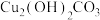 ],已知碱式碳酸铜受热会分解生成三种氧化物,小明设计了以铜锈为原料采用不同途径制备金属铜的转化流程如图(部分反应物、生成物、反应条件已略去),其中B、F为气体。
],已知碱式碳酸铜受热会分解生成三种氧化物,小明设计了以铜锈为原料采用不同途径制备金属铜的转化流程如图(部分反应物、生成物、反应条件已略去),其中B、F为气体。
(2)若G的浓溶液可做干燥剂,写出④反应的化学方程式
(3)该转化关系中属于置换反应的是
(4)F物质的一种用途是
您最近一年使用:0次



