解题方法
1 . 将打磨后的镁条放入盛有50 mL热水(pH约为6.4)的烧杯中,用pH传感器和浊度传感器监测溶液的pH和浊度(浊度是指溶液对光线通过时所产生的阻碍程度。通常浊度越高,溶液越浑浊)随时间的变化如图。下列有关描述正确的是

A.该实验中反应的化学方程式为Mg+H2O Mg(OH)2+H2↑ Mg(OH)2+H2↑ |
| B.实线表示溶液浊度随时间的变化 |
| C.50s时向溶液中滴入石蕊试液,溶液变红 |
| D.150s后溶液浊度下降是因为生成的Mg(OH)2沉降了 |
您最近一年使用:0次
解题方法
2 . 规范的操作是实验安全和成功的重要保证。下列实验操作中正确的是
A.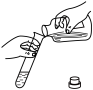 液体的倾倒 液体的倾倒 | B.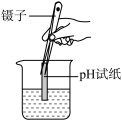 测溶液的 测溶液的 |
C.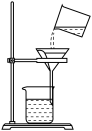 过滤 过滤 | D.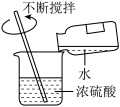 稀释浓硫酸 稀释浓硫酸 |
您最近一年使用:0次
3 . 下列图像能正确反映对应变化关系的是
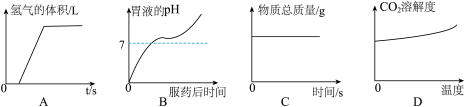
| A.向未经打磨的铝片中滴加一定量的稀盐酸 |
B.按医嘱服用胃舒平【主要成分 (不溶于水)】治疗胃酸过多症 (不溶于水)】治疗胃酸过多症 |
| C.密闭容器中点燃红磷 |
| D.从冰箱里拿出汽水 |
您最近一年使用:0次
解题方法
4 . 身边的一些物质 如下,下列说法
如下,下列说法错误 的是
 如下,下列说法
如下,下列说法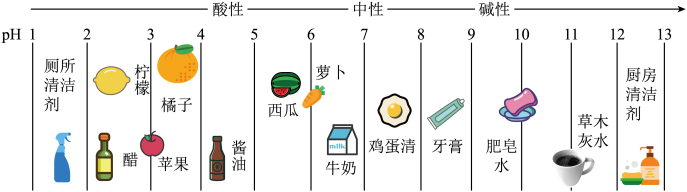
| A.胃酸过多的人可以多饮用柠檬水 | B.牙膏呈碱性 |
| C.向厨房清洁剂滴入酚酞,溶液变红 | D.西瓜呈酸性 |
您最近一年使用:0次
解题方法
5 . 进行正确的实验操作是解决实验问题的关键。下列实验操作正确的是
A. 称量氯化钠固体 称量氯化钠固体 | B. 测溶液的pH 测溶液的pH |
C. 加热固体 加热固体 | D. 稀释浓硫酸 稀释浓硫酸 |
您最近一年使用:0次
名校
解题方法
6 . 规范的实验操作是实验成功的保证。以下化学实验操作中正确的是
A.测定溶液的酸碱度 |
B.配制氢氧化钠溶液 |
C.验证质量守恒定律 |
D.加热液体 |
您最近一年使用:0次
7 . 下图是某同学设计的有关盐的化学性质的创新实验装置。 ,打开
,打开 加入稀盐酸,观察到的现象是
加入稀盐酸,观察到的现象是________ ;甲中发生反应的化学方程式为________ 。
(2)随后关闭 ,打开
,打开 ,观察到的现象为
,观察到的现象为________ 。
(3)探究实验结束后,同学们又分别做了三组实验,以下三组实验中,能检验乙中加入稀盐酸是否过量的是________(填字母)。

 ,打开
,打开 加入稀盐酸,观察到的现象是
加入稀盐酸,观察到的现象是(2)随后关闭
 ,打开
,打开 ,观察到的现象为
,观察到的现象为(3)探究实验结束后,同学们又分别做了三组实验,以下三组实验中,能检验乙中加入稀盐酸是否过量的是________(填字母)。
A.取少量乙中溶液,测量 |
| B.取少量乙中溶液,向其中加入镁粉,观察现象 |
| C.取少量乙中溶液,向其中加入硝酸银溶液,观察现象 |
您最近一年使用:0次
8 . 纯碱是一种重要的化工原料,广泛用于玻璃、造纸、纺织和洗涤剂的生产。某化学兴趣小组对纯碱的制备、性质及用途开展了一系列探究活动。
【活动一】了解纯碱的制备 —— “侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收氨气和二氧化碳,生成碳酸氢钠和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱。
(1)纯碱属于_____________ (填“酸”“碱”或“盐”) 。请写出“侯氏制碱法”反应原理中第一步反应的化学方程式________________________ 。
【活动二】探究纯碱的性质 —— Na2CO3溶液呈碱性
查阅资料:① 溶液呈碱性是因为存在较多的 OH⁻。
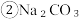 在水中全部解离出Na+和
在水中全部解离出Na+和  ; K2CO3与 Na2CO3化学性质相似。
; K2CO3与 Na2CO3化学性质相似。
③ CaCl2溶液呈中性, Ca2+、Cl-对溶液的酸碱性没有影响。
提出猜想:
(2)猜想一:H2O单独起作用,产生较多的OH⁻,使溶液呈碱性。
猜想二:__________________________ ,使溶液呈碱性。
猜想三: 与H2O 作用,产生较多的OH-,使溶液呈碱性。
与H2O 作用,产生较多的OH-,使溶液呈碱性。
实验探究:
(3)
解释与结论:
(4)同学们和老师交流,得知 和 H2O作用,产生较多的OH⁻和另一种阴离子。
和 H2O作用,产生较多的OH⁻和另一种阴离子。
拓展与延伸:结合活动二的所有信息和结论,运用初中化学所学知识,经过分析推理可得出:Na2CO3溶液中含有的阴离子是_____________________ 。
【活动三】探究纯碱的用途 —— 用于生产洗涤剂
查阅资料:Na2CO3可用于生产洗涤剂。
Na2CO3溶液呈碱性,可清洗油污,溶液碱性越强,去油污效果越好。
实验探究:兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。用不同温度的水,配制溶质质量分数分别为2%、6%和 10%的 溶液,并测定溶液 pH ,记录数据如下表:
溶液,并测定溶液 pH ,记录数据如下表:
解释与结论:
(5)表格中X表示的数据是__________ 。
(6)实验①、②、③对比,可得出的结论是_________________________ 。要证明Na2CO3溶液的溶质质量分数与pH变化的关系,可选择的实验的编号是__________ 。
拓展与应用:
(7)依据实验结论可知,下列物质可用于去油污的是 (填字母序号)。
【活动一】了解纯碱的制备 —— “侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收氨气和二氧化碳,生成碳酸氢钠和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱。
(1)纯碱属于
【活动二】探究纯碱的性质 —— Na2CO3溶液呈碱性
查阅资料:① 溶液呈碱性是因为存在较多的 OH⁻。
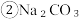 在水中全部解离出Na+和
在水中全部解离出Na+和  ; K2CO3与 Na2CO3化学性质相似。
; K2CO3与 Na2CO3化学性质相似。③ CaCl2溶液呈中性, Ca2+、Cl-对溶液的酸碱性没有影响。
提出猜想:
(2)猜想一:H2O单独起作用,产生较多的OH⁻,使溶液呈碱性。
猜想二:
猜想三:
 与H2O 作用,产生较多的OH-,使溶液呈碱性。
与H2O 作用,产生较多的OH-,使溶液呈碱性。实验探究:
(3)
| 实验操作 | 实验现象 | 实验结论 |
| 向试管中加入一定量的蒸馏水,滴入2 滴酚酞溶液。 | 溶液无明显变化 | 猜想一不成立 |
| 向试管中加入一定量的NaCl溶液, 滴入2滴酚酞溶液。 | 溶液无明显变化 | 猜想二不成立 |
| ①向试管中加入一定量的Na2CO3溶液,滴入2滴酚酞溶液。 ②往①所得溶液中逐滴加入 | ①溶液由无色变红色 ② | 猜想三 成立 |
解释与结论:
(4)同学们和老师交流,得知
 和 H2O作用,产生较多的OH⁻和另一种阴离子。
和 H2O作用,产生较多的OH⁻和另一种阴离子。拓展与延伸:结合活动二的所有信息和结论,运用初中化学所学知识,经过分析推理可得出:Na2CO3溶液中含有的阴离子是
【活动三】探究纯碱的用途 —— 用于生产洗涤剂
查阅资料:Na2CO3可用于生产洗涤剂。
Na2CO3溶液呈碱性,可清洗油污,溶液碱性越强,去油污效果越好。
实验探究:兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。用不同温度的水,配制溶质质量分数分别为2%、6%和 10%的
 溶液,并测定溶液 pH ,记录数据如下表:
溶液,并测定溶液 pH ,记录数据如下表:| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | X | 10% | 10% |
| 溶液温度/℃ | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 70 |
| 溶液 pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
(5)表格中X表示的数据是
(6)实验①、②、③对比,可得出的结论是
拓展与应用:
(7)依据实验结论可知,下列物质可用于去油污的是 (填字母序号)。
| A.NaCl | B.NaOH | C.K2CO3 | D.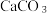 |
您最近一年使用:0次
9 . 下列图像能正确反映对应变化关系的是
A. 向一定量稀盐酸溶液中不断滴入水 向一定量稀盐酸溶液中不断滴入水 |
B. 一定质量的碳酸氢钠固体受热分解 一定质量的碳酸氢钠固体受热分解 |
C. 向等质量的Mg和Zn中,分别加入过量的稀盐酸 向等质量的Mg和Zn中,分别加入过量的稀盐酸 |
D. 电解水时生成氢气和氧气的体积比 电解水时生成氢气和氧气的体积比 |
您最近一年使用:0次
解题方法
10 . 室温时,向盛有稀硫酸的烧杯中逐滴加入 溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化)。
溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化)。__________ (填化学式)。
(2)c点烧杯内溶液的
_____ 7(填“>” “=”“<”)。
(3)d点溶液中滴加紫色石蕊溶液,溶液颜色为____________ 。
 溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化)。
溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化)。
(2)c点烧杯内溶液的

(3)d点溶液中滴加紫色石蕊溶液,溶液颜色为
您最近一年使用:0次



