名校
解题方法
1 . 向盛有碱溶液的烧杯中缓慢滴加稀硫酸,下列说法正确的是
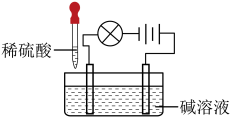
| A.实验中的酸碱中和反应一定没有放出热量 |
| B.若灯泡发光,则溶液中含有可自由移动的离子 |
| C.灯泡亮度变化只与溶液中的OH-有关 |
| D.若灯泡变化为“亮→灭→亮”,则碱溶液可能是KOH溶液 |
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案,不能达到相应实验目的的是
|
|
|
|
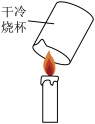
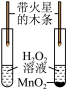
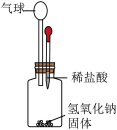
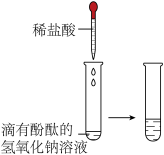
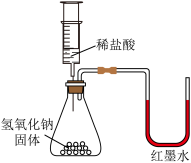
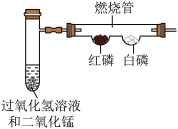
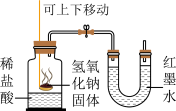
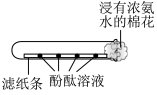
| A.验证产物有水 | B.探究 能否加快 能否加快 的分解 的分解 | C.探究氢氧化钠与盐酸反应放热 | D.探究铁锈蚀的条件 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 盐酸与氢氧化钠溶液的中和反应是学生必做的基础实验内容之一,某同学完成该实验的同时利用数字化传感器测量溶液pH的变化,测得图像如图1。______ 溶液滴加到另一种溶液中;其中a点表示的意义是______ ,b点所示溶液中,含有的溶质是______ 。
(2)图2是探究中和反应能量变化的装置,仪器c的名称是______ ,将稀盐酸加入滴有酚酞的氢氧化钠溶液中U型管中液面的变化是______ 。
(3)验证反应后溶液中稀盐酸有剩余,下列操作不可行的是______。

(2)图2是探究中和反应能量变化的装置,仪器c的名称是
(3)验证反应后溶液中稀盐酸有剩余,下列操作不可行的是______。
A.取样,滴加 溶液 溶液 | B.取样,加入锌粉 |
C.取样,加入 粉末 粉末 | D.取样,加入CuO粉末 |
您最近一年使用:0次
4 . 酸碱中和反应是初中阶段重要的一类反应,请你参与一起探究。
【实验1】从能量变化角度探究酸和碱的反应
某小组同学测量盐酸与氢氧化钠溶液反应过程中温度的变化,观察到溶液温度升高,因此,得出两者能反应的结论。有同学认为此结论不够严谨,在密闭隔热容器中设计了以下实验:
①10mL一定浓度的盐酸与10mL蒸馏水混合,测量溶液温度的变化。
②10mL一定浓度的氢氧化钠溶液与10mL蒸馏水混合,测量溶液温度的变化。
③10mL一定浓度的盐酸与10mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
用数字化实验技术测得3个实验中溶液温度随时间变化的关系如图1所示。
(1)由图1可知,盐酸、氢氧化钠溶液稀释时均______ (填“放热”或“吸热”),但它们稀释时温度的变化量远______ (填“大于”或“小于”)两溶液混合时温度的变化量,由此说明氢氧化钠和盐酸发生了反应。
(2)从微观角度分析,此中和反应的温度变化主要是由于______ (填离子符号),两种离子反应放出热量的缘故,由此说明氢氧化钠和盐酸发生了中和反应。
(3)在10mL溶质质量分数为10%的NaOH溶液(密度为1.1g/mL)中加入溶质质量分数为5%的盐酸(密度为1.0g/mL)溶液的体积为______ mL,就能使反应后溶液的pH等于7。(结果保留整数)
小组同学根据图2进行相应实验操作,利用电导率传感器分别测定A试管和B试管反应过程中溶液的电导率变化,结果如图3和图4,电导率的大小能反映离子浓度的大小。
(4)根据图3所示电导率变化,请写出对应试管中发生反应的化学方程式为______ 。基本反应类型为______ 。
(5)图4中电导率的变化______ (填“能”或“不能”)说明酸和碱发生了反应,a点所示溶液中含有的溶质是______ (填化学符号)。
【实验1】从能量变化角度探究酸和碱的反应
某小组同学测量盐酸与氢氧化钠溶液反应过程中温度的变化,观察到溶液温度升高,因此,得出两者能反应的结论。有同学认为此结论不够严谨,在密闭隔热容器中设计了以下实验:
①10mL一定浓度的盐酸与10mL蒸馏水混合,测量溶液温度的变化。
②10mL一定浓度的氢氧化钠溶液与10mL蒸馏水混合,测量溶液温度的变化。
③10mL一定浓度的盐酸与10mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
用数字化实验技术测得3个实验中溶液温度随时间变化的关系如图1所示。
(1)由图1可知,盐酸、氢氧化钠溶液稀释时均
(2)从微观角度分析,此中和反应的温度变化主要是由于
(3)在10mL溶质质量分数为10%的NaOH溶液(密度为1.1g/mL)中加入溶质质量分数为5%的盐酸(密度为1.0g/mL)溶液的体积为


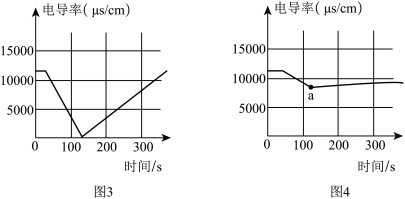
小组同学根据图2进行相应实验操作,利用电导率传感器分别测定A试管和B试管反应过程中溶液的电导率变化,结果如图3和图4,电导率的大小能反映离子浓度的大小。
(4)根据图3所示电导率变化,请写出对应试管中发生反应的化学方程式为
(5)图4中电导率的变化
您最近一年使用:0次
2024·甘肃庆阳·一模
解题方法
5 . 某化学兴趣小组的同学往氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象。
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量。
【实验设计】
(1)甲、乙两位同学分别设计了如下实验方案,请你帮他们完成实验报告。
【评价反思】
(2)你认为实验设计方案不合理的同学是__ ,理由是______________ 。
【拓展延伸】有同学提出还可利用pH的变化判断酸碱是否发生了反应,下图是小组同学利用pH传感器探究氢氧化钠溶液与稀盐酸反应的pH变化曲线。__ (填“A”、“B”或“C”)。
(4)C点所示溶液中含有的阳离子为____ (填离子符号)。
(5)该实验通过验证__________ (填“反应物消失”或“有新物质生成”)证明物质发生了反应。
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量。
【实验设计】
(1)甲、乙两位同学分别设计了如下实验方案,请你帮他们完成实验报告。
同学 | 实验操作 | 现象 | 结论 |
甲 |
| 氢氧化钠与盐酸发生了化学反应,反应的化学方程式为 | |
乙 |
| U形玻璃管中 | 氢氧化钠与盐酸发生了化学反应,且反应放热 |
【评价反思】
(2)你认为实验设计方案不合理的同学是
【拓展延伸】有同学提出还可利用pH的变化判断酸碱是否发生了反应,下图是小组同学利用pH传感器探究氢氧化钠溶液与稀盐酸反应的pH变化曲线。
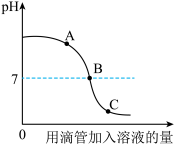
(4)C点所示溶液中含有的阳离子为
(5)该实验通过验证
您最近一年使用:0次
解题方法
6 . 某校兴趣小组同学利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,仪器A中溶液慢慢加入烧杯中溶液,用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3。已知烧杯中溶液的质量为10g,质量分数为4%。________ (填化学式)。
(2)图3中V的数值最接近_______ 。
(3)计算仪器A中溶液的溶质质量分数(写出计算过程)。

(2)图3中V的数值最接近
(3)计算仪器A中溶液的溶质质量分数(写出计算过程)。
您最近一年使用:0次
名校
解题方法
7 . 学习了酸碱盐之后,化学兴趣小组的同学开展了利用紫甘蓝制作酸碱指示剂的项目式学习。
【查阅资料】
1.紫甘蓝汁液的变色范围如表:
2.饱和Na2CO3溶液的pH=11.6
【活动一】制取试剂
利用紫甘蓝自制酸碱指示剂的步骤依次为:研碎→酒精浸泡→过滤→装瓶。
(1)提取紫甘蓝的汁液,需用酒精溶液浸泡的原因是______ 。
【活动二】应用试剂
同学们用自制的紫甘蓝汁液验证中和反应:取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,观察到溶液由无色变为黄色;再逐滴加入稀盐酸,溶液从上至下依次呈现不同的颜色,宛若彩虹,非常美丽。
【提出问题】为什么反应过程中溶液中的紫甘蓝汁液会呈现多彩的颜色呢?
【进行猜想】可能是反应过程中,溶液中各部位的酸碱度(pH)不同。
【实验探究】
(2)为验证猜想,同学们设计如下实验方案:另取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,______ 。
【得出结论】猜想正确
【交流反思】
(3)氢氧化钠溶液与稀盐酸反应的化学方程式为_______ 。
(4)除题给方案外,还可以通过测量_______ 验证氢氧化钠溶液与稀盐酸发生中和反应。
【活动三】拓展延伸
老师向滴有紫甘蓝汁液的稀盐酸和CaCl2的混合溶液中,逐滴加入饱和Na2CO3溶液,反应所得沉淀或气体的质量变化如图所示。_______ (填化学式)。
(6)加入饱和Na2CO3溶液质量由0至bg的过程中,溶液颜色的变化情况是______ 。
【查阅资料】
1.紫甘蓝汁液的变色范围如表:
| pH值 | pH<6.5 | 7.0<pH<7.1 | 7.5<pH<8.5 | 8.5<pH<12 | pH>12.5 |
| 紫甘蓝汁液 | 粉红色 | 紫色 | 蓝色 | 绿色 | 黄色 |
【活动一】制取试剂
利用紫甘蓝自制酸碱指示剂的步骤依次为:研碎→酒精浸泡→过滤→装瓶。
(1)提取紫甘蓝的汁液,需用酒精溶液浸泡的原因是
【活动二】应用试剂
同学们用自制的紫甘蓝汁液验证中和反应:取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,观察到溶液由无色变为黄色;再逐滴加入稀盐酸,溶液从上至下依次呈现不同的颜色,宛若彩虹,非常美丽。
【提出问题】为什么反应过程中溶液中的紫甘蓝汁液会呈现多彩的颜色呢?
【进行猜想】可能是反应过程中,溶液中各部位的酸碱度(pH)不同。
【实验探究】
(2)为验证猜想,同学们设计如下实验方案:另取适量氢氧化钠溶液于试管中,滴入几滴紫甘蓝汁液,
【得出结论】猜想正确
【交流反思】
(3)氢氧化钠溶液与稀盐酸反应的化学方程式为
(4)除题给方案外,还可以通过测量
【活动三】拓展延伸
老师向滴有紫甘蓝汁液的稀盐酸和CaCl2的混合溶液中,逐滴加入饱和Na2CO3溶液,反应所得沉淀或气体的质量变化如图所示。

(6)加入饱和Na2CO3溶液质量由0至bg的过程中,溶液颜色的变化情况是
您最近一年使用:0次
2024-04-13更新
|
221次组卷
|
3卷引用:2024年安徽省合肥市包河区中考一模化学试题
解题方法
8 . 下列实验方案的创新设计既实现绿色环保又能达到实验目的的是
A. 探究燃烧的条件 探究燃烧的条件 |
B. 验证质量守恒定律 验证质量守恒定律 |
C. 验证NaOH与稀盐酸反应是放热反应 验证NaOH与稀盐酸反应是放热反应 |
D.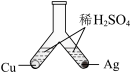 探究Cu和Ag的金属活动性强弱 探究Cu和Ag的金属活动性强弱 |
您最近一年使用:0次
9 . 下列创新小实验的说法不正确 的是
|
|
|
|
| A.均匀微热燃烧管,观察到白磷燃烧而红磷不燃烧,说明物质燃烧需要温度达到可燃物的着火点 | B.探究中和反应是否放热,观察到U型管液面左低右高 | C.探究分子在不断运动,观察到酚酞溶液从右到左依次变红 | D.探究二氧化锰的催化作用,观察到甲试管口带火星木条不复燃,乙试管口带火星木条复燃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下列基于实验事实得出的结论中正确的是
| 选项 | 实验事实 | 结论 |
| A | 向氢氧化钠固体中滴加稀硫酸,有热量放出 | 中和反应是放热反应 |
| B | 硫在氧气中燃烧较在空气中燃烧剧烈 | 氧气浓度越高,物质燃烧越剧烈 |
| C | 向某固体中滴加稀盐酸,有气泡产生 | 该固体一定含有碳酸盐 |
| D | 向氯化钡溶液中滴加某无色溶液,有白色沉淀生成 | 无色溶液的溶质一定是硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次