名校
1 . 乙醛酸是一种重要的化工中间体,可用如下图所示的电化学装置合成。图中的双极膜中间层中的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法正确的是


| A.KBr在上述电化学合成过程中只起电解质的作用 |
B.阳极上的反应式为: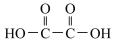   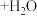 |
| C.制得1mol乙醛酸,理论上外电路中迁移了2mol电子 |
| D.双极膜中间层中的H+在外电场作用下向铅电极方向迁移 |
您最近半年使用:0次
名校
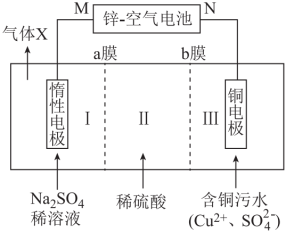
2 . 可利用碱性锌-空气电池(反应原理: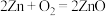 )电解处理含铜污水,回收铜单质,并制备较高浓度硫酸,电解装置如图所示。下列说法错误的是
)电解处理含铜污水,回收铜单质,并制备较高浓度硫酸,电解装置如图所示。下列说法错误的是
 )电解处理含铜污水,回收铜单质,并制备较高浓度硫酸,电解装置如图所示。下列说法错误的是
)电解处理含铜污水,回收铜单质,并制备较高浓度硫酸,电解装置如图所示。下列说法错误的是
| A.b膜是阴离子交换膜 |
B.电解装置工作一段时间后,I区溶液中 的浓度不变 的浓度不变 |
C.理论上,每生成1.6g气体X,有 从I区经a膜移向II区 从I区经a膜移向II区 |
D.N极为电源负极,电极反应式为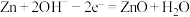 |
您最近半年使用:0次
3 . 根据光合作用的原理可设计出如图所示的原电池装置。下列说法正确的是
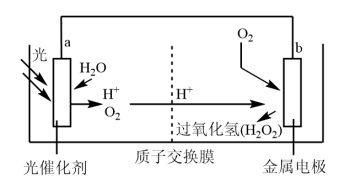

| A.a电极为原电池的正极 |
| B.电子移动方向是a→导线→b |
| C.b电极的电极反应式为O2+2H++4e-=H2O2 |
| D.a电极上每生成1molO2,通过质子交换膜的H+的物质的量为2mol |
您最近半年使用:0次
名校
4 . 科学家利用多晶铜高效催化电解 制乙烯,原理如图所示。已知:电解前后电解液浓度几乎不变。下列说法正确的是
制乙烯,原理如图所示。已知:电解前后电解液浓度几乎不变。下列说法正确的是

 制乙烯,原理如图所示。已知:电解前后电解液浓度几乎不变。下列说法正确的是
制乙烯,原理如图所示。已知:电解前后电解液浓度几乎不变。下列说法正确的是
A.铂电极为阳极,产生的气体是 和 和 |
B.铜电极的电极反应式为 |
C.通电过程中,溶液中 通过阴离子交换膜向右槽移动 通过阴离子交换膜向右槽移动 |
D.当电路中通过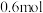 电子时,理论上能产生 电子时,理论上能产生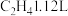 |
您最近半年使用:0次
5 . 次磷酸 是一元中强酸,工业上采用电渗析法制备,其工作原理如图所示。下列叙述错误的是
是一元中强酸,工业上采用电渗析法制备,其工作原理如图所示。下列叙述错误的是
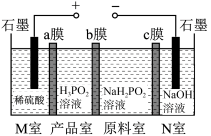
 是一元中强酸,工业上采用电渗析法制备,其工作原理如图所示。下列叙述错误的是
是一元中强酸,工业上采用电渗析法制备,其工作原理如图所示。下列叙述错误的是
A.M室发生的电极反应式为 |
B.电解过程中N室溶液的 逐渐增大 逐渐增大 |
| C.装置中a膜、b膜、c膜均为阳离子交换膜 |
| D.理论上M室和N室石墨电极上产生的气体物质的量之比为1∶2 |
您最近半年使用:0次
名校
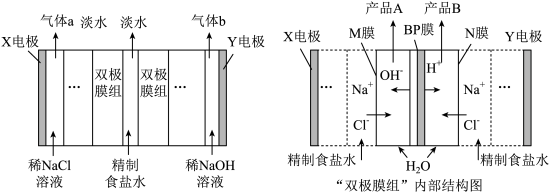
6 . 目前可采用“双极膜组”电渗析法淡化海水,同时获得副产品A和B,模拟工作原理如图所示。M和N为离子交换膜,在直流电作用下,双极阴阳膜(BP)复合层间的 解离成
解离成 和
和 ,作为
,作为 和
和 的离子源。下列说法正确的是
的离子源。下列说法正确的是
 解离成
解离成 和
和 ,作为
,作为 和
和 的离子源。下列说法正确的是
的离子源。下列说法正确的是
| A.X电极为阴极,电极反应式为2H2O+2e-=2OH-+H2↑ |
| B.M为阳离子交换膜,N为阴离子交换膜,BP膜的作用是选择性通过Cl-和Na+ |
| C.每生成5.6L气体a,理论上获得副产品A和B各0.5mol |
| D.“双极膜组”电渗析法也可应用于从盐溶液(MX)制备相应的酸(HX)和碱(MOH) |
您最近半年使用:0次
2023-04-29更新
|
1105次组卷
|
4卷引用:安徽省皖南八校2023届高三下学期第三次大联考理综化学试题
安徽省皖南八校2023届高三下学期第三次大联考理综化学试题(已下线)题型21 四室膜和双极膜电解装置及其应用(已下线)专题10 电化学及其应用-2023年高考化学真题题源解密(全国通用)湖北省部分县市区省级示范高中温德克英协作体2023-2024学年高二上学期期末综合性调研考试化学试题
解题方法
7 . 现代膜技术可使某种离子具有单向通过能力,常用于电解池、原电池中。电解NaB(OH)4溶液可制备H3BO3,其工作原理如图所示。下列说法错误的是


| A.NaB(OH)4中B的化合价为+3价 |
| B.N室发生的电极反应式为2H2O+2e-=H2↑+2OH- |
| C.去掉a膜,阳极区用稀硫酸作电解液,不影响H3BO3的纯度 |
| D.a、c膜均为阳离子交换膜,b膜为阴离子交换膜 |
您最近半年使用:0次
名校
8 . 一种新型H2O2液态燃料电池的工作原理示意图如下(a、b均为石墨电极)。下列正确的是
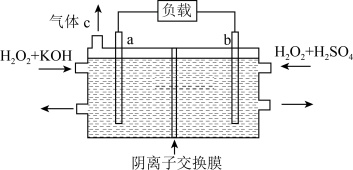

| A.电极b为正极,发生还原反应 |
| B.负极区pH增大 |
| C.正极的电极反应式为H2O2+2e-+2H+=2H2O |
D.当电路中转移0.1mol电子时,通过阴离子交换膜的 为9.6g 为9.6g |
您最近半年使用:0次
2023-04-17更新
|
345次组卷
|
2卷引用:山东省日照市莒县第一中学2022-2023学年高一下学期4月月考化学试题
9 . 一种成本低、稳定性好的全碱性多硫化物---空气液流二次电池工作时,原理如图所示。下列说法正确的是
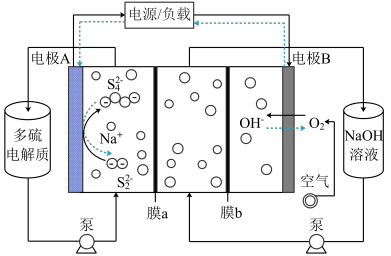

| A.连接负载时,电极A为正极 |
B.连接负载时,阳极区的电极反应式为2 - 2e- = - 2e- =  |
| C.连接电源时,电路中每通过2 NA个电子,生成NaOH的质量为80 g |
| D.膜a为阴离子交换膜,膜b为阳离子交换膜 |
您最近半年使用:0次
解题方法
10 . 钠碱循环法脱除烟气中的SO2,生成的吸收液中含有Na2SO3和NaHSO3。电解吸收液回收SO2,并实现碱液的循环。双极膜内层为水层,工作时水层中的H2O解离成H+和OH-,并分别通过离子交换膜向两侧发生迁移。如图为吸收液的电渗析装置示意图。下列说法正确的是
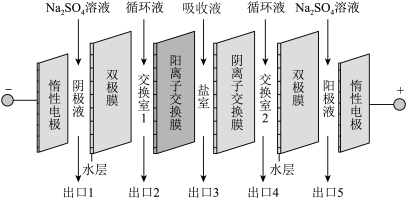

| A.出口4的产物为NaOH溶液 |
| B.出口5中Na2SO4溶液的浓度增大 |
C. 、 、 可从盐室最终进入阳极液中 可从盐室最终进入阳极液中 |
| D.阴极电极反应式为2H++2e- =H2↑ |
您最近半年使用:0次



