1 . Li-SO2Cl2电池可作为电源电解制备Ni(H2PO2)2,其工作原理如图所示。
已知电池反应方程式为 。
。

回答下列问题:
(1)Li电极是___________ (填“正极”或“负极”),C电极上的电极反应为___________ 。
(2)Li电极与___________ (填“镍”或“不锈钢”)相连,膜c为___________ 交换膜(填“阳离子”或“阴离子”)。
(3)电解一段时间后,Ⅳ室中氢氧化钠溶液浓度将___________ (填“增大”、“减小”或“不变”)。
(4)理论上产品室每获得283.5g的Ni(H2PO2)2,Li电极的质量减少___________ g。
已知电池反应方程式为
 。
。
回答下列问题:
(1)Li电极是
(2)Li电极与
(3)电解一段时间后,Ⅳ室中氢氧化钠溶液浓度将
(4)理论上产品室每获得283.5g的Ni(H2PO2)2,Li电极的质量减少
您最近半年使用:0次
2 . 在直流电源作用下,双极膜中间层中的H2O解离为H+和OH-。某技术人员利用双极膜(膜c、膜d)和离子交换膜高效制备H2SO4和NaOH,工作原理如图所示:
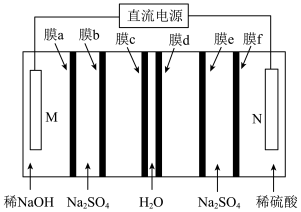
下列说法正确的是

下列说法正确的是
| A.电势:N电极<M电极 |
| B.双极膜膜c输出H+,膜a、膜e为阴离子交换膜 |
| C.N极电极反应式为2H2O+2e-=2OH-+H2↑ |
| D.当电路中转移1mole-时,整套装置将制得1molH2SO4 |
您最近半年使用:0次
名校
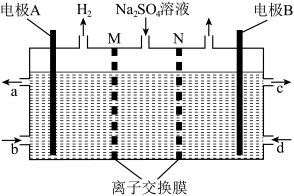
3 . 如图所示的阴、阳离子交换膜电解槽中,用惰性电极电解 溶液可制得硫酸和氢氧化钠溶液。下列说法不正确的是
溶液可制得硫酸和氢氧化钠溶液。下列说法不正确的是
 溶液可制得硫酸和氢氧化钠溶液。下列说法不正确的是
溶液可制得硫酸和氢氧化钠溶液。下列说法不正确的是
A.阳极反应式为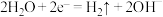 |
B. 为阴离子交换膜 为阴离子交换膜 |
C.进口b补充的是稀 溶液 溶液 |
D.电解过程中阳极附近的 不断降低 不断降低 |
您最近半年使用:0次
4 . 海水原位直接电解制氢的全新技术(如图所示)是利用海水侧和电解质(KOH)侧的水蒸气压力差使海水自发蒸发,并以蒸汽形式通过透气膜扩散到电解质侧重新液化,为电解提供淡水,工作时KOH溶液的浓度保持不变。下列叙述错误的是
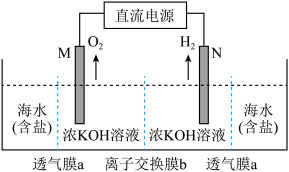

| A.电解制氢过程中电能转化为化学能 |
| B.膜b为阴离子交换膜 |
C.N电极的反应式为: |
| D.铅酸蓄电池做电源时,Pb电极与N电极相连 |
您最近半年使用:0次
名校
5 . 近日,美国工程院院士华裔科学家邵阳教授采用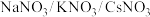 共晶盐电解液和
共晶盐电解液和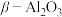 ,膜研制了一种熔盐型
,膜研制了一种熔盐型 电池,其工作原理如图所示:
电池,其工作原理如图所示:

该电池工作时,下列说法正确的是
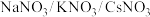 共晶盐电解液和
共晶盐电解液和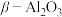 ,膜研制了一种熔盐型
,膜研制了一种熔盐型 电池,其工作原理如图所示:
电池,其工作原理如图所示:
该电池工作时,下列说法正确的是
A. 既表现氧化性又表现还原性 既表现氧化性又表现还原性 |
B.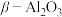 膜能阻止电子和离子通过 膜能阻止电子和离子通过 |
C.镍电极的电极反应式为 |
D.电池总反应为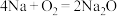 |
您最近半年使用:0次
2023-09-01更新
|
575次组卷
|
2卷引用:安徽省合肥市第八中学2022-2023学年高三上学期12月月考化学试题
名校
解题方法
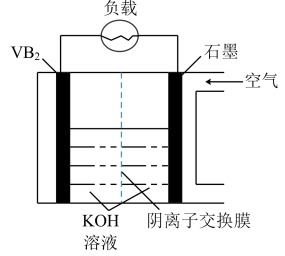
6 . 硼化钒( )一空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时发生的反应为
)一空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时发生的反应为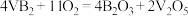 。下列说法正确的是
。下列说法正确的是
 )一空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时发生的反应为
)一空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时发生的反应为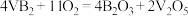 。下列说法正确的是
。下列说法正确的是
A. 电极为电池正极 电极为电池正极 |
B.电流由 极经KOH溶液流向石墨电极 极经KOH溶液流向石墨电极 |
C.当外电路转移1mol电子时,1 mol  从 从 电极移向石墨电极 电极移向石墨电极 |
D.电池工作过程中, 电极区电解质溶液浓度不变 电极区电解质溶液浓度不变 |
您最近半年使用:0次
2023-08-31更新
|
118次组卷
|
2卷引用:山西省大同市2023-2024学年高三上学期开学质量检测化学试题
2023高三下·全国·专题练习
名校
解题方法
7 . 微生物脱盐电池既可以处理废水中和铵盐,同时又能实现海水的淡化,原理如图所示,其中阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。下列说法正确的是
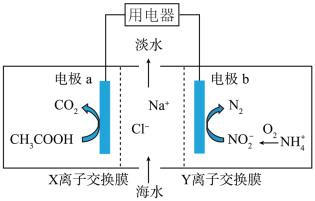
| A.电极a为正极,该电极上发生还原反应 |
| B.X离子交换膜为阳离子交换膜,Y离子交换膜为阴离子交换膜 |
| C.电极b上,每生成标况下2.24LN2,电路中转移0.6mol电子 |
| D.电池工作一段时间后,电极a和电极b产生的气体的物质的量之比为1∶2 |
您最近半年使用:0次
2023高三下·全国·专题练习
8 . 普通电解精炼铜的方法所制备的铜中仍含杂质,利用下面的双膜(阴离子交换膜和过滤膜)电解装置可制备高纯度的Cu。下列有关叙述中正确的是
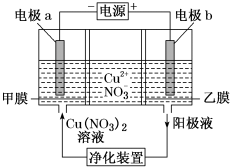

| A.电极a为精铜,电极b为粗铜 |
| B.甲膜为过滤膜,可阻止阳极泥及漂浮物杂质进入阴极区 |
| C.乙膜为阴离子交换膜,可阻止杂质阳离子进入阴极区 |
| D.当电路中通过1 mol电子时,可生成16 g精铜 |
您最近半年使用:0次
2023高三下·全国·专题练习
解题方法
9 . 完成下列问题。
(1)硝酸铵钙晶体[5Ca(NO3)2·NH4NO3·10H2O]极易溶于水,是一种绿色的复合肥料,生产硝酸铵钙工厂的废水中常含有硝酸铵,净化方法有反硝化净化法和电解法。
① 在酸性条件下可转化为N2,该反硝化方法可用半反应(同电极反应式)表示
在酸性条件下可转化为N2,该反硝化方法可用半反应(同电极反应式)表示___________ 。
②目前常用电解法净化,工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
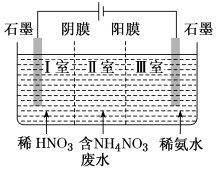
阳极的电极反应式为___________ 。Ⅰ室可回收的产品为___________ (填名称)。Ⅲ室可回收到氨气,请结合方程式和文字解释其原因___________ 。
(2)全钒液流储能电池是利用不同价态离子发生氧化还原反应来实现化学能和电能相互转化的,其装置原理如图:
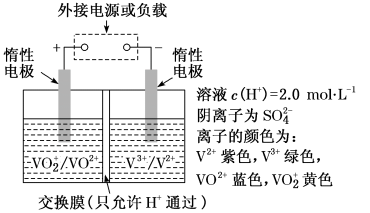
①当左槽溶液逐渐由黄变蓝,其电极反应式为___________ 。
②充电过程中,右槽溶液颜色逐渐由___________ 色变为___________ 色。
③放电过程中氢离子的作用是___________ 和___________ ;充电时若转移的电子数为6.02×1023个,左槽溶液中n(H+)的变化量为___________ 。
(1)硝酸铵钙晶体[5Ca(NO3)2·NH4NO3·10H2O]极易溶于水,是一种绿色的复合肥料,生产硝酸铵钙工厂的废水中常含有硝酸铵,净化方法有反硝化净化法和电解法。
①
 在酸性条件下可转化为N2,该反硝化方法可用半反应(同电极反应式)表示
在酸性条件下可转化为N2,该反硝化方法可用半反应(同电极反应式)表示②目前常用电解法净化,工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。

阳极的电极反应式为
(2)全钒液流储能电池是利用不同价态离子发生氧化还原反应来实现化学能和电能相互转化的,其装置原理如图:

①当左槽溶液逐渐由黄变蓝,其电极反应式为
②充电过程中,右槽溶液颜色逐渐由
③放电过程中氢离子的作用是
您最近半年使用:0次
名校
10 . 1,5-戊二胺[H2N(CH2)5NH2]用于高聚物制备和生物研究。利用双极膜(BPM)电渗析产碱技术可将生物发酵液中的1,5-戊二胺硫酸盐{[H3N(CH2)5NH3]SO4}转换为1,5-戊二胺产品,实现无害化提取,工作原理如图所示。下列说法正确的是


| A.N极电势高于M极 |
| B.可以从Ⅱ室得到浓度增大的H2SO4溶液 |
| C.理论上Ⅰ室和Ⅴ室产生的气体体积比为2∶1 |
| D.若Na2SO4溶液换为NaCl溶液,N极反应式为2Cl--2e-=Cl2↑,产生有毒气体 |
您最近半年使用:0次
2023-08-14更新
|
428次组卷
|
2卷引用:河北省迁安市第一中学2022-2023学年高三上学期期中考试化学试题



