1 . 常温下,下列离子在酸性条件下能大量存在的是
A. | B. | C. | D.CH3COO- |
您最近一年使用:0次
2024-01-10更新
|
152次组卷
|
3卷引用:贵州省黔东南州2023-2024学年高二上学期 期末化学试题
2 . W、X、Y、Z为原子序数依次增大的短周期元素,四种元素组成的无机盐溶于盐酸有无色无味的气体生成,离子 与
与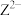 具有相同的核外电子数,下列叙述正确的是
具有相同的核外电子数,下列叙述正确的是
 与
与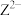 具有相同的核外电子数,下列叙述正确的是
具有相同的核外电子数,下列叙述正确的是A.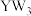 分子的空间结构为三角锥形 分子的空间结构为三角锥形 | B.原子半径: |
| C.X单质只有4种同素异形体 | D.W、Y、Z三种元素形成的化合物都是酸 |
您最近一年使用:0次
名校
解题方法
3 . 某实验小组用 溶液和
溶液和 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。
Ⅰ.配制 溶液
溶液
(1)若实验中需要配制 溶液,则需要称量NaOH固体
溶液,则需要称量NaOH固体_______ g。
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):_______ 。
Ⅱ.中和热的测定:
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。_______ ,实验中还需要用到量取溶液体积的玻璃仪器是_______ 。
(4)取 溶液和30mL硫酸溶液进行实验,实验数据如表。
溶液和30mL硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
②近似认为 溶液和
溶液和 硫酸溶液的密度都是
硫酸溶液的密度都是 ,中和后生成溶液的比热容
,中和后生成溶液的比热容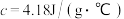 。则中和热
。则中和热
_______  (保留一位小数)。
(保留一位小数)。
③上述实验数值结果与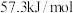 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是_______ (填字母)。
a.实验装置保温、隔热效果差
b.配制 溶液时俯视刻度线读数
溶液时俯视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用量筒量取NaOH溶液的体积时仰视读数
 溶液和
溶液和 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。Ⅰ.配制
 溶液
溶液(1)若实验中需要配制
 溶液,则需要称量NaOH固体
溶液,则需要称量NaOH固体(2)从图中选择称量NaOH固体所需要的仪器是(填字母):
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |
|
|
|
|
|
|
| 序号 | a | b | c | d | e | f |
Ⅱ.中和热的测定:
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。

(4)取
 溶液和30mL硫酸溶液进行实验,实验数据如表。
溶液和30mL硫酸溶液进行实验,实验数据如表。①请填写表中的空白:
温度 实验次数 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温度差平均值( )/℃ )/℃ | ||
 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
 溶液和
溶液和 硫酸溶液的密度都是
硫酸溶液的密度都是 ,中和后生成溶液的比热容
,中和后生成溶液的比热容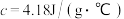 。则中和热
。则中和热
 (保留一位小数)。
(保留一位小数)。③上述实验数值结果与
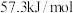 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是a.实验装置保温、隔热效果差
b.配制
 溶液时俯视刻度线读数
溶液时俯视刻度线读数c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用量筒量取NaOH溶液的体积时仰视读数
您最近一年使用:0次
2023-02-01更新
|
239次组卷
|
2卷引用:贵州省凯里市第一中学2022-2023学年高二上学期期末考试化学试题
4 . 在无色透明的溶液中,可以大量共存的离子组是
A. | B. |
C. | D. |
您最近一年使用:0次
解题方法
5 . 在实验室采用如图装置制备、收集气体,合理的是


| 编号 | 气体 | a | b |
| A |  | 浓氨水 | 生石灰 |
| B |  | 稀盐酸 | 碳酸钙 |
| C |  | 浓盐酸 | 二氧化锰 |
| D |  | 浓硝酸 | 铁片 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 氦气所含原子数目为 氦气所含原子数目为 |
B.常温下,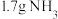 含共价键数目为 含共价键数目为 |
C.常温下, 的 的 溶液中,所含 溶液中,所含 数目为 数目为 |
D. 与水反应,生成 与水反应,生成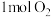 转移电子数目为 转移电子数目为 |
您最近一年使用:0次
解题方法
7 . 设NA为阿伏加德罗常数。下列说法正确的是
| A.同温同压下,O2和O3的密度可能相同 |
| B.0.5 mol 环丙烷和0. 5 mol丙烯所含共用电子对数均为4. 5NA |
| C.18g H2O和20 g D2O(重水)所含中子数目均为8NA |
| D.室温下,pH相同的KCl溶液和Na2SO4溶液,其溶质的物质的量浓度相同 |
您最近一年使用:0次
名校
8 . 已知X、Y、Z、W、M 是核电荷数依次增大的五种短周期主族元素。 常温下这五种元素对应的单质均为常见气体。下列说法错误的是
| A.原子半径:M>W;氢化物的稳定性:Y<Z |
| B.Y、Z、W为同周期元素;X、Y、M三元素的最高正化合价依次升高 |
| C.W元素的非金属性最强,所以其最高价氧化物的水化物酸性最强 |
| D.M的单质溶于X和Z形成的常见化合物中,在疫情期间应用广泛 |
您最近一年使用:0次
2022-08-08更新
|
148次组卷
|
2卷引用:贵州省铜仁市2021-2022学年高二下学期期末质量检测理综化学试题
9 . 某化学小组为测定某化学品[通式为aAl(OH)3·bMgCO3 cH2O,a、b、c均为正整数]的组成及镁元素的质量分数,设计以下两种实验方案,填写下列空白:
I.甲同学设计如下方案:
①称取一定质量的样品和足量的稀硫酸按如图所示装量置实验,测定CO2的体积(忽略水蒸气体积 );

②对步骤①所得装置I中混合物进行过滤;在滤液中加入过量氨水,过滤;
③灼烧步骤②所得滤渣,直至残留固体恒重。
(1)利用如图装置测定二氧化碳体积(装置II中盛装饱和碳酸氢钠溶液),“安全漏斗”的“安全”含义是_______ 。实验完毕后,装置I内残留有CO2 ,对测定结果是否有影响? 答:_____ (填“有”或“无”)。
(2)下列有关Al(OH)3的说法正确的是_______ (填字母)。
a. Al(OH)3既能与所有酸反应,又能与所有碱反应
b.氢氧化铝的酸性比H2CO3弱
c.Al(OH)3不稳定性,受热分解生成Al2O3和H2O
d.氢氧化铝胶体粒子可聚沉水中杂质
(3)灼烧滤渣除需要酒精灯、三脚架、泥三角、玻璃棒、坩埚钳外,还缺少的仪器是_______ (填名称)。
II.乙同学利用如图装置测定:

(4)A的作用是_________ ;C中试剂是______ (填名称)。
(5)若样品质量为29.4 g,装置C、D分别净增10.8g、4.4 g,则样品的主要成分化学式为_______ ;样品中镁元素的质量分数为_______ (保留小数点后1位小数)。
I.甲同学设计如下方案:
①称取一定质量的样品和足量的稀硫酸按如图所示装量置实验,测定CO2的体积(忽略水蒸气体积 );

②对步骤①所得装置I中混合物进行过滤;在滤液中加入过量氨水,过滤;
③灼烧步骤②所得滤渣,直至残留固体恒重。
(1)利用如图装置测定二氧化碳体积(装置II中盛装饱和碳酸氢钠溶液),“安全漏斗”的“安全”含义是
(2)下列有关Al(OH)3的说法正确的是
a. Al(OH)3既能与所有酸反应,又能与所有碱反应
b.氢氧化铝的酸性比H2CO3弱
c.Al(OH)3不稳定性,受热分解生成Al2O3和H2O
d.氢氧化铝胶体粒子可聚沉水中杂质
(3)灼烧滤渣除需要酒精灯、三脚架、泥三角、玻璃棒、坩埚钳外,还缺少的仪器是
II.乙同学利用如图装置测定:

(4)A的作用是
(5)若样品质量为29.4 g,装置C、D分别净增10.8g、4.4 g,则样品的主要成分化学式为
您最近一年使用:0次
解题方法
10 . 某溶液中可能存在 7种离子中的某几种。现取该溶液进行实验,得到如下现象:
7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中滴加足量 溶液,无沉淀生成;
溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
已知: 。
。
据此可以判断,该溶液中一定存在的离子组是
 7种离子中的某几种。现取该溶液进行实验,得到如下现象:
7种离子中的某几种。现取该溶液进行实验,得到如下现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中滴加足量
 溶液,无沉淀生成;
溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
已知:
 。
。据此可以判断,该溶液中一定存在的离子组是
A. | B. |
C. | D. |
您最近一年使用:0次
2022-07-19更新
|
462次组卷
|
2卷引用:贵州省黔东南苗族侗族自治州)2021-2022学年高二下学期期末联考化学试题









