解题方法
1 . 过氧化钙( )广泛应用于水产养殖、污水处理,是优良的供氧剂。
)广泛应用于水产养殖、污水处理,是优良的供氧剂。
探究一; 与水反应除生成氧气外,还生成什么物质?
与水反应除生成氧气外,还生成什么物质?
(1)取适量 放入试管中加适量水,向试管中滴加酚酞溶液,液体变成红色,说明生成了
放入试管中加适量水,向试管中滴加酚酞溶液,液体变成红色,说明生成了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________________ 。
(2)此供氧剂长期暴露在空气中,会变质生成 ,为检验此供氧剂是否变质,某同学向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。其他同学不认同上述方案的理由是
,为检验此供氧剂是否变质,某同学向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。其他同学不认同上述方案的理由是___________________ 。
探究二:测定久置过氧化钙纯度。
方案一:通过测定产生氧气的体积,最终计算出供氧剂中过氧化钙的含量。
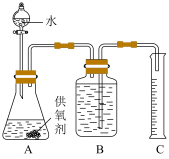
(3)取一定质量的供氧剂溶于水,按照如图装置进行装配。读出体积时要注意:①该反应为放热反应。待气体恢复至室温再读数;②_____________ ;③视线和凹液面最低处保持水平再读数。
方案二:把样品中的 转化为碳酸钙,通过测定碳酸钙沉淀的质量,求得
转化为碳酸钙,通过测定碳酸钙沉淀的质量,求得 的质量,具体流程如下:
的质量,具体流程如下:

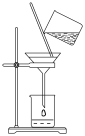
(4)指出下图所示过滤操作中不规范之处_______________ 。
(5)滴加的 溶液要过量的原因是
溶液要过量的原因是______________ ,计算样品中 的物质的量为
的物质的量为____________ 。
 )广泛应用于水产养殖、污水处理,是优良的供氧剂。
)广泛应用于水产养殖、污水处理,是优良的供氧剂。探究一;
 与水反应除生成氧气外,还生成什么物质?
与水反应除生成氧气外,还生成什么物质?(1)取适量
 放入试管中加适量水,向试管中滴加酚酞溶液,液体变成红色,说明生成了
放入试管中加适量水,向试管中滴加酚酞溶液,液体变成红色,说明生成了 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(2)此供氧剂长期暴露在空气中,会变质生成
 ,为检验此供氧剂是否变质,某同学向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。其他同学不认同上述方案的理由是
,为检验此供氧剂是否变质,某同学向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。其他同学不认同上述方案的理由是探究二:测定久置过氧化钙纯度。
方案一:通过测定产生氧气的体积,最终计算出供氧剂中过氧化钙的含量。
(3)取一定质量的供氧剂溶于水,按照如图装置进行装配。读出体积时要注意:①该反应为放热反应。待气体恢复至室温再读数;②

方案二:把样品中的
 转化为碳酸钙,通过测定碳酸钙沉淀的质量,求得
转化为碳酸钙,通过测定碳酸钙沉淀的质量,求得 的质量,具体流程如下:
的质量,具体流程如下:
(4)指出下图所示过滤操作中不规范之处

(5)滴加的
 溶液要过量的原因是
溶液要过量的原因是 的物质的量为
的物质的量为
您最近一年使用:0次
名校
解题方法
2 . 某小组为探究 (三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。

(1)在实验进行的过程中,应该持续通入氮气的目的是___________ 。
(2)若实验中观察装置F中澄清石灰水变浑浊,装置E中固体变为红色,则说明 的热分解产物中一定含有
的热分解产物中一定含有___________ 。
(3)该样品完全热分解后,欲检测固体生成物中的组成,某同学待装置冷却后取少量固体加入稀硫酸溶解,再加入 溶液变红,说明
溶液变红,说明___________ 。
(4)已知: 是一种光敏化合物,见光分解。该实验小组在探究
是一种光敏化合物,见光分解。该实验小组在探究 热分解后,用该装置再次探究它光解的产物,现取
热分解后,用该装置再次探究它光解的产物,现取 固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
完成下列小题:
①若反应后 元素的化合价降为
元素的化合价降为 价,K元素的化合价未改变,且两者仍为草酸
价,K元素的化合价未改变,且两者仍为草酸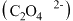 盐,写出三草酸合铁酸钾完全光解的化学方程式
盐,写出三草酸合铁酸钾完全光解的化学方程式___________ 。
②据此计算出该 固体的纯度为
固体的纯度为___________ (保留一位有效数字) 。
③样品完全分解后,实验小组停止通氮气,一段时间后,某同学取少许装置A中的残留物于试管中,加入稀硫酸溶解,滴入1~2滴 溶液,发现溶液变红,这与上述
溶液,发现溶液变红,这与上述 分解产物为
分解产物为 价
价 的结论不符可能的原因是
的结论不符可能的原因是___________ 。
 (三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(1)在实验进行的过程中,应该持续通入氮气的目的是
(2)若实验中观察装置F中澄清石灰水变浑浊,装置E中固体变为红色,则说明
 的热分解产物中一定含有
的热分解产物中一定含有(3)该样品完全热分解后,欲检测固体生成物中的组成,某同学待装置冷却后取少量固体加入稀硫酸溶解,再加入
 溶液变红,说明
溶液变红,说明(4)已知:
 是一种光敏化合物,见光分解。该实验小组在探究
是一种光敏化合物,见光分解。该实验小组在探究 热分解后,用该装置再次探究它光解的产物,现取
热分解后,用该装置再次探究它光解的产物,现取 固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。完成下列小题:
①若反应后
 元素的化合价降为
元素的化合价降为 价,K元素的化合价未改变,且两者仍为草酸
价,K元素的化合价未改变,且两者仍为草酸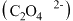 盐,写出三草酸合铁酸钾完全光解的化学方程式
盐,写出三草酸合铁酸钾完全光解的化学方程式②据此计算出该
 固体的纯度为
固体的纯度为③样品完全分解后,实验小组停止通氮气,一段时间后,某同学取少许装置A中的残留物于试管中,加入稀硫酸溶解,滴入1~2滴
 溶液,发现溶液变红,这与上述
溶液,发现溶液变红,这与上述 分解产物为
分解产物为 价
价 的结论不符可能的原因是
的结论不符可能的原因是
您最近一年使用:0次
名校
3 . 二氯异氰尿酸钠(NaC3N3O3Cl2)是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。工业上合成二氯异氰尿酸钠的方法有多种,其中NaClO法是向NaOH溶液通入Cl2产生高浓度NaClO溶液,然后与氰尿酸(C3H3N3O3)反应制取二氯异氰尿酸钠:2NaClO+C3H3N3O3=NaC3N3O3Cl2+NaOH+H2O。
(1)从下面选择所需装置完成实验,按气流从左至右,导管口连接顺序为______ (填小写字母)。
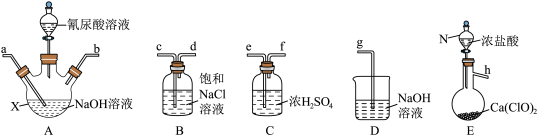
(2)若发现实际操作过程中仪器N中浓盐酸不易流下,可将仪器N换为_________ 。
(3)装置A中制备NaClO溶液完成的现象是___________ ,在加氰尿酸溶液过程仍需不断通入Cl2的理由是___________ 。
(4)有效氯含量是判断产品质量的标准。实验采用碘量法测定产物有效氯的含量,原理为: +H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O,
+H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O, ,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
①配制样品溶液时,需要用到的玻璃仪器除烧杯、玻璃棒外,还需要___________ 。
②二氯异氰尿酸钠优质品要求有效氯大于60%,通过计算判断该样品是否为优质品________ 。( 该样品的有效氯  )(写出计算过程)
)(写出计算过程)
③若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值______ (填“偏高”或“偏低”)。
(5)高铁酸钾是一种重要的多功能绿色净水剂,暗紫色具有金属光泽的粉末,无臭无味,干燥品在室温下稳定,在强碱溶液中稳定。
①配平K2FeO4与水反应的化学方程式,并用单线桥标出电子转移方向和数目________ 。___K2FeO4+____H2O=___Fe(OH)3胶体+____O2↑+____KOH,被还原的元素是___________ 。
②结合高铁酸钾的性质,说明它是一种多功能绿色净水剂的原因:_________ 。
(1)从下面选择所需装置完成实验,按气流从左至右,导管口连接顺序为

(2)若发现实际操作过程中仪器N中浓盐酸不易流下,可将仪器N换为
(3)装置A中制备NaClO溶液完成的现象是
(4)有效氯含量是判断产品质量的标准。实验采用碘量法测定产物有效氯的含量,原理为:
 +H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O,
+H++2H2O=C3H3N3O3+2HClO,HClO+2I-+H+=I2+Cl-+H2O, ,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。
,准确称取1.120g样品,配成250mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;加入0.1000mol/LNa2S2O3溶液20.00mL恰好完全反应。①配制样品溶液时,需要用到的玻璃仪器除烧杯、玻璃棒外,还需要
②二氯异氰尿酸钠优质品要求有效氯大于60%,通过计算判断该样品是否为优质品
 )(写出计算过程)
)(写出计算过程)③若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值
(5)高铁酸钾是一种重要的多功能绿色净水剂,暗紫色具有金属光泽的粉末,无臭无味,干燥品在室温下稳定,在强碱溶液中稳定。
①配平K2FeO4与水反应的化学方程式,并用单线桥标出电子转移方向和数目
②结合高铁酸钾的性质,说明它是一种多功能绿色净水剂的原因:
您最近一年使用:0次
名校
解题方法
4 . 为探究Na与CO2反应产物,某化学兴趣小组按如图装置进行实验。已知PdCl2能被CO还原得到银白色的Pd。

请回答下列问题:
(1)仪器X的名称是___________ 。
(2)B、C装置的目的是使进入D装置中的气体为干燥、纯净的CO2,则其中装置B的具体作用是___________ 。
(3)先称量硬质玻璃管的质量为m1g,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2g.再按如下顺序进行实验操作。
①打开K1和K2,通入CO2至E中出现实验现象为___________ ;
②点燃酒精灯,加热;
③熄灭酒精灯;
④冷却到室温;
⑤关闭K1和K2;
⑥称量硬质玻璃管。
重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3g。
(4)加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色物质产生。
③F中试管内壁有银白物质产生。
(5)探究硬质玻璃管中,固体产物所含钠元素的存在形式:
假设一:只有Na2CO3;
假设二:只有Na2O;
假设三:___________ 。
请完成下列实验设计(完善操作步骤及相应实验现象),验证上述假设:
步骤1.将硬质玻璃管中的固体产物溶于水后过滤;
步骤2.往步骤1所得滤液中加入足量的___________ 溶液产生白色沉淀,过滤;
步骤3.往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色。
结论:假设一成立。
(6)根据上述实验现象及下表实验数据,写出Na与CO2反应的总化学方程式:___________ 。

请回答下列问题:
(1)仪器X的名称是
(2)B、C装置的目的是使进入D装置中的气体为干燥、纯净的CO2,则其中装置B的具体作用是
(3)先称量硬质玻璃管的质量为m1g,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2g.再按如下顺序进行实验操作。
①打开K1和K2,通入CO2至E中出现实验现象为
②点燃酒精灯,加热;
③熄灭酒精灯;
④冷却到室温;
⑤关闭K1和K2;
⑥称量硬质玻璃管。
重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3g。
(4)加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色物质产生。
③F中试管内壁有银白物质产生。
(5)探究硬质玻璃管中,固体产物所含钠元素的存在形式:
假设一:只有Na2CO3;
假设二:只有Na2O;
假设三:
请完成下列实验设计(完善操作步骤及相应实验现象),验证上述假设:
步骤1.将硬质玻璃管中的固体产物溶于水后过滤;
步骤2.往步骤1所得滤液中加入足量的
步骤3.往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色。
结论:假设一成立。
(6)根据上述实验现象及下表实验数据,写出Na与CO2反应的总化学方程式:
| m1 | m2 | m3 |
| 66.70g | 69.00g | 72.15g |
您最近一年使用:0次



