名校
解题方法
1 . 人类对物质微观结构的探索从未停歇,随着科学技术的发展,新的发现将继续揭开开原子更深层次结构的奥秘.
(1)原子结构模型的演变顺序正确的是
①道尔顿模型 ②有核模型 ③葡萄干面包模型 ④电子云模型 ⑤玻尔模型
(2)第一位通过实验证明原子可以再分的科学家是
(3)卢瑟福团队用 粒子
粒子 来轰击金箔,该化学符号中4代表的含义是①
来轰击金箔,该化学符号中4代表的含义是①_____________ ;在1~18号元素中,最外层电子数与氦原子相等的元素是②_____________ (填元素符号)。
(4)氦元素在自然界中仅有 和
和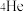 两种原子,它们具有相同的
两种原子,它们具有相同的
(5)当用 粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
(6)关于 粒子散射实验现象的记载如下:①________的
粒子散射实验现象的记载如下:①________的 粒子都直接穿过金箔,②______的
粒子都直接穿过金箔,②______的 粒子发生偏转,③ 的
粒子发生偏转,③ 的 粒子甚至被直接反弹回去.①②③三处空格分别为
粒子甚至被直接反弹回去.①②③三处空格分别为
(7)通过该试验,卢瑟福得出了原子结构的_____________ 模型。
(8)2022年诺贝尔化学奖授予三位在“点击化学和生物正交化学”方面作出突出贡献的科学家.点击化学的核心理念是,通过小单元的简便拼接,快速可靠地完成各种各样分子的化学合成.在点击化学中,反应快速发生,而且不会产生副产物.下列有关点击化学说法错误的是
(1)原子结构模型的演变顺序正确的是
①道尔顿模型 ②有核模型 ③葡萄干面包模型 ④电子云模型 ⑤玻尔模型
| A.①③②⑤④ | B.①②③④⑤ | C.①⑤③②④ | D.①③⑤④② |
(2)第一位通过实验证明原子可以再分的科学家是
| A.德谟克利特 | B.道尔顿 | C.汤姆孙 | D.卢瑟福 |
(3)卢瑟福团队用
 粒子
粒子 来轰击金箔,该化学符号中4代表的含义是①
来轰击金箔,该化学符号中4代表的含义是①(4)氦元素在自然界中仅有
 和
和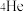 两种原子,它们具有相同的
两种原子,它们具有相同的 | A.质子数 | B.中子数 | C.物理性质 | D.化学性质 |
(5)当用
 粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是 
| A.A | B.B | C.C | D.D |
(6)关于
 粒子散射实验现象的记载如下:①________的
粒子散射实验现象的记载如下:①________的 粒子都直接穿过金箔,②______的
粒子都直接穿过金箔,②______的 粒子发生偏转,③ 的
粒子发生偏转,③ 的 粒子甚至被直接反弹回去.①②③三处空格分别为
粒子甚至被直接反弹回去.①②③三处空格分别为 | A.绝大多数,极少数,个别 | B.个别,极少数,绝大多数 |
| C.几乎半数,几乎半数,个别 | D.个别,几乎半数,几乎半数 |
(7)通过该试验,卢瑟福得出了原子结构的
(8)2022年诺贝尔化学奖授予三位在“点击化学和生物正交化学”方面作出突出贡献的科学家.点击化学的核心理念是,通过小单元的简便拼接,快速可靠地完成各种各样分子的化学合成.在点击化学中,反应快速发生,而且不会产生副产物.下列有关点击化学说法错误的是
| A.点击化学的反应中会出现新的分子 | B.点击化学的反应中会出现新的原子 |
| C.点击化学能提高反应的准确性 | D.点击化学在生物医疗领域有广泛的应用前景 |
您最近一年使用:0次
名校
解题方法
2 . 100mL 甲溶液可能含有H+、K+、NH 、Ba2+、CO
、Ba2+、CO 、SO
、SO 、Cl-中的若干种。取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。下列说法中不正确的是
、Cl-中的若干种。取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。下列说法中不正确的是

 、Ba2+、CO
、Ba2+、CO 、SO
、SO 、Cl-中的若干种。取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。下列说法中不正确的是
、Cl-中的若干种。取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。下列说法中不正确的是
| A.原溶液一定不存在 H+、Ba2+,可能存在K+,可通过焰色试验来检验 |
| B.原溶液一定存在Cl-, 且c(Cl-)≤0.1mol/L |
| C.沉淀1转化为沉淀2时,放出的气体标况下的体积为224mL |
D.若甲溶液中先加 BaCl2溶液,产生白色沉淀,再加足量稀盐酸沉淀不溶解,不能证明此溶液中含有SO |
您最近一年使用:0次
2023-11-08更新
|
518次组卷
|
2卷引用: 四川省成都市树德中学2023-2024学年高一上学期11月期中考试化学试题
3 . 三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O(M=491g/mol)是一种感光剂和高效的污水处理剂。
I.某研究小组同学查阅资料发现K3[Fe(C2O4)3]·3H2O加热后会分解产生CO和CO2,于是设计了如下实验进行验证。请回答:
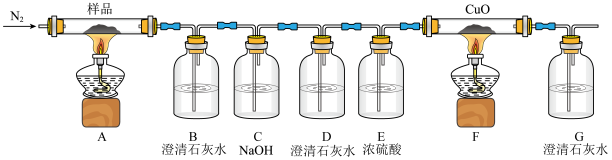
(1)C中NaOH溶液的作用为___________ ;D中澄清石灰水作用为___________ 。
(2)证明有CO产生的现象为___________ 。
(3)该装置还存在的缺陷是___________ 。
II.制备K3[Fe(C2O4)3]·3H2O的途径如下,请回答下列问题:
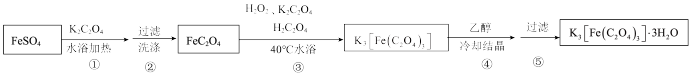
研究小组通过查阅资料得知:
a.K3[Fe(C2O4)3]·3H2O对光敏感,易溶于水,难溶于乙醇;
b.很多草酸盐(例如CaC2O4、BaC2O4)难溶于水,但能溶解于稀硝酸。
(4)步骤③中,控制水浴温度不能超过40℃的原因为___________ 。
(5)研究小组的同学对K3[Fe(C2O4)3]组成有两种看法,分别为:
甲同学:K3[Fe(C2O4)3]由K+、Fe3+、 构成;
构成;
乙同学:K3[Fe(C2O4)3]由K+、[Fe(C2O4)3]3-构成。
请设计实验,验证哪位同学的说法是正确的:___________ 。
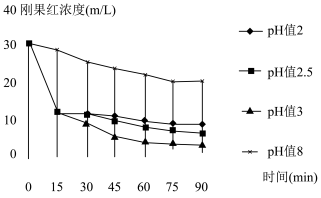
(6)K3[Fe(C2O4)3]联合H2O2体系可用于降解染料,一定浓度的该混合溶液,在不同pH条件下降解刚果红的效率如图所示,在实际应用过程中,应选择pH=___________ 。
(7)关于制备流程,下列说法正确的是___________。
(8)制得的K3[Fe(C2O4)3]·3H2O含少量FeC2O4·2H2O,为测定其纯度,进行如下实验:
步骤I:称取5.000g三草酸合铁酸钾晶体,配制成1.000L溶液,固体完全溶解。
步骤II:取20.00mL溶液,与0.1000molL-酸性KMnO4溶液反应,消耗2.46mL。
步骤III:另取20.00mL溶液,加入过量铜粉,过滤,洗涤,将滤液和洗涤液合并。
步骤IV:将合并液与0.1000mol/L酸性KMnO4溶液反应,消耗2.86mL。
已知 与
与 的反应为(未配平):
的反应为(未配平): +
+ +H+→CO2↑+Mn2++H2O
+H+→CO2↑+Mn2++H2O
①写出Fe2+与酸性KMnO4溶液反应的离子方程式:___________ 。
②研究小组制得的K3[Fe(C2O4)3]·3H2O纯度为___________ 。
I.某研究小组同学查阅资料发现K3[Fe(C2O4)3]·3H2O加热后会分解产生CO和CO2,于是设计了如下实验进行验证。请回答:

(1)C中NaOH溶液的作用为
(2)证明有CO产生的现象为
(3)该装置还存在的缺陷是
II.制备K3[Fe(C2O4)3]·3H2O的途径如下,请回答下列问题:

研究小组通过查阅资料得知:
a.K3[Fe(C2O4)3]·3H2O对光敏感,易溶于水,难溶于乙醇;
b.很多草酸盐(例如CaC2O4、BaC2O4)难溶于水,但能溶解于稀硝酸。
(4)步骤③中,控制水浴温度不能超过40℃的原因为
(5)研究小组的同学对K3[Fe(C2O4)3]组成有两种看法,分别为:
甲同学:K3[Fe(C2O4)3]由K+、Fe3+、
 构成;
构成;乙同学:K3[Fe(C2O4)3]由K+、[Fe(C2O4)3]3-构成。
请设计实验,验证哪位同学的说法是正确的:
(6)K3[Fe(C2O4)3]联合H2O2体系可用于降解染料,一定浓度的该混合溶液,在不同pH条件下降解刚果红的效率如图所示,在实际应用过程中,应选择pH=

(7)关于制备流程,下列说法正确的是___________。
| A.步骤①为复分解反应,步骤③为氧化还原反应 |
| B.步骤②判断沉淀是否洗涤干净,可以取少量最后一次洗涤液,加入氯化钡溶液,观察是否有白色沉淀产生 |
| C.步骤④,加入乙醇目的在于降低K3[Fe(C2O4)3]的溶解度,使其结晶析出 |
| D.步骤④⑤可以在日光下进行 |
(8)制得的K3[Fe(C2O4)3]·3H2O含少量FeC2O4·2H2O,为测定其纯度,进行如下实验:
步骤I:称取5.000g三草酸合铁酸钾晶体,配制成1.000L溶液,固体完全溶解。
步骤II:取20.00mL溶液,与0.1000molL-酸性KMnO4溶液反应,消耗2.46mL。
步骤III:另取20.00mL溶液,加入过量铜粉,过滤,洗涤,将滤液和洗涤液合并。
步骤IV:将合并液与0.1000mol/L酸性KMnO4溶液反应,消耗2.86mL。
已知
 与
与 的反应为(未配平):
的反应为(未配平): +
+ +H+→CO2↑+Mn2++H2O
+H+→CO2↑+Mn2++H2O①写出Fe2+与酸性KMnO4溶液反应的离子方程式:
②研究小组制得的K3[Fe(C2O4)3]·3H2O纯度为
您最近一年使用:0次
名校
解题方法
4 . 为检验某加碘食盐中是否含有 ,取相同食盐样品进行下表所示实验:
,取相同食盐样品进行下表所示实验:
已知:
下列说法中正确的是
 ,取相同食盐样品进行下表所示实验:
,取相同食盐样品进行下表所示实验:已知:

| 实验① | 实验② | 实验③ |
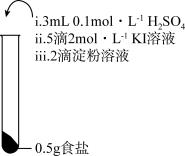 | 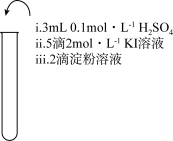 | 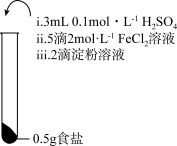 |
| 振荡,溶液迅速变为蓝色 | 振荡,一段时间后溶液变为浅蓝色 | 振荡,溶液变为浅黄色 |
A.仅由实验①就能证明食盐样品中存在 |
B.以上实验说明离子的还原性: |
C.实验③能证明食盐样品中不存在 |
D.实验②中发生反应的离子方程式为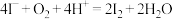 |
您最近一年使用:0次
2023-11-04更新
|
299次组卷
|
2卷引用:北京交通大学附属中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
5 . 某同学进行有关 的性质实验。下列说法不正确的是
的性质实验。下列说法不正确的是

 的性质实验。下列说法不正确的是
的性质实验。下列说法不正确的是
| A.图I可以用来收集氯气 |
B.图III中若气球干瘪,证明 可与NaOH反应 可与NaOH反应 |
| C.图II中生成棕黄色的烟,加少量水溶解得到蓝色溶液 |
D.图I中发生反应的离子方程式为 |
您最近一年使用:0次
2022-12-28更新
|
211次组卷
|
2卷引用:陕西省渭南市华阴市2021-2022学年高一上学期期末考试化学试题
6 . 下图为氯化钠在不同状态下的导电实验微观示意图(X、Y都是石墨电极)。下列说法不正确 的是
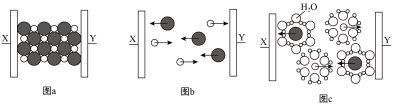

A.图示中的 代表的是 代表的是 | B.图a表示氯化钠固体,不导电 |
| C.图b表示氯化钠熔融时离子键被破坏 | D.图c能证明氯化钠溶液是电解质 |
您最近一年使用:0次
名校
解题方法
7 . 实验室用如下方法测定 与
与 的混合物中
的混合物中 的质量分数。
的质量分数。
(1)称取该混合物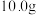 ,溶于水配成
,溶于水配成 溶液,下列操作会使所配溶液浓度偏小的有
溶液,下列操作会使所配溶液浓度偏小的有____ (填标号)。
A.未将洗涤液转移至容量瓶中
B.定容时俯视刻度线
C.定容振荡摇匀后液面低于刻度线,未做处理
(2)量取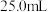 上述溶液于烧杯中,滴加足量
上述溶液于烧杯中,滴加足量 溶液,将
溶液,将 、
、 完全转化为沉淀,其中
完全转化为沉淀,其中 参与反应的离子方程式为
参与反应的离子方程式为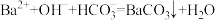 ,
, 属于
属于_______ (填“酸碱”或“盐”)。
(3)简述证明溶液中 、
、 已完全转化为沉淀的操作及现象:
已完全转化为沉淀的操作及现象:________ 。
 与
与 的混合物中
的混合物中 的质量分数。
的质量分数。(1)称取该混合物
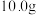 ,溶于水配成
,溶于水配成 溶液,下列操作会使所配溶液浓度偏小的有
溶液,下列操作会使所配溶液浓度偏小的有A.未将洗涤液转移至容量瓶中
B.定容时俯视刻度线
C.定容振荡摇匀后液面低于刻度线,未做处理
(2)量取
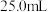 上述溶液于烧杯中,滴加足量
上述溶液于烧杯中,滴加足量 溶液,将
溶液,将 、
、 完全转化为沉淀,其中
完全转化为沉淀,其中 参与反应的离子方程式为
参与反应的离子方程式为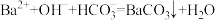 ,
, 属于
属于(3)简述证明溶液中
 、
、 已完全转化为沉淀的操作及现象:
已完全转化为沉淀的操作及现象:
您最近一年使用:0次
解题方法
8 . Ⅰ. 广泛用作水处理剂及漂白剂。
广泛用作水处理剂及漂白剂。
已知:25℃时 溶液中
溶液中 、
、 物质的量分数随
物质的量分数随 的分布如图所示。
的分布如图所示。

(1)工业上将 通入
通入 的
的 溶液中制备
溶液中制备 。
。
①制备 的化学方程式为
的化学方程式为______ 。
②溶液 时,该溶液中主要存在的阴离子有
时,该溶液中主要存在的阴离子有______ (填化学式)。
Ⅱ. 是一种重要的杀菌消毒剂,其一种生产工艺如下:
是一种重要的杀菌消毒剂,其一种生产工艺如下:

(2)写出“反应”步骤中生成 的化学方程式
的化学方程式______ 。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和
和 ,要加入的试剂分别为
,要加入的试剂分别为______ ,______ 。精制时如何证明 已经完全除尽:
已经完全除尽:______ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,发生如下反应:
,发生如下反应:
______ ______
______ ______
______ ______
______ ______
______ ______
______
①配平上述化学方程式。______
②某容器中发生一个化学反应,其中涉及 、
、 、
、 、
、 、
、 、
、 六种粒子。其中
六种粒子。其中 、
、 的物质的量随时间变化的曲线如图所示。
的物质的量随时间变化的曲线如图所示。

则该反应的离子方程式为:______ 。
 广泛用作水处理剂及漂白剂。
广泛用作水处理剂及漂白剂。已知:25℃时
 溶液中
溶液中 、
、 物质的量分数随
物质的量分数随 的分布如图所示。
的分布如图所示。
(1)工业上将
 通入
通入 的
的 溶液中制备
溶液中制备 。
。①制备
 的化学方程式为
的化学方程式为②溶液
 时,该溶液中主要存在的阴离子有
时,该溶液中主要存在的阴离子有Ⅱ.
 是一种重要的杀菌消毒剂,其一种生产工艺如下:
是一种重要的杀菌消毒剂,其一种生产工艺如下:
(2)写出“反应”步骤中生成
 的化学方程式
的化学方程式(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 和
和 ,要加入的试剂分别为
,要加入的试剂分别为 已经完全除尽:
已经完全除尽:(4)“尾气吸收”是吸收“电解”过程排出的少量
 ,发生如下反应:
,发生如下反应:______
 ______
______ ______
______ ______
______ ______
______ ______
______
①配平上述化学方程式。
②某容器中发生一个化学反应,其中涉及
 、
、 、
、 、
、 、
、 、
、 六种粒子。其中
六种粒子。其中 、
、 的物质的量随时间变化的曲线如图所示。
的物质的量随时间变化的曲线如图所示。
则该反应的离子方程式为:
您最近一年使用:0次
9 . 某小组同学分别探究 溶液、
溶液、 溶液的性质。
溶液的性质。
Ⅰ.探究 溶液的性质。
溶液的性质。
(1)预测 具有氧化性,因此可以与Zn反应,此时Zn体现
具有氧化性,因此可以与Zn反应,此时Zn体现______ 性。
(2)预测 具有还原性,预测依据是
具有还原性,预测依据是______ ,因此可以与酸性 溶液反应。
溶液反应。
(3)进行如下实验操作:
①i中的现象是产生白色沉淀,变为灰绿色,最终为红褐色,用化学方程式表示产生该现象的原因: 、
、______ 。
②iii中的现象是______ 。
(4)某同学认为 中现象并不能证明
中现象并不能证明 具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象,②为证实该反应中
具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象,②为证实该反应中 确实被氧化,需要在反应后的溶液中加入试剂
确实被氧化,需要在反应后的溶液中加入试剂______ ,观察到现象______ 。
Ⅱ.探究 溶液的性质。
溶液的性质。
小组同学进行如下实验操作并观察到对应现象:
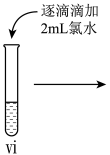
(5)ⅳ中反应的离子方程式是______ 。
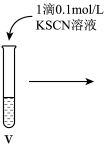
(6)vi中滴加氯水过程中,氯水反应的离子方程式是______ 。
Ⅲ.小组同学探究vi中褪色原因,提出两种假设:a.铁离子被转化,b.被转化。
(7)进一步预测 可能被转化为
可能被转化为 ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象______ 。
 溶液、
溶液、 溶液的性质。
溶液的性质。Ⅰ.探究
 溶液的性质。
溶液的性质。(1)预测
 具有氧化性,因此可以与Zn反应,此时Zn体现
具有氧化性,因此可以与Zn反应,此时Zn体现(2)预测
 具有还原性,预测依据是
具有还原性,预测依据是 溶液反应。
溶液反应。(3)进行如下实验操作:
 | 序号 | 操作 |
i | 滴加 | |
iii | 加入少量锌粉 | |
iii | 滴加酸性 |
 、
、②iii中的现象是
(4)某同学认为
 中现象并不能证明
中现象并不能证明 具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象,②为证实该反应中
具有还原性,他的理由有二:①将酸性高锰酸钾稀释也可能产生该现象,②为证实该反应中 确实被氧化,需要在反应后的溶液中加入试剂
确实被氧化,需要在反应后的溶液中加入试剂Ⅱ.探究
 溶液的性质。
溶液的性质。小组同学进行如下实验操作并观察到对应现象:
操作 |
|
|
|
现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色,而后红色褪去 |
(5)ⅳ中反应的离子方程式是
(6)vi中滴加氯水过程中,氯水反应的离子方程式是
Ⅲ.小组同学探究vi中褪色原因,提出两种假设:a.铁离子被转化,b.被转化。
(7)进一步预测
 可能被转化为
可能被转化为 ,通过实验验证了该预测,写出实验操作及现象
,通过实验验证了该预测,写出实验操作及现象
您最近一年使用:0次
名校
解题方法
10 . 某小组同学欧探究 的性质,经历如下探究过程:
的性质,经历如下探究过程:
预测: 中的O作为核心元素,化合价为-1价,因此预测
中的O作为核心元素,化合价为-1价,因此预测 既具有氧化性,也具有还原性。
既具有氧化性,也具有还原性。
(1)预测其具有氧化性的依据是___________ 。
实验和观察:小组同学分别选用酸性溶液、酸化的KI溶液与 溶液反应以验证预测。
溶液反应以验证预测。
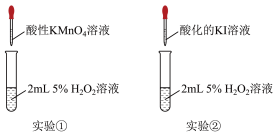
(2)实验①利用了酸性高锰酸钾的___________ 性质,该实验中,证明 溶液与
溶液与 反应的现象除了溶液颜色变浅或褪色外,还有
反应的现象除了溶液颜色变浅或褪色外,还有___________ 。
(3)实验②是为了验证 的氧化性,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式
的氧化性,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式___________ 。
(4)以上实验可得出的结论是___________ 。
(5)过氧化氢 俗称双氧水,根据下列A~D涉及
俗称双氧水,根据下列A~D涉及 的反应,填空。
的反应,填空。
A.
B.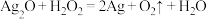
C.
D.
① 仅体现氧化性的反应是
仅体现氧化性的反应是___________ (填字母,下同)。
② 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是___________ 。
 的性质,经历如下探究过程:
的性质,经历如下探究过程:预测:
 中的O作为核心元素,化合价为-1价,因此预测
中的O作为核心元素,化合价为-1价,因此预测 既具有氧化性,也具有还原性。
既具有氧化性,也具有还原性。(1)预测其具有氧化性的依据是
实验和观察:小组同学分别选用酸性溶液、酸化的KI溶液与
 溶液反应以验证预测。
溶液反应以验证预测。
(2)实验①利用了酸性高锰酸钾的
 溶液与
溶液与 反应的现象除了溶液颜色变浅或褪色外,还有
反应的现象除了溶液颜色变浅或褪色外,还有(3)实验②是为了验证
 的氧化性,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式
的氧化性,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式(4)以上实验可得出的结论是
(5)过氧化氢
 俗称双氧水,根据下列A~D涉及
俗称双氧水,根据下列A~D涉及 的反应,填空。
的反应,填空。A.

B.
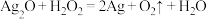
C.

D.

①
 仅体现氧化性的反应是
仅体现氧化性的反应是②
 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是
您最近一年使用:0次