1 . 利用废铝箔(主要成分为 ,含少量
,含少量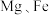 等)制明矾
等)制明矾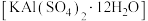 的一种工艺流程如下:
的一种工艺流程如下:
 ,含少量
,含少量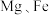 等)制明矾
等)制明矾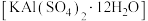 的一种工艺流程如下:
的一种工艺流程如下: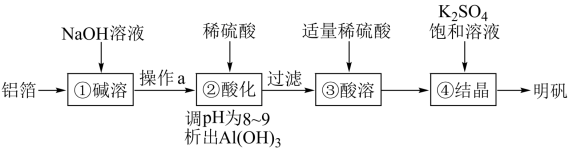
A.①中生成了 : :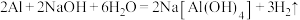 |
B.操作 是过滤,以除去难溶于 是过滤,以除去难溶于 溶液的杂质 溶液的杂质 |
| C.②③中加入稀硫酸的作用均是除去杂质 |
D.由④可知,室温下明矾的溶解度小于 和 和 的溶解度 的溶解度 |
您最近半年使用:0次
2 . 某主族元素的离子 的最外层电子排布式为
的最外层电子排布式为 ,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
 的最外层电子排布式为
的最外层电子排布式为 ,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是A. 具有强氧化性 具有强氧化性 | B.X的最高价氧化物具有强氧化性 |
| C.该元素是第IVA族元素 | D.X的常见化合价有 、 、 |
您最近半年使用:0次
3 . 探究硝酸银溶液对氯水漂白性的影响
资料:i.次氯酸盐具有一定的漂白性,但比HClO漂白性弱。
ii.相同条件下,还原性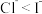 。
。
iii.溶解度较大的沉淀可以转化为溶解度较小的沉淀。
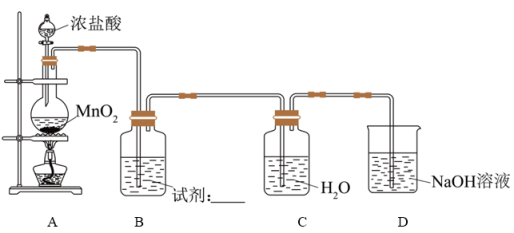
Ⅰ.氯水的制备装置如图所示:
(2)A中反应的离子方程式是___________ 。
(3)B中试剂是___________ 。
(4)结合离子方程式表示D中NaOH溶液的作用是___________ 。
Ⅱ.探究氯水与 溶液的反应
溶液的反应
(5)实验①的目的是排除稀释对品红褪色的影响,故试剂a是___________ 。
实验①的目的是排除稀释对品红褪色的影响,所以需要加入水实
(6)根据②中品红褪色慢的现象,推测发生复分解反应___________ (填化学方程式)生成AgClO沉淀,导致②中HClO减少,白色沉淀为AgCl和AgClO的混合物。
资料:i.次氯酸盐具有一定的漂白性,但比HClO漂白性弱。
ii.相同条件下,还原性
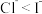 。
。iii.溶解度较大的沉淀可以转化为溶解度较小的沉淀。
Ⅰ.氯水的制备装置如图所示:
| A.新制氯水中还有三种分子、四种离子 |
| B.氯水颜色呈现出浅黄绿色 |
| C.取一滴久置氯水蘸在pH试纸上,pH试纸不变色 |
| D.取少量的新制氯水加入淀粉碘化钾溶液,观察到溶液变蓝 |
(2)A中反应的离子方程式是
(3)B中试剂是
(4)结合离子方程式表示D中NaOH溶液的作用是
Ⅱ.探究氯水与
 溶液的反应
溶液的反应| 序号 | 向1mL氯水中加入 | 现象 |
| ① | 试剂a+1滴品红 | 几秒后品红褪色 |
| ② | 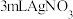 溶液+1滴品红 溶液+1滴品红 | 产生白色沉淀,几分钟后品红褪色 |
(5)实验①的目的是排除稀释对品红褪色的影响,故试剂a是
实验①的目的是排除稀释对品红褪色的影响,所以需要加入水实
(6)根据②中品红褪色慢的现象,推测发生复分解反应
您最近半年使用:0次
4 . 下列化学用语正确的是
A. 的结构式: 的结构式: |
B. 的电子式: 的电子式:  |
C. 的分子结构模型: 的分子结构模型: |
D. 溶于水电离: 溶于水电离: |
您最近半年使用:0次
解题方法
5 . 卤素单质的沸点与相对分子质量的关系如图所示,下列说法正确的是

A.①的最高价含氧酸为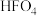 | B.常温下可用钢瓶贮存单质② |
C.单质③的 溶液呈紫红色 溶液呈紫红色 | D.单质④与 混合,在光照条件下,能剧烈反应 混合,在光照条件下,能剧烈反应 |
您最近半年使用:0次
名校
解题方法
6 . X、Y、Z均为元素周期表中前20号元素, Xb+、Yb-、Z(b+1)-三种简单离子的电子层结构相同,下列说法正确的是
| A.原子半径: Z>Y>X | B.离子半径:  |
C.气态氢化物的稳定性:  | D.Z(b+1) ⁻的还原性一定强于 Yb⁻ |
您最近半年使用:0次
名校
7 . 下列物质中属于电解质的是
| A.稀硫酸 | B.硫酸钡 | C.盐酸 | D.氨水 |
您最近半年使用:0次
名校
8 . 三氧化二铬 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化:
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。
(1)写出溶液B中的所有阳离子__________ 。写出步骤Ⅱ中生成气体C的离子方程式__________ 。沉淀E的化学式为__________ 。
(2)下列说法正确的是__________。
(3)在碱性条件下, 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式__________ 。根据该反应原理,设计实验检验上述反应后溶液中生成的阴离子__________ 。
 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化: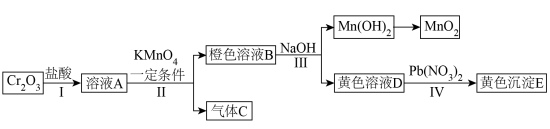
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数
 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。(1)写出溶液B中的所有阳离子
(2)下列说法正确的是__________。
| A.气体C在工业上可通过电解法制备 |
| B.在溶液B中加入乙醇,溶液变为绿色,再变为蓝色 |
| C.将步骤Ⅰ中的盐酸换成硫酸,仅影响步骤Ⅱ的反应 |
| D.在步骤Ⅲ中,溶液B加入纯碱溶液,也能分离出锰元素 |
(3)在碱性条件下,
 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式
您最近半年使用:0次
名校
解题方法
9 . A、B、C、D、E为原子序数依次增大的前20号主族元素,五种元素中仅A、C同主族,B、C、D位于同一周期,元素B在同周期中金属性最强,元素C的最外层电子数为最内层的3倍。下列说法正确的是
A.化学键中离子键成分的百分数: |
| B.简单离子半径:E>C>D |
C.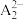 和 和 离子的结构与化学性质均相似 离子的结构与化学性质均相似 |
D.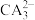 与 与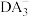 离子空间结构均为平面三角形 离子空间结构均为平面三角形 |
您最近半年使用:0次
名校
10 . 溶液中可以大量共存的离子组合是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近半年使用:0次



