名校
解题方法
1 . 下列反应的离子方程式书写正确的是
A.碘化亚铁溶液中通入足量的氯气: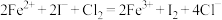 |
B.加碘盐与药物碘化钾片尽量不要同时服用: |
C.向 溶液中加入过量的NaOH溶液: 溶液中加入过量的NaOH溶液: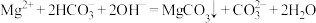 |
D.向 溶液中滴入 溶液中滴入 使 使 反应完全: 反应完全: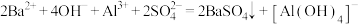 |
您最近半年使用:0次
今日更新
|
601次组卷
|
3卷引用:湖南省“一起考”大联考2023-2024学年高三下学期3月模拟考试(模拟一)化学试题
湖南省“一起考”大联考2023-2024学年高三下学期3月模拟考试(模拟一)化学试题江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 (已下线)题型4 离子反应 氧化还原反应(25题)-2024年高考化学常考点必杀300题(新高考通用)
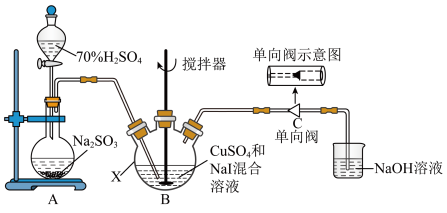
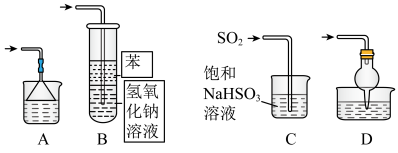
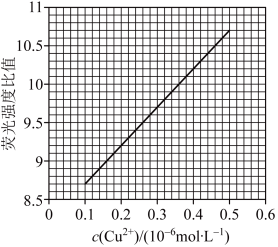
2 . 碘化亚铜(CuI)可用作有机合成催化剂,是一种白色粉末,不溶于水,在空气中相对稳定。实验室制备碘化亚铜的装置如图(部分夹持及加热装置已略去):
I.取50.0gCuSO4∙5H2O、80.0gNaI于仪器B中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
II.打开分液漏斗,将产生的SO2通向黄色沉淀,充分反应后得到白色沉淀;
III.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
IV.测定产品中CuI的纯度。
回答下列问题:
(1)在使用分液漏斗组装发生装置之前必需进行的操作是_______ 。
(2)已知步骤I中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为_______ 。
(3)步骤II通入SO2的主要目的是_______ 。写出通入SO2所发生的离子方程式_______ 。
(4)下图中能起到与单向阀C相同作用的是_______ 。(下图容器中未标注的液体均为氢氧化钠溶液)_______ %(保留一位小数),据此推算CuI的产率接近于_______ (填标号)。
I.取50.0gCuSO4∙5H2O、80.0gNaI于仪器B中,加入适量蒸馏水溶解,搅拌,得到黄色沉淀;
II.打开分液漏斗,将产生的SO2通向黄色沉淀,充分反应后得到白色沉淀;
III.将分离出的白色沉淀经过“系列操作”得到19.1g产品;
IV.测定产品中CuI的纯度。
回答下列问题:
(1)在使用分液漏斗组装发生装置之前必需进行的操作是
(2)已知步骤I中的黄色沉淀含CuI和一种单质,制备CuI的化学方程式为
(3)步骤II通入SO2的主要目的是
(4)下图中能起到与单向阀C相同作用的是
您最近半年使用:0次
3 . 某兴趣小组探究高锰酸钾和氨水的反应,实验如下:
注:实验中c(KMnO4) = 0.01 mol·L-1。
下列说法不正确 的是
| 序号 | 试剂 | 实验现象 |
| ① | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水+0.5 mL蒸馏水 | 溶液完全褪色所需时间:③<②<①。实验均产生棕褐色固体(经检验为MnO2),都伴有少量气泡产生(经检验为N2)。 |
| ② | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水 + 0.5 mL 1 mol·L-1稀硫酸 | |
| ③ | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水 + 0.5 mL 1 mol·L-1 Na2SO4溶液 | |
| ④ | 2 mL KMnO4溶液 + 1 mL 5 mol·L-1 (NH4)2SO4溶液 + 0.5 mL蒸馏水 | 无明显变化 |
下列说法
A.实验①中发生了反应2 MnO + 2NH3 = 2MnO2 + N2↑ + 2OH- + 2H2O + 2NH3 = 2MnO2 + N2↑ + 2OH- + 2H2O |
B.溶液完全褪色所需时间② < ①的主要原因:c(H+)增大,MnO 的氧化性增强 的氧化性增强 |
C.对比实验③④可得出,还原性:NH3 > NH |
| D.在实验④的试剂中,逐滴加入浓NaOH溶液,可观察到溶液褪色 |
您最近半年使用:0次
4 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
(1)盛放浓盐酸的仪器名称是___________ ,a的作用为___________ 。
(2)d中可选用试剂___________(填字母)。
(3)浓盐酸与二氧化锰反应的离子方程式是___________ 。
(4)b中采用的加热方式是___________ ,化学反应的离子方程式是___________ 。
(5)c中采用冰水浴冷却的目的是___________ 。
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显___________ 色。可知该条件下KClO3的氧化能力___________ (填“大于”或“小于”)NaClO。
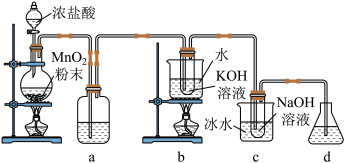
(1)盛放浓盐酸的仪器名称是
(2)d中可选用试剂___________(填字母)。
| A.Na2S | B.NaCl | C.Ca(OH)2 | D.H2SO4 |
(3)浓盐酸与二氧化锰反应的离子方程式是
(4)b中采用的加热方式是
(5)c中采用冰水浴冷却的目的是
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显
您最近半年使用:0次
5 . 下列有关物质的性质与用途不具有对应关系的是
| A.干冰升华时吸热,可用作人工降雨 |
B. 吸收 吸收 产生 产生 ,可用作呼吸面具供氧剂 ,可用作呼吸面具供氧剂 |
C. 溶液显酸性,可蚀刻印刷电路板上的Cu 溶液显酸性,可蚀刻印刷电路板上的Cu |
D. 固体受热分解产生 固体受热分解产生 ,可用作膨松剂 ,可用作膨松剂 |
您最近半年使用:0次
解题方法
6 . 随着科学技术的发展,锂电池已经成为了主流。某电解质阴离子(如下图)在锂电工业中广泛应用,其组成元素X、Y、Z、R、W均为短周期主族元素,原子序数依次增大且X、Y、Z、R位于同周期。下列叙述不正确的是
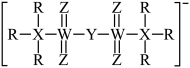
| A.简单氢化物的沸点:Z>Y>X |
| B.气态氢化物稳定性:R>Z>W |
| C.WF4、WF6分子中每个原子都达到8电子结构 |
| D.最高价氧化物对应的水化物酸性:Y>X |
您最近半年使用:0次
解题方法
7 . 古代技术是古人智慧的结晶,下列古代技术应用中不涉及化学变化的是
| A.用粮食酿造白酒 | B.用黏土烧制陶瓷 |
| C.用青铜铸制食具 | D.用炉甘石炼锌 |
您最近半年使用:0次
8 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.将0.2 mol  水解制成胶体,所得胶体粒子数为 水解制成胶体,所得胶体粒子数为 |
B.2.3 g Na与氧气完全反应,反应中转移的电子数介于 到 到 之间 之间 |
C.标准状况下, 完全燃烧后生成的 完全燃烧后生成的 分子个数约为 分子个数约为 |
D.8.0 g  和CuO的混合物中含有铜原子数为 和CuO的混合物中含有铜原子数为 |
您最近半年使用:0次
9 . 工业上用S8(分子结构: )CH4为原料制备CS2,发生反应:
)CH4为原料制备CS2,发生反应: ,
, 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
A.1molH2S中含有的孤电子对数为 |
B.生成17gH2S,转移的电子数为 |
C.消耗1molS8,断裂的S-S键数目为 |
D.22.4LCH4中含有的电子数为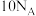 |
您最近半年使用:0次
名校
10 . “马氏试砷法”原理中的“砷镜”可溶于 的碱性溶液,发生的反应为
的碱性溶液,发生的反应为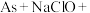
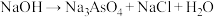 (末配平)。下列说法正确的是
(末配平)。下列说法正确的是
 的碱性溶液,发生的反应为
的碱性溶液,发生的反应为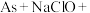
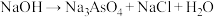 (末配平)。下列说法正确的是
(末配平)。下列说法正确的是A.配平后 的化学计量数为5 的化学计量数为5 |
| B.该反应的氧化剂与还原剂的物质的量之比为5:2 |
C. 的电子式为 的电子式为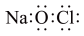 |
D.该反应每生成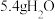 ,转移 ,转移 电子 电子 |
您最近半年使用:0次



