名校
1 . X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素,周期表的全部元素中X的原子半径最小,X与R的最外层电子数相等;Z的内层电子数是最外层电子数的一半,U的最高化合价和最低化合价的代数和为6;R和Q可形成原子数之比为 和
和 的两种化合物:R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。
的两种化合物:R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。
请回答下列问题:
(1)Z元素在元素周期表中的位置是_____ ;由上述元素中的四种元素形成的既含有离子键又含有共价键的化合物为_____ (写出其中一种物质的名称)。
(2)Q、R、T三种元素的简单离子半径由小到大顺序为_____ (用离子符号表示)。
(3)T与R二者的最高价氧化物对应的水化物反应的化学方程式为_____ 。T与U二者的最高价氧化物对应的水化物反应的离子方程式为_____ 。
(4)下列可以判断R和T金属性强弱的是_____(填序号)。
(5)Q、R两元素可形成离子化合物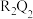 ,
,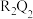 的电子式为
的电子式为_____ ;用电子式表示化合物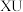 的形成过程
的形成过程_____ 。
 和
和 的两种化合物:R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。
的两种化合物:R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。请回答下列问题:
(1)Z元素在元素周期表中的位置是
(2)Q、R、T三种元素的简单离子半径由小到大顺序为
(3)T与R二者的最高价氧化物对应的水化物反应的化学方程式为
(4)下列可以判断R和T金属性强弱的是_____(填序号)。
| A.单质的熔点R比T低 |
| B.单质与酸反应时,失电子数R比T少 |
| C.单质与水反应R比T剧烈 |
| D.最高价氧化物的水化物的碱性R比T强 |
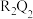 ,
,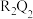 的电子式为
的电子式为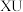 的形成过程
的形成过程
您最近半年使用:0次
名校
解题方法
2 . 下列关于元素周期表和元素周期律的说法正确的是
①每一周期都从碱金属元素开始,最后以稀有气体元素结束
②最外层电子数为2的元素不一定是金属元素
③元素周期表有7个横行,即7个周期,16个纵列,即16个族
④元素周期表中第10列没有非金属元素
⑤Ⅷ族是容纳元素最多的族
⑥同周期第IIA族和第IIIA族元素的原子序数之差为1
⑦ 是半导体材料,
是半导体材料, 也是半导体材料,推测该族元素的单质都是半导体材料
也是半导体材料,推测该族元素的单质都是半导体材料
⑧根据元素周期表中“对角线规则”推测 既能与盐酸反应又能与
既能与盐酸反应又能与 溶液反应
溶液反应
①每一周期都从碱金属元素开始,最后以稀有气体元素结束
②最外层电子数为2的元素不一定是金属元素
③元素周期表有7个横行,即7个周期,16个纵列,即16个族
④元素周期表中第10列没有非金属元素
⑤Ⅷ族是容纳元素最多的族
⑥同周期第IIA族和第IIIA族元素的原子序数之差为1
⑦
 是半导体材料,
是半导体材料, 也是半导体材料,推测该族元素的单质都是半导体材料
也是半导体材料,推测该族元素的单质都是半导体材料⑧根据元素周期表中“对角线规则”推测
 既能与盐酸反应又能与
既能与盐酸反应又能与 溶液反应
溶液反应| A.①②④⑧ | B.②③⑤ | C.②⑥⑦ | D.②④⑧ |
您最近半年使用:0次
名校
3 . W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层电子数与其K层电子数相等,WX2是形成酸雨的物质之一,下列说法正确的是
| A.原子半径:X>W | B.Z的含氧酸是强酸 |
| C.YX对应的水化物具有两性 | D.原子的得电子能力:X>Z |
您最近半年使用:0次
名校
解题方法
4 . 下列有关说法或各组性质的比较中,正确的有几项
①通过反应 ,可以证明非金属性的强弱:
,可以证明非金属性的强弱:
 在熔融状态下不仅破坏了离子键,还破坏了共价键
在熔融状态下不仅破坏了离子键,还破坏了共价键
④沸点: ⑤离子还原性:
⑤离子还原性: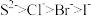
⑥酸性: ⑦金属性:
⑦金属性: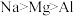
⑧气态氢化物稳定性:
①通过反应
 ,可以证明非金属性的强弱:
,可以证明非金属性的强弱:
② 的电子式可表示为
的电子式可表示为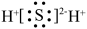
 在熔融状态下不仅破坏了离子键,还破坏了共价键
在熔融状态下不仅破坏了离子键,还破坏了共价键④沸点:
 ⑤离子还原性:
⑤离子还原性: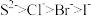
⑥酸性:
 ⑦金属性:
⑦金属性: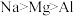
⑧气态氢化物稳定性:

| A.2 | B.3 | C.4 | D.5 |
您最近半年使用:0次
名校
5 . 某汽车安全气囊的气体发生剂主要含有 等物质,汽车发生碰撞时,会产生大量气体使气囊迅速膨胀。下列说法不正确的是
等物质,汽车发生碰撞时,会产生大量气体使气囊迅速膨胀。下列说法不正确的是
 等物质,汽车发生碰撞时,会产生大量气体使气囊迅速膨胀。下列说法不正确的是
等物质,汽车发生碰撞时,会产生大量气体使气囊迅速膨胀。下列说法不正确的是A. 是气体发生剂,受热分解产生 是气体发生剂,受热分解产生 和 和 |
B. 因吸收产气过程中释放的热量而分解 因吸收产气过程中释放的热量而分解 |
C. 是助氧剂,在反应过程中生成的 是助氧剂,在反应过程中生成的 属于离子化合物 属于离子化合物 |
D.在 与 与 的反应中, 的反应中, 作为还原剂被还原成较为安全的 作为还原剂被还原成较为安全的 |
您最近半年使用:0次
名校
解题方法
6 . NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.标准状况下,11.2L氖气中所含电子数为0.5NA |
B.32g环状S8( )分子中含有的 )分子中含有的 键的数目为NA 键的数目为NA |
C.常温常压下,3.6gD2O与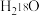 组成的体系中含有中子数2NA 组成的体系中含有中子数2NA |
D.某电池的总反应为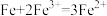 ,当有5.6gFe溶解时电路中有0.3NA电子通过 ,当有5.6gFe溶解时电路中有0.3NA电子通过 |
您最近半年使用:0次
名校
解题方法
7 . 下列物质中,只含共价键的是
A. | B. | C. | D. |
您最近半年使用:0次
解题方法
8 . 在一定条件下,不能由两种单质直接化合而生成的化合物是
| A.SO3 | B.Na2O2 | C.FeCl3 | D.Na2O |
您最近半年使用:0次
解题方法
9 . 用NA表示阿伏伽德罗常数的值。下列判断正确的是
| A.1molH2含有的原子数目为NA |
| B.常温常压下,11.2LO2中含有的原子数目为NA |
| C.1L1mol·L-1CaCl2溶液中含有的Cl-离子数目为2NA |
| D.5.6gFe与足量的稀硫酸反应,转移电子的数目为0.3NA |
您最近半年使用:0次
解题方法
10 . CO(g)+H2O(g) CO2(g)+H2(g),关于该反应的说法正确的是
CO2(g)+H2(g),关于该反应的说法正确的是
 CO2(g)+H2(g),关于该反应的说法正确的是
CO2(g)+H2(g),关于该反应的说法正确的是| A.CO发生还原反应 | B.H2O得电子 |
| C.CO2是还原产物 | D.生成2.24LH2转移0.2mole- |
您最近半年使用:0次



