名校
1 . 氯及其化合物应用广泛。氯的单质 可由
可由 与浓盐酸反应制得。氯的氧化物
与浓盐酸反应制得。氯的氧化物 可用于自来水消毒,
可用于自来水消毒, 是一种黄绿色气体,易溶于水,与碱反应会生成
是一种黄绿色气体,易溶于水,与碱反应会生成 与
与 ,在稀硫酸和
,在稀硫酸和 的混合溶液中通入
的混合溶液中通入 气体可制得
气体可制得 。新制氯水可将
。新制氯水可将 氧化为
氧化为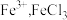 溶液可用于刻蚀覆铜板。下列反应的离子方程式表示不正确的是
溶液可用于刻蚀覆铜板。下列反应的离子方程式表示不正确的是
 可由
可由 与浓盐酸反应制得。氯的氧化物
与浓盐酸反应制得。氯的氧化物 可用于自来水消毒,
可用于自来水消毒, 是一种黄绿色气体,易溶于水,与碱反应会生成
是一种黄绿色气体,易溶于水,与碱反应会生成 与
与 ,在稀硫酸和
,在稀硫酸和 的混合溶液中通入
的混合溶液中通入 气体可制得
气体可制得 。新制氯水可将
。新制氯水可将 氧化为
氧化为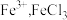 溶液可用于刻蚀覆铜板。下列反应的离子方程式表示不正确的是
溶液可用于刻蚀覆铜板。下列反应的离子方程式表示不正确的是A.用 制 制 |
B. 与碱反应: 与碱反应: |
C.制取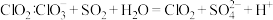 |
D.新制氯水氧化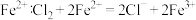 |
您最近半年使用:0次
名校
2 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温常压下,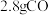 和 和 混合气体中含有的原子数为 混合气体中含有的原子数为 |
B.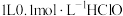 溶液中含有的 溶液中含有的 离子数为 离子数为 |
C. 中含有的质子数为 中含有的质子数为 |
D. 和足量 和足量 反应,转移的电子数为 反应,转移的电子数为 |
您最近半年使用:0次
名校
解题方法
3 . 室温下,下列各组离子在指定溶液中能大量共存的是
A.澄清透明的溶液: 、CO 、CO |
B.强碱性溶液: |
C. 溶液: 溶液: |
D.与铁反应放出氢气的溶液: |
您最近半年使用:0次
名校
解题方法
4 . 反应 可用于氯气管道的检漏。下列说法正确的是
可用于氯气管道的检漏。下列说法正确的是
 可用于氯气管道的检漏。下列说法正确的是
可用于氯气管道的检漏。下列说法正确的是A.中子数为20的氯原子: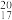 Cl Cl | B. 分子的结构式是N=N 分子的结构式是N=N |
C. 分子的电子式是 分子的电子式是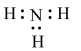 | D.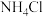 中既含有离子键又含有共价键 中既含有离子键又含有共价键 |
您最近半年使用:0次
名校
5 . 化学与生活、科技、社会发展息息相关。下列说法正确的是
A.碳纳米材料中,碳纳米管和 互为同位素 互为同位素 |
| B.用于火箭发动机的碳化硅陶瓷是一种新型无机非金属材料 |
C.华为新上市手机的芯片材料是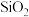 |
D.“北斗卫星”授时系统的“星载铷钟”含铷元素,其单质遇水能极其缓慢地反应放出 |
您最近半年使用:0次
名校
解题方法
6 . 如图是无机物 在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体,
在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体, 都含有相同的元素。
都含有相同的元素。
(1)写出反应①的化学方程式:_______ 。
(2)在①②③④中属于氮的固定的是_______ (填序号)。
(3)下列说法正确的是_______(填字母)。
(4) 易溶于水。已知某温度压强下
易溶于水。已知某温度压强下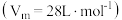 ,将体积为
,将体积为 的试管充满
的试管充满 后倒扣在水中。
后倒扣在水中。
①最终试管中所得 的物质的量浓度为(不考虑
的物质的量浓度为(不考虑 的扩散)
的扩散)_______  。
。
②若 按物质的量之比
按物质的量之比 被
被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是_______ 。为提高吸收速率与效率,最好选用_______ 装置(填字母)。 制取
制取 ,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗
,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗 的
的 制取
制取 ,在该过程中至少消耗的
,在该过程中至少消耗的 的物质的量为
的物质的量为_______  。
。
(6)实验室里检验 中阳离子的方法是
中阳离子的方法是_______ 。
 在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体,
在一定条件下的转化关系(部分产物及反应条件未标出)。已知:常温下A为气体, 都含有相同的元素。
都含有相同的元素。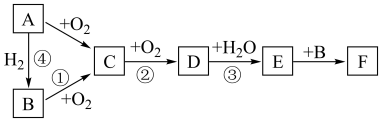
(1)写出反应①的化学方程式:
(2)在①②③④中属于氮的固定的是
(3)下列说法正确的是_______(填字母)。
A.通过水可以除去 中含有的少量D 中含有的少量D |
B.物质 均可以用向上排空气法收集 均可以用向上排空气法收集 |
C. 的浓溶液的存放方法是保存在无色细口玻璃瓶 的浓溶液的存放方法是保存在无色细口玻璃瓶 |
D.物质 中只含离子键 中只含离子键 |
(4)
 易溶于水。已知某温度压强下
易溶于水。已知某温度压强下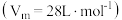 ,将体积为
,将体积为 的试管充满
的试管充满 后倒扣在水中。
后倒扣在水中。①最终试管中所得
 的物质的量浓度为(不考虑
的物质的量浓度为(不考虑 的扩散)
的扩散) 。
。②若
 按物质的量之比
按物质的量之比 被
被 溶液吸收,只生成一种盐,则该反应的离子方程式是
溶液吸收,只生成一种盐,则该反应的离子方程式是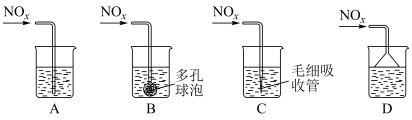
 制取
制取 ,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗
,为了提高原料的利用率并尽量减轻对环境的污染,C须循环使用。若消耗 的
的 制取
制取 ,在该过程中至少消耗的
,在该过程中至少消耗的 的物质的量为
的物质的量为 。
。(6)实验室里检验
 中阳离子的方法是
中阳离子的方法是
您最近半年使用:0次
名校
7 . 某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和 ,
,
①浓盐酸与 混合加热生成氯气的离子方程式为
混合加热生成氯气的离子方程式为______ ;
②电极反应式:
ⅰ.还原反应:
ⅱ.氧化反应:____________ 。
③根据电极反应式,分析A中仍存在盐酸和 的原因。
的原因。
ⅰ.随 降低或
降低或 升高,
升高, 氧化性减弱。
氧化性减弱。
ⅱ.随 降低,
降低,____________ 。
④补充实验证实了③中的分析。
a是______ ,b是______ 。
(2)利用 对
对 氧化性的影响,探究卤素离子的还原性。
氧化性的影响,探究卤素离子的还原性。
相同浓度的KCl、KBr和KI溶液,能与 反应所需的最低
反应所需的最低 由大到小的顺序是
由大到小的顺序是____________ ,从原子结构角度说明理由____________ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将 氧化为
氧化为 。经实验证实了推测。该化合物是
。经实验证实了推测。该化合物是____________ 。
(4)总结:物质氧化性和还原性变化的一般规律是____________ 。
(1)浓盐酸与
 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和 ,
,①浓盐酸与
 混合加热生成氯气的离子方程式为
混合加热生成氯气的离子方程式为②电极反应式:
ⅰ.还原反应:

ⅱ.氧化反应:
③根据电极反应式,分析A中仍存在盐酸和
 的原因。
的原因。ⅰ.随
 降低或
降低或 升高,
升高, 氧化性减弱。
氧化性减弱。ⅱ.随
 降低,
降低,④补充实验证实了③中的分析。
序号 | 实验 | 加入试剂 | 现象 |
Ⅰ |
| 较浓硫酸 | 有氯气 |
Ⅱ | a | 有氯气 | |
III | a和b | 无氯气 |
(2)利用
 对
对 氧化性的影响,探究卤素离子的还原性。
氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与
 反应所需的最低
反应所需的最低 由大到小的顺序是
由大到小的顺序是(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将
 氧化为
氧化为 。经实验证实了推测。该化合物是
。经实验证实了推测。该化合物是(4)总结:物质氧化性和还原性变化的一般规律是
您最近半年使用:0次
名校
解题方法
8 . X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子K层和L层电子数之比为1∶2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,R的一种氧化物能使品红溶液褪色,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)X的最高价氧化物的电子式为______ ;
(2)X、Y、Z、W的原子半径由大到小的顺序:____________ (用元素符号表示)。
(3)元素W在周期表的位置______ ,其最高价氧化物对应水化物与R的最高价氧化物对应水化物(酸性或碱性)强弱是______ (用化学式表示)。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做其吸收剂,写出吸收剂与足量该氧化物反应的离子方程式____________ 。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1∶3,则该反应的化学方程式为____________ 。
(1)X的最高价氧化物的电子式为
(2)X、Y、Z、W的原子半径由大到小的顺序:
(3)元素W在周期表的位置
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做其吸收剂,写出吸收剂与足量该氧化物反应的离子方程式
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1∶3,则该反应的化学方程式为
您最近半年使用:0次
名校
9 . 有下列物质:① ②
② ③
③ ④NaOH⑤
④NaOH⑤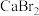 ⑥
⑥ 请回答下列问题:
请回答下列问题:
(1)只含有离子键的化合物有______ (填序号,下同):
(2)既含有极性键又含有非极性键的共价化合物有______ ;
 ②
② ③
③ ④NaOH⑤
④NaOH⑤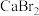 ⑥
⑥ 请回答下列问题:
请回答下列问题:(1)只含有离子键的化合物有
(2)既含有极性键又含有非极性键的共价化合物有
您最近半年使用:0次
名校
10 . 下列化学用语不正确的是
A. 的电子式: 的电子式: |
B.S的原子结构示意图: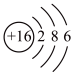 |
C.KOH的电离方程式: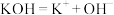 |
D.用电子式表示HCl的形成过程: |
您最近半年使用:0次




