名校
1 . 一节1号干电池可以让1平方米土地上的庄稼颗粒无收,回收电池既可以防止污染又可以变废为宝。废旧锌锰干电池内部的黑色物质A主要含有 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:________ (填化学式)。
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为 ,另一个是
,另一个是________ 。灼烧时,MnOOH与空气中的氧气反应的化学方程式为________________ 。
(3)第III步中为提高反应速率,可以采取的措施有________ (任写一条)。
(4)已知: 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为________________ ;
②操作VI中需要的玻璃仪器有________ ;
③你认为操作VII中检测的方法及现象是________ 时可继续进行操作VIII;
④操作VIII中用无水乙醇洗涤的目的是________ 。
 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为
 ,另一个是
,另一个是(3)第III步中为提高反应速率,可以采取的措施有
(4)已知:
 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: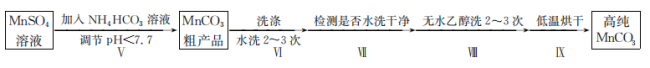
 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为②操作VI中需要的玻璃仪器有
③你认为操作VII中检测的方法及现象是
④操作VIII中用无水乙醇洗涤的目的是
您最近半年使用:0次
名校
2 . 下列实验“操作和现象”与“结论”对应关系正确的是
操作 | 现象 | 结论 | |
A. | 向NaBr溶液中滴入少量氯水和苯,振荡、静置 | 溶液上层呈橙色 | 还原性: |
B. | 将氯气缓缓通入到紫色的石蕊溶液中 | 石蕊溶液先变红后褪色 | 氯气与水反应生成了酸性物质和漂白性物质 |
C. | 将装满氯水的圆底烧瓶倒置在盛有水的水槽中,日光照射 | 烧瓶内有气泡生成 | 日光照射时,逸出的气体只可能是 |
D. | 分别加热 和 和 固体 固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 .  能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备
能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备 的原理为
的原理为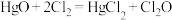 ,装置如图所示。
,装置如图所示。 的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;②
的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;② 与有机物、还原剂接触或加热时会发生燃烧并爆炸。
与有机物、还原剂接触或加热时会发生燃烧并爆炸。
下列说法中正确的是
 能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备
能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备 的原理为
的原理为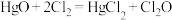 ,装置如图所示。
,装置如图所示。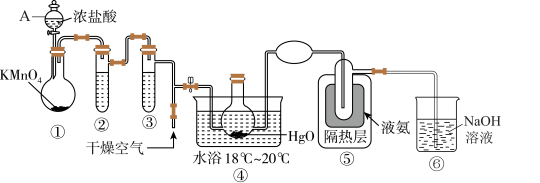
 的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;②
的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;② 与有机物、还原剂接触或加热时会发生燃烧并爆炸。
与有机物、还原剂接触或加热时会发生燃烧并爆炸。下列说法中正确的是
A.装置②中盛装的试剂是浓硫酸,用来干燥 |
| B.装置④与⑤之间可用橡胶管连接 |
C. 易液化,装置⑤中的液氨只能冷凝 易液化,装置⑤中的液氨只能冷凝 ,因此从装置⑤中逸出气体的主要成分是 ,因此从装置⑤中逸出气体的主要成分是 |
D.通入干燥空气的目的是将生成的 稀释,减小爆炸危险 稀释,减小爆炸危险 |
您最近半年使用:0次
名校
解题方法
4 . 下列各组离子或分子在给定条件的溶液中可能大量共存的是
A.加入铝片有大量氢气产生的溶液中: 、 、 、 、 、 、 |
B.在0.1mol/L的盐酸中: 、 、 、 、 、 、 |
C.在强碱性溶液中: 、 、 、 、 、 、 |
D.碱性无色溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
名校
5 . NA代表阿伏加德罗常数的值,以下说法正确的是
| A.将足量Zn与100mL18mol/L浓硫酸反应,生成224mL气体,转移电子为0.02NA |
| B.在标准状况下,22.4LHF所含的原子总数为2NA |
C.1mol 固体中含离子总数与1mol 固体中含离子总数与1mol 固体中含离子总数之比为 固体中含离子总数之比为 |
D.1mol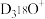 (其中D代表重氢原子符号)中含有的中子数为10NA (其中D代表重氢原子符号)中含有的中子数为10NA |
您最近半年使用:0次
名校
解题方法
6 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 的硫酸溶液中,含氢离子数目为 的硫酸溶液中,含氢离子数目为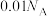 |
B.在常温常压下,11.2LCO2分子中含氧原子数目小于 |
C.21g 分子中含σ键数目一定是 分子中含σ键数目一定是 |
D.在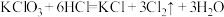 中,每生成3mol 中,每生成3mol ,转移的电子数为 ,转移的电子数为 |
您最近半年使用:0次
7 . 利用废铝箔(主要成分为 ,含少量
,含少量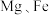 等)制明矾
等)制明矾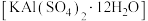 的一种工艺流程如下:
的一种工艺流程如下:
 ,含少量
,含少量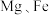 等)制明矾
等)制明矾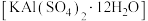 的一种工艺流程如下:
的一种工艺流程如下: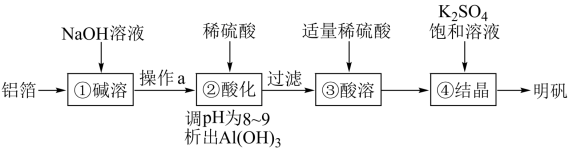
A.①中生成了 : :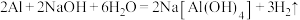 |
B.操作 是过滤,以除去难溶于 是过滤,以除去难溶于 溶液的杂质 溶液的杂质 |
| C.②③中加入稀硫酸的作用均是除去杂质 |
D.由④可知,室温下明矾的溶解度小于 和 和 的溶解度 的溶解度 |
您最近半年使用:0次
解题方法
8 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液;②H2O2(在水中一部分可以电离出阴、阳离子);③ClO2;④O3;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号),“84”消毒液中有效成分的电离方程式为___________ ,双氧水的电子式为___________ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”),若1 mol NaClO参加反应,转移电子数___________ (阿伏加德罗常数为NA)。
②若混合使用“洁厕灵”(主要成分为盐酸)与“84”消毒液会产生氯气。原因是(用离子方程式表示)___________ 。
(3)ClO2在杀菌消毒过程中会产生亚氯酸盐(ClO ),需将其转化为Cl− 除去,下列试剂可将ClO
),需将其转化为Cl− 除去,下列试剂可将ClO 转化为Cl− 的是
转化为Cl− 的是___________ (填标号)。
a.FeSO4 b.O3 c.KMnO4 d.Na2CO3
(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
②若混合使用“洁厕灵”(主要成分为盐酸)与“84”消毒液会产生氯气。原因是(用离子方程式表示)
(3)ClO2在杀菌消毒过程中会产生亚氯酸盐(ClO
 ),需将其转化为Cl− 除去,下列试剂可将ClO
),需将其转化为Cl− 除去,下列试剂可将ClO 转化为Cl− 的是
转化为Cl− 的是a.FeSO4 b.O3 c.KMnO4 d.Na2CO3
您最近半年使用:0次
9 . 某主族元素的离子 的最外层电子排布式为
的最外层电子排布式为 ,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
 的最外层电子排布式为
的最外层电子排布式为 ,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是A. 具有强氧化性 具有强氧化性 | B.X的最高价氧化物具有强氧化性 |
| C.该元素是第IVA族元素 | D.X的常见化合价有 、 、 |
您最近半年使用:0次
解题方法
10 . 铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为_______ ,发生反应的离子方程式为_______ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是_______ 。
(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为_______ 。
(4)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:_______ 。
② 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为_______ 。
③滤液II中溶质的用途之一是_______ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为
(4)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:
②
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为③滤液II中溶质的用途之一是
您最近半年使用:0次



