1 . 短周期元素A、B、C、D的原子序数依次增大,A元素原子的核外电子只有一种运动状态:基态B原子s能级的电子总数比p能级的多1;基态C原子中成对电子数是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题
(1)B原子的轨道表示式___________ 。
(2)A和C原子个数比为1∶1的化合物的电子式___________ 。
(3)元素A、B、C中,第一电离能最大的是___________ (填元素名称)。
(4)在B、C、D三种元素的简单离子中,其离子的半径最小的是___________ 。(填离子符号)
(5)C的简单氢化物的键角小于B的简单氢化物,其原因是___________ 。
(6)BC₃的空间结构为___________ 。
(7)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB晶体的密度为a g⋅cm ,则晶体中两个最近D原子之间的距离为
,则晶体中两个最近D原子之间的距离为___________ pm(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
(1)B原子的轨道表示式
(2)A和C原子个数比为1∶1的化合物的电子式
(3)元素A、B、C中,第一电离能最大的是
(4)在B、C、D三种元素的简单离子中,其离子的半径最小的是
(5)C的简单氢化物的键角小于B的简单氢化物,其原因是
(6)BC₃的空间结构为
(7)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB晶体的密度为a g⋅cm
 ,则晶体中两个最近D原子之间的距离为
,则晶体中两个最近D原子之间的距离为 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。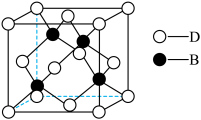
您最近半年使用:0次
2 . 实验室用废铁屑制取无水氯化铁并测其纯度。实验方案如下:
Ⅰ. 制备
制备
①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是_______ 。
(2)控制温度在40~50℃的原因是_______ 。
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为_______ 。
Ⅱ.无水 制备
制备
已知 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。
(4)按图装置进行实验。锥形瓶中生成无水 的总化学方程式为
的总化学方程式为_______ ;仪器A的作用是_______ 。
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用 溶液滴定(
溶液滴定(
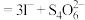 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。
①所制产品的纯度为_______ (以无水 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);
②所制产品中可能含有 杂质,检验
杂质,检验 的试剂为
的试剂为_______ (填化学式)溶液;产生 的原因可能是
的原因可能是_______ 。
Ⅰ.
 制备
制备①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是
(2)控制温度在40~50℃的原因是
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为
Ⅱ.无水
 制备
制备已知
 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。(4)按图装置进行实验。锥形瓶中生成无水
 的总化学方程式为
的总化学方程式为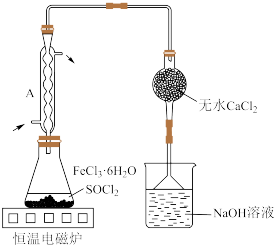
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用
 溶液滴定(
溶液滴定(
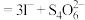 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。①所制产品的纯度为
 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);②所制产品中可能含有
 杂质,检验
杂质,检验 的试剂为
的试剂为 的原因可能是
的原因可能是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 探究pH对 溶液的配制和保存的影响。
溶液的配制和保存的影响。
I. 溶液的配制
溶液的配制
将 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
II. 溶液的保存
溶液的保存
将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
(1)①中的浑浊主要是FeOOH,用离子方程式表示其生成过程_______ 。
(2)该实验的初步结论:保存 溶液的最佳pH是
溶液的最佳pH是_______ 。
(3)进一步探究pH对 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;
ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因_______ 。
b.依据实验i和ii推断:③比②中 更易变质的原因是
更易变质的原因是_______ 。
c.按上述原理进行实验,证实①中 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,_______ 。
 溶液的配制和保存的影响。
溶液的配制和保存的影响。I.
 溶液的配制
溶液的配制将
 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:| 编号 | 溶剂 | 溶液性状 | |
| ① | 蒸馏水 | 浅黄色澄清溶液 |  ;滴加1mol/LKSCN溶液无明显变化 ;滴加1mol/LKSCN溶液无明显变化 |
| ② |  | 无色澄清溶液 |  ;滴加1mol/LKSCN溶液微微变红 ;滴加1mol/LKSCN溶液微微变红 |
| ③ |  | 无色澄清溶液 | 滴加1mol/LKSCN溶液微微变红 |
 溶液的保存
溶液的保存将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
| 编号 | 溶液性状 | |
| ① | 橙色浑浊 | 用 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 |
| ② | 无色溶液 | 滴加1mol/L的KSCN溶液后显浅红色 |
| ③ | 无色溶液 | 滴加1mol/L的KSCN溶液后显红色,颜色比②略深 |
(2)该实验的初步结论:保存
 溶液的最佳pH是
溶液的最佳pH是(3)进一步探究pH对
 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: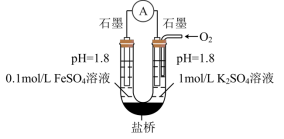
 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因
b.依据实验i和ii推断:③比②中
 更易变质的原因是
更易变质的原因是c.按上述原理进行实验,证实①中
 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
您最近半年使用:0次
名校
4 . 1986年,化学家用化学法制氟,其原理如下:
① (未配平);
(未配平);
② ;
;
③ 。
。
下列说法正确的是
①
 (未配平);
(未配平);②
 ;
;③
 。
。下列说法正确的是
| A.①中氧化产物和还原产物的物质的量之比为2∶3 |
B. 能与 能与 溶液发生反应 溶液发生反应 |
C. 因为其具有强酸性而被用于刻蚀玻璃 因为其具有强酸性而被用于刻蚀玻璃 |
D.用上述方法制备1  ,理论上需要消耗30 ,理论上需要消耗30  |
您最近半年使用:0次
2024-04-02更新
|
131次组卷
|
4卷引用:河北省保定市定州市第二中学2023-2024学年高一下学期3月月考化学试题
5 . 连二硫酸锰(MnS2O6,其中Mn为+2价)是一种常用的果蔬保鲜剂,易溶于水,室温下其水溶液在pH为2.8~3.5时最稳定。回答下列问题:
Ⅰ.制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。
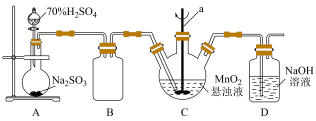
(1)仪器a的名称为________ ,装置B的作用是________ 。
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是_______ 。实验时需要向C中通入稍过量的SO2,目的是________ 。
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为_______ ,判断反应完成的现象是_______ ,待反应结束后经除杂、减压蒸发浓缩、结晶可得产品MnS2O6•nH2O。
Ⅱ.测定产品中Mn的质量分数
称取ag产品充分加热使其分解为MnSO4,然后加水溶解,用cmol•L-1的KMnO4溶液进行滴定(Mn元素均转化为MnO2)。
(4)滴定时,发生反应的离子方程式为_______ ;若滴定消耗KMnO4溶液的体积为VmL,则产品中Mn的质量分数为_______ 。
(5)下列操作会使得测定结果偏大的是_______ 。
Ⅰ.制备连二硫酸锰(MnS2O6)
某化学小组利用MnO2悬浊液吸收SO2气体制取连二硫酸锰的装置(部分夹持、加热仪器已省略)如图所示。

(1)仪器a的名称为
(2)装置C中的反应温度需要控制在0℃左右,控制温度的方法是
(3)装置C中反应生成等物质的量的MnS2O6和MnSO4,则反应的化学方程式为
Ⅱ.测定产品中Mn的质量分数
称取ag产品充分加热使其分解为MnSO4,然后加水溶解,用cmol•L-1的KMnO4溶液进行滴定(Mn元素均转化为MnO2)。
(4)滴定时,发生反应的离子方程式为
(5)下列操作会使得测定结果偏大的是
| A.滴定前锥形瓶用蒸馏水洗后未用待测MnSO4溶液润洗 |
| B.滴定前平视读数,滴定结束俯视读数 |
| C.滴定前滴定管中尖嘴处有气泡,滴定后气泡消失 |
| D.对连二硫酸锰产品进行加热操作时加热不充分 |
您最近半年使用:0次
6 . 向 溶液中通入一定体积的
溶液中通入一定体积的 使其充分反应,再向所得溶液中逐滴滴加
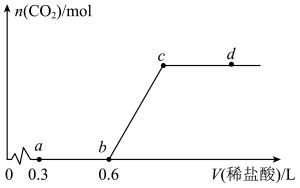
使其充分反应,再向所得溶液中逐滴滴加 的稀盐酸,测得产生
的稀盐酸,测得产生 的物质的量随加入盐酸的体积变化如图所示(不考虑
的物质的量随加入盐酸的体积变化如图所示(不考虑 的溶解)。下列说法正确的是
的溶解)。下列说法正确的是
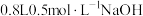 溶液中通入一定体积的
溶液中通入一定体积的 使其充分反应,再向所得溶液中逐滴滴加
使其充分反应,再向所得溶液中逐滴滴加 的稀盐酸,测得产生
的稀盐酸,测得产生 的物质的量随加入盐酸的体积变化如图所示(不考虑
的物质的量随加入盐酸的体积变化如图所示(不考虑 的溶解)。下列说法正确的是
的溶解)。下列说法正确的是
A.根据题中所给信息,可以求得图中的c点坐标为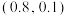 |
| B.由0到a的过程中,溶质的总物质的量持续增大 |
| C.由a到b的过程中,发生了1个化学反应 |
D.若减少初始 的通入量,则c点横纵坐标都将减小 的通入量,则c点横纵坐标都将减小 |
您最近半年使用:0次
7 . 某校化学兴趣小组研究学校附近的空气质量,遇到了下列问题,请你帮助他们。
(1)甲组同学设计了如图所示的实验装置,对悬浮颗粒物、空气中 含量进行测定。A装置的名称为
含量进行测定。A装置的名称为___________ 。
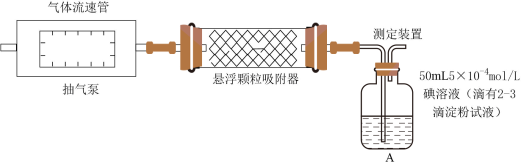
注:气体流速管是用来测量单位时间内通过气体的体积的装置
①用上述装置定量测定空气中的 和可吸入颗粒的含量,除测定气体流速(单位:cm3∙min-1)和反应所需时间外还需要的数据是
和可吸入颗粒的含量,除测定气体流速(单位:cm3∙min-1)和反应所需时间外还需要的数据是___________ 。
②已知:碘单质微溶于水, 可以增大碘在水中的溶解度。请你协助甲组同学完成
可以增大碘在水中的溶解度。请你协助甲组同学完成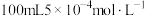 碘溶液的配制:
碘溶液的配制:
a.将容量瓶置于水平台面上,加入蒸馏水至距容量瓶刻度线1~2cm时,改用胶头滴管逐滴滴加,直至液体凹液面与刻度线相平。
b.用电子天平准确称取1.27g碘单质加入烧杯中,同时加入少量碘化钾固体,加水溶解后转入容量瓶中。
c.从上一步所得溶液中取出10.00mL溶液倒入烧杯中,加水稀释至100mL。
d.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转入到1000mL容量瓶中。
合理的步骤顺序是___________ 。
(2)乙组同学拟用如图简易装置测定空气中的 含量:
含量:
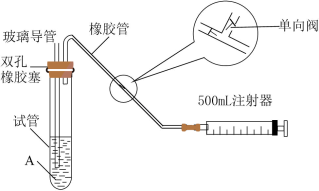
①检查该装置的气密性时,先在试管中装入适量的水(保证玻璃管的下端浸没在水中)。然后___________ (填写操作方法及实验现象),则证明该装置的气密性良好。
②测定指定地点空气中的 含量时,准确移取
含量时,准确移取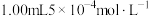 碘溶液,注入如图所示试管中。用适量的蒸馏水稀释后,再加2~3滴淀粉溶液,配制成溶液A.甲、乙两组同学分别使用如图所示相同的实验装置和溶液A,在同一地点、同时推拉注射器的活塞,反复抽气,直到溶液的蓝色全部褪尽为止停止抽气,记录抽气次数如下(假设每次抽气500mL)。
碘溶液,注入如图所示试管中。用适量的蒸馏水稀释后,再加2~3滴淀粉溶液,配制成溶液A.甲、乙两组同学分别使用如图所示相同的实验装置和溶液A,在同一地点、同时推拉注射器的活塞,反复抽气,直到溶液的蓝色全部褪尽为止停止抽气,记录抽气次数如下(假设每次抽气500mL)。
我国环境空气质量标准对空气质量测定中 的最高浓度限值如下表:
的最高浓度限值如下表:
经老师和同学们分析,甲组测定结果更为准确,则该地点的空气中 的含量为
的含量为___________ 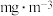 (保留2位有效数字),属于
(保留2位有效数字),属于___________ (填汉字)级标准。请你分析乙组实验结果产生较大偏差的原因是(两个小组所用装置和药品均无问题)___________ 。
(1)甲组同学设计了如图所示的实验装置,对悬浮颗粒物、空气中
 含量进行测定。A装置的名称为
含量进行测定。A装置的名称为
注:气体流速管是用来测量单位时间内通过气体的体积的装置
①用上述装置定量测定空气中的
 和可吸入颗粒的含量,除测定气体流速(单位:cm3∙min-1)和反应所需时间外还需要的数据是
和可吸入颗粒的含量,除测定气体流速(单位:cm3∙min-1)和反应所需时间外还需要的数据是②已知:碘单质微溶于水,
 可以增大碘在水中的溶解度。请你协助甲组同学完成
可以增大碘在水中的溶解度。请你协助甲组同学完成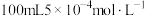 碘溶液的配制:
碘溶液的配制:a.将容量瓶置于水平台面上,加入蒸馏水至距容量瓶刻度线1~2cm时,改用胶头滴管逐滴滴加,直至液体凹液面与刻度线相平。
b.用电子天平准确称取1.27g碘单质加入烧杯中,同时加入少量碘化钾固体,加水溶解后转入容量瓶中。
c.从上一步所得溶液中取出10.00mL溶液倒入烧杯中,加水稀释至100mL。
d.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转入到1000mL容量瓶中。
合理的步骤顺序是
(2)乙组同学拟用如图简易装置测定空气中的
 含量:
含量:
①检查该装置的气密性时,先在试管中装入适量的水(保证玻璃管的下端浸没在水中)。然后
②测定指定地点空气中的
 含量时,准确移取
含量时,准确移取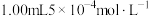 碘溶液,注入如图所示试管中。用适量的蒸馏水稀释后,再加2~3滴淀粉溶液,配制成溶液A.甲、乙两组同学分别使用如图所示相同的实验装置和溶液A,在同一地点、同时推拉注射器的活塞,反复抽气,直到溶液的蓝色全部褪尽为止停止抽气,记录抽气次数如下(假设每次抽气500mL)。
碘溶液,注入如图所示试管中。用适量的蒸馏水稀释后,再加2~3滴淀粉溶液,配制成溶液A.甲、乙两组同学分别使用如图所示相同的实验装置和溶液A,在同一地点、同时推拉注射器的活塞,反复抽气,直到溶液的蓝色全部褪尽为止停止抽气,记录抽气次数如下(假设每次抽气500mL)。| 分组 | 甲组 | 乙组 |
| 抽气次数 | 110 | 145 |
| 实验时长(min) | 6.5 | 4 |
 的最高浓度限值如下表:
的最高浓度限值如下表:最高浓度限值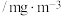 | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
 的含量为
的含量为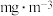 (保留2位有效数字),属于
(保留2位有效数字),属于
您最近半年使用:0次
8 . 二氧化氯(ClO2)是一种安全消毒剂,有强氧化性,易溶于水,沸点为11℃,在空气中体积分数超过10%时有爆炸性。工业上利用硫铁矿[主要成分为(FeS2)]还原氯酸钠(NaClO3)制取ClO2。利用下图装置模拟工业制备ClO2:向三颈烧瓶中加入NaClO3溶液、浓H2SO4并通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿。
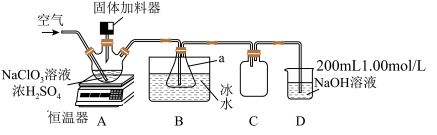
实验结束后,装置D中检测到含氯微粒有Cl-、ClO 和ClO
和ClO ,下列说法正确的是
,下列说法正确的是

实验结束后,装置D中检测到含氯微粒有Cl-、ClO
 和ClO
和ClO ,下列说法正确的是
,下列说法正确的是| A.35ClO2与37ClO2之间互为同位素 |
| B.若不考虑其他反应,装置D溶液可吸收0.2molClO2 |
C.反应后溶液中Cl-和ClO 的物质的量之比等于1:5 的物质的量之比等于1:5 |
D.反应后溶液中一定存在n(Na+)=n(Cl-)+n(ClO )+n(ClO )+n(ClO ) ) |
您最近半年使用:0次
9 . 铁酸锌(ZnFe2O4)是可见光的敏感半导体材料,也可以用作脱硫剂,难溶于水和稀硫酸,以锌灰(含ZnO及少量PbO、CuO、Fe2O3、SiO2)和Fe2(SO4)3为原料制备的ZnFe2O4的过程可以表示为下图:

已知:锌和铝都是活泼金属,它们的单质及化合物的性质具有一定的相似性
(1)请写出ZnO与氢氧化钠溶液反应的化学反应方程式:___________ 。
(2)下列说法正确的是___________。
(3)浸取过程中为了提高锌灰的浸取效果,还可以采取哪些方法(写出两种)___________ 。
(4)700℃时ZnFe2O4会分解,设计实验验证ZnFe2O4中含有Fe元素:___________ 。
(5)400℃时,装有脱硫剂的硫化反应器中,ZnFe2O4与H2、H2S反应生硫化物,其化学方程式为___________ 。

已知:锌和铝都是活泼金属,它们的单质及化合物的性质具有一定的相似性
(1)请写出ZnO与氢氧化钠溶液反应的化学反应方程式:
(2)下列说法正确的是___________。
| A.杂质中的SiO2属于酸性氧化物,能与Fe2O3反应 |
| B.除杂过程包括加足量锌粉、双氧水氧化等步骤,除Pb2+和Cu2+外,与锌粉反应的离子还有Fe3+和H+ |
| C.碳酸氢钠是为了调节溶液的pH,也可以用弱碱NH3·H2O代替 |
| D.ZnFe2O4难溶于稀硫酸,但在SO2-H2SO4体系中溶解度会明显增大 |
(3)浸取过程中为了提高锌灰的浸取效果,还可以采取哪些方法(写出两种)
(4)700℃时ZnFe2O4会分解,设计实验验证ZnFe2O4中含有Fe元素:
(5)400℃时,装有脱硫剂的硫化反应器中,ZnFe2O4与H2、H2S反应生硫化物,其化学方程式为
您最近半年使用:0次
名校
解题方法
10 . 现有 、
、 、
、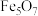 混合物共
混合物共 ,加盐酸后固体全部溶解,共收集到
,加盐酸后固体全部溶解,共收集到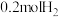 ,且向反应后的溶液中加入
,且向反应后的溶液中加入 溶液不显红色,则原混合物中铁的物质的量可能为
溶液不显红色,则原混合物中铁的物质的量可能为
 、
、 、
、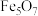 混合物共
混合物共 ,加盐酸后固体全部溶解,共收集到
,加盐酸后固体全部溶解,共收集到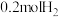 ,且向反应后的溶液中加入
,且向反应后的溶液中加入 溶液不显红色,则原混合物中铁的物质的量可能为
溶液不显红色,则原混合物中铁的物质的量可能为A. | B. | C.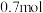 | D.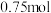 |
您最近半年使用:0次



