解题方法
1 . 实验室用下图装置制备干燥的Cl2并研究其性质。其中,a为湿润的淀粉KI试纸,b、c分别为湿润和干燥的红纸条,d为湿润的蓝色石蕊试纸。

(1)写出上图制备Cl2的化学方程式_______ 。
(2)为达成实验目的,甲、乙、丙中所用试剂分别是:甲中为_______ ;乙中为_______ ;丙中为_______ 。
(3)下列关于实验现象及Cl2性质的说法中,不正确 的是_______(填字母)。
(4)写出工业上制备漂白粉的化学方程式_______ ;写出工业上制备漂白液的离子方程式_______ 。

(1)写出上图制备Cl2的化学方程式
(2)为达成实验目的,甲、乙、丙中所用试剂分别是:甲中为
(3)下列关于实验现象及Cl2性质的说法中,
| A.一段时间后,观察到a变蓝 |
| B.b褪色,说明Cl2具有漂白性 |
| C.b褪色而c不褪色,说明Cl2能与水反应 |
| D.d先变红,一段时间后褪色,说明氯水有酸性 |
(4)写出工业上制备漂白粉的化学方程式
您最近半年使用:0次
2 . 校化学兴趣小组为验证Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
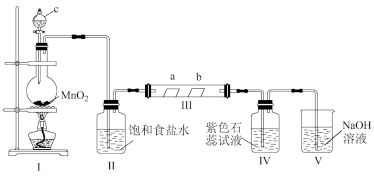
(1)实验室用MnO2和浓盐酸制备Cl2的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若实验中产生的Cl2足量,装置Ⅳ中的实验现象___________ 。
(4)写出装置V中反应的离子方程式___________ 。
(5)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。

(6)可用Cl2和Ca(OH)2制备的漂粉精
①漂白精的有效成分是___________ 。
②漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的化学方程式是:___________
③池水的酸碱性对漂粉精的消毒效果影响明显。
a.若池水碱性过强,杀毒作用会___________ (填“增强”或“减弱”)。
b.若池水酸性过强,会刺激眼睛和皮肤。有时加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是___________ (填离子符号)。

(1)实验室用MnO2和浓盐酸制备Cl2的化学方程式为
(2)装置Ⅱ的作用是
(3)若实验中产生的Cl2足量,装置Ⅳ中的实验现象
(4)写出装置V中反应的离子方程式
(5)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(6)可用Cl2和Ca(OH)2制备的漂粉精
①漂白精的有效成分是
②漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的化学方程式是:
③池水的酸碱性对漂粉精的消毒效果影响明显。
a.若池水碱性过强,杀毒作用会
b.若池水酸性过强,会刺激眼睛和皮肤。有时加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是
您最近半年使用:0次
名校
解题方法
3 . 化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)装置I中仪器c的名称是___________ 。
(2)实验结束后,同学们在装置Ⅲ中观察到 的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的___________ (填序号)装置。
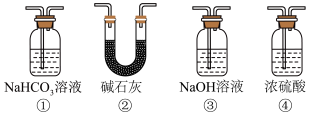
(3)若产生的 足量,装置Ⅳ中的实验现象是
足量,装置Ⅳ中的实验现象是___________ 。
(4)写出装置V中发生反应的离子方程式___________ 。
(5)将制得的氯气通入如图装置可制备无水 ,已知
,已知 在
在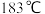 升华,遇潮湿空气立即产生大量白雾。
升华,遇潮湿空气立即产生大量白雾。

①实验开始时应先___________ (填“通入氯气”或“点燃酒精灯”)。
②用粗短导管连接A、B的目的是___________ 。C中碱石灰的作用是___________ 。
③若制备氯气时消耗 为
为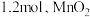 和铝粉均足量,所得产品
和铝粉均足量,所得产品 经纯化后测得质量为
经纯化后测得质量为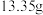 ,则该实验中
,则该实验中 的产率为
的产率为___________ ( )。
)。
(6)若将 通入热的烧碱溶液中,可以得到
通入热的烧碱溶液中,可以得到 和
和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为
的个数比为 时,混合液中
时,混合液中 和
和 的个数比为
的个数比为___________ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)装置I中仪器c的名称是
(2)实验结束后,同学们在装置Ⅲ中观察到
 的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
(3)若产生的
 足量,装置Ⅳ中的实验现象是
足量,装置Ⅳ中的实验现象是(4)写出装置V中发生反应的离子方程式
(5)将制得的氯气通入如图装置可制备无水
 ,已知
,已知 在
在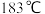 升华,遇潮湿空气立即产生大量白雾。
升华,遇潮湿空气立即产生大量白雾。
①实验开始时应先
②用粗短导管连接A、B的目的是
③若制备氯气时消耗
 为
为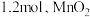 和铝粉均足量,所得产品
和铝粉均足量,所得产品 经纯化后测得质量为
经纯化后测得质量为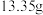 ,则该实验中
,则该实验中 的产率为
的产率为 )。
)。(6)若将
 通入热的烧碱溶液中,可以得到
通入热的烧碱溶液中,可以得到 和
和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为
的个数比为 时,混合液中
时,混合液中 和
和 的个数比为
的个数比为
您最近半年使用:0次
4 . 某化学兴趣小组为探究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
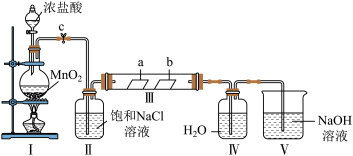
回答下列问题:
(1)加入药品前,必须先___________ 。盛装浓盐酸的仪器名称为___________ 。
(2)装置I中发生反应的离子方程式为___________ 。
(3)装置V中NaOH溶液的作用是___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应如何改进?___________ 。

回答下列问题:
(1)加入药品前,必须先
(2)装置I中发生反应的离子方程式为
(3)装置V中NaOH溶液的作用是
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应如何改进?
您最近半年使用:0次
5 . 为达到实验目的,下列方案设计恰当的是
| A | B | C | D | |
| 实验目的 | 制备 胶体 胶体 | 观察钠燃烧的现象 | 证明热稳定性: | 实验室收集氯气 |
| 装置 | 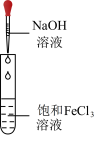 | 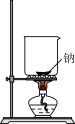 | 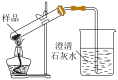 | 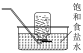 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 实验室用下图装置制备干燥的 并研究其性质,其中,a为湿润的淀粉
并研究其性质,其中,a为湿润的淀粉 试纸,b、c分别为湿润和干燥的红纸条,d为湿润的蓝色石蕊试纸。
试纸,b、c分别为湿润和干燥的红纸条,d为湿润的蓝色石蕊试纸。
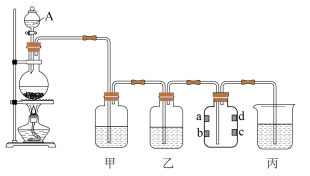
(1)仪器A的名称_____ ,写出制备 的化学方程式:
的化学方程式:_____ 。
(2)为达成实验目的,甲、乙中所用试剂分别为_____ 、_____ 。
(3)丙中试剂的作用:_____
(4)一段时间后,观察到a中现象_____ ,d中现象_____ 。
(5)对比b、c的现象,说明_____ 。
 并研究其性质,其中,a为湿润的淀粉
并研究其性质,其中,a为湿润的淀粉 试纸,b、c分别为湿润和干燥的红纸条,d为湿润的蓝色石蕊试纸。
试纸,b、c分别为湿润和干燥的红纸条,d为湿润的蓝色石蕊试纸。
(1)仪器A的名称
 的化学方程式:
的化学方程式:(2)为达成实验目的,甲、乙中所用试剂分别为
(3)丙中试剂的作用:
(4)一段时间后,观察到a中现象
(5)对比b、c的现象,说明
您最近半年使用:0次
7 . 某校化学兴趣小组为制备纯净的Cl2并研究Cl2的部分性质,设计了如图所示的实验仪器和药品。其中Ⅰ为干燥的红色试纸,Ⅱ为湿润的红色试纸。

(1)按气流从左到右的方向连接各仪器接口,正确的顺序是a→___________ (填小写字母)。
(2)装置A中盛放MnO2的仪器名称是___________ ,装置A中制备氯气的化学方程式为___________ 。
(3)装置B的作用是___________ 。
(4)若通入足量Cl2,实验过程中装置E中的实验现象___________ 。
(5)实验结束后,该组同学在装置D中观察到Ⅱ的红色褪去,但是并未观察到“Ⅰ无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置D之前添加图中的___________ 装置(填序号)。
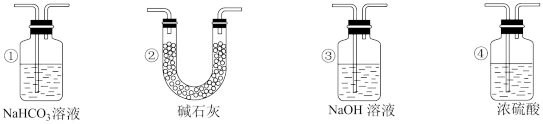
(6)1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图(反应温度为450℃):
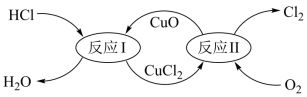
①反应Ⅱ的化学方程式为___________ 。
②该方法制取氯气,主要消耗的原料是___________ ,每生成标准状况下22.4L氯气转移的电子数目是___________ 。

(1)按气流从左到右的方向连接各仪器接口,正确的顺序是a→
(2)装置A中盛放MnO2的仪器名称是
(3)装置B的作用是
(4)若通入足量Cl2,实验过程中装置E中的实验现象
(5)实验结束后,该组同学在装置D中观察到Ⅱ的红色褪去,但是并未观察到“Ⅰ无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置D之前添加图中的

(6)1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图(反应温度为450℃):

①反应Ⅱ的化学方程式为
②该方法制取氯气,主要消耗的原料是
您最近半年使用:0次
2024-01-05更新
|
231次组卷
|
4卷引用:广东省深圳市高级中学2021-2022学年高一上学期期末考试化学试题
8 . 某化学兴趣小组为探究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

回答下列问题:
(1)盛装浓盐酸的仪器的名称为___________ 。
(2)装置Ⅰ中发生反应的化学方程式为___________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在___________ 和___________ (填装置序号)之间添加洗气装置,该装置的作用是___________ 。
(4)装置Ⅴ中NaOH溶液的作用是___________ ,相关反应的离子方程式为___________ 。
(5)工业上可用氢氧化钠与氯气反应制取84消毒液,在生活中84消毒液不可与洁厕灵(HCl)混用,否则会产生一种黄绿色有毒气体,其原因是___________ (用离子方程式解释)。
(6)氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强,氯水中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。
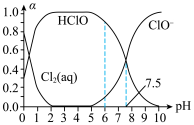
①用氯处理饮用水,pH=7.5时的杀菌效果比pH=6.5时的杀菌效果___________ (填“好”或“差”)。
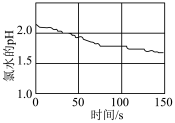
②利用数字化实验测定光照氯水得到光照过程中氯水的pH变化情况如图所示,变化原因是___________ (用方程式或必要的文字说明)。

回答下列问题:
(1)盛装浓盐酸的仪器的名称为
(2)装置Ⅰ中发生反应的化学方程式为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在
(4)装置Ⅴ中NaOH溶液的作用是
(5)工业上可用氢氧化钠与氯气反应制取84消毒液,在生活中84消毒液不可与洁厕灵(HCl)混用,否则会产生一种黄绿色有毒气体,其原因是
(6)氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强,氯水中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。

①用氯处理饮用水,pH=7.5时的杀菌效果比pH=6.5时的杀菌效果
②利用数字化实验测定光照氯水得到光照过程中氯水的pH变化情况如图所示,变化原因是

您最近半年使用:0次
9 . 某校化学兴趣小组为验证 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
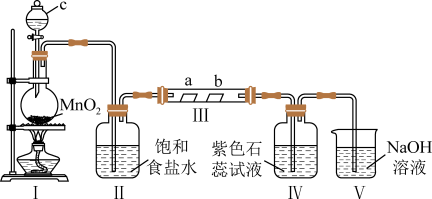
(1)装置Ⅰ中仪器c的名称是______ ,实验室用 和浓盐酸制备
和浓盐酸制备 的化学方程式为
的化学方程式为______ 。
(2)装置Ⅱ的作用是______ 。
(3)若实验中产生的 足量,装置Ⅳ中的实验现象
足量,装置Ⅳ中的实验现象______ 。
(4)写出装置Ⅴ中反应的离子方程式______ 。
(5)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的______ 装置(填序号)。
①
 溶液 ②
溶液 ②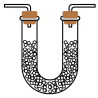 碱石灰
碱石灰
③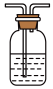
 溶液 ④
溶液 ④ 浓硫酸
浓硫酸
(6)可用 和
和 制备的漂粉精
制备的漂粉精
①漂粉精常用于游泳池的消毒,起消毒作用的是 。漂粉精在水中释放
。漂粉精在水中释放 的途径主要是:
的途径主要是:
______ (把反应补充完整)。
②池水的酸碱性对漂粉精的消毒效果影响明显。
a.若池水碱性过强,杀毒作用会______ (填“增强”或“减弱”)。
b.若池水酸性过强,会刺激眼睛和皮肤。有时加入 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是______ (填离子符号)。
③漂白精中的 在碱性条件下能够制备新型净水剂——高铁酸钾
在碱性条件下能够制备新型净水剂——高铁酸钾 ,补全下面的离子方程式:
,补全下面的离子方程式:______ 。




 ______=
______=

 ______+
______+ ______
______
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
(1)装置Ⅰ中仪器c的名称是
 和浓盐酸制备
和浓盐酸制备 的化学方程式为
的化学方程式为(2)装置Ⅱ的作用是
(3)若实验中产生的
 足量,装置Ⅳ中的实验现象
足量,装置Ⅳ中的实验现象(4)写出装置Ⅴ中反应的离子方程式
(5)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的
①

 溶液 ②
溶液 ② 碱石灰
碱石灰③

 溶液 ④
溶液 ④ 浓硫酸
浓硫酸(6)可用
 和
和 制备的漂粉精
制备的漂粉精①漂粉精常用于游泳池的消毒,起消毒作用的是
 。漂粉精在水中释放
。漂粉精在水中释放 的途径主要是:
的途径主要是:
②池水的酸碱性对漂粉精的消毒效果影响明显。
a.若池水碱性过强,杀毒作用会
b.若池水酸性过强,会刺激眼睛和皮肤。有时加入
 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是③漂白精中的
 在碱性条件下能够制备新型净水剂——高铁酸钾
在碱性条件下能够制备新型净水剂——高铁酸钾 ,补全下面的离子方程式:
,补全下面的离子方程式:



 ______=
______=

 ______+
______+ ______
______
您最近半年使用:0次
名校
解题方法
10 . 某校化学兴趣小组为探究 性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
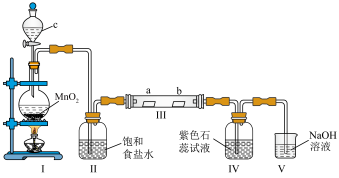
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸共热制备氯气的离子方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生的 足量,实验过程中装置Ⅳ中的实验现象是
足量,实验过程中装置Ⅳ中的实验现象是___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
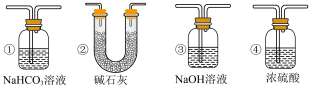
通过装置Ⅲ观察到预期现象,得出的结论是___________ 。
(5)实验结束后为了检验溶液中含有 ,请写出实验方案:
,请写出实验方案:___________ 。
(6)装置Ⅴ中可用饱和 溶液,反应的生成物有3种,其中有
溶液,反应的生成物有3种,其中有 、NaClO。试写出该反应的化学方程式:
、NaClO。试写出该反应的化学方程式:___________ 。
(7)整个实验应在通风厨中进行,并开启通风设备,原因是___________ 。
 性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生的
 足量,实验过程中装置Ⅳ中的实验现象是
足量,实验过程中装置Ⅳ中的实验现象是(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

通过装置Ⅲ观察到预期现象,得出的结论是
(5)实验结束后为了检验溶液中含有
 ,请写出实验方案:
,请写出实验方案:(6)装置Ⅴ中可用饱和
 溶液,反应的生成物有3种,其中有
溶液,反应的生成物有3种,其中有 、NaClO。试写出该反应的化学方程式:
、NaClO。试写出该反应的化学方程式:(7)整个实验应在通风厨中进行,并开启通风设备,原因是
您最近半年使用:0次



