名校
解题方法
1 . 利用如图的装置(省略部分加热装置)制备 (铋酸钠),已知
(铋酸钠),已知 不溶于冷水且在酸性溶液中迅速分解,
不溶于冷水且在酸性溶液中迅速分解, 是一种难溶于水的白色沉淀。下列说法正确的是
是一种难溶于水的白色沉淀。下列说法正确的是
 (铋酸钠),已知
(铋酸钠),已知 不溶于冷水且在酸性溶液中迅速分解,
不溶于冷水且在酸性溶液中迅速分解, 是一种难溶于水的白色沉淀。下列说法正确的是
是一种难溶于水的白色沉淀。下列说法正确的是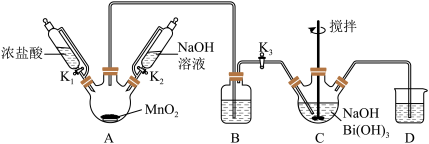
A.装置B应放入饱和 溶液,目的是吸收A中挥发的盐酸 溶液,目的是吸收A中挥发的盐酸 |
B.为使 完全转化为 完全转化为 ,反应过程中应向装置C通入过量 ,反应过程中应向装置C通入过量 |
C.拆除装置前必须进行的操作是关闭 、 、 ,打开 ,打开 |
D.上述反应中若消耗22.4L  则理论上可制得280g 则理论上可制得280g  |
您最近半年使用:0次
2 . 某校化学实验兴趣小组为了探究在实验室制备 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明
挥发出来,同时证明 的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。
的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。 仪器的名称是
仪器的名称是___________ ,浓盐酸与足量的 反应制取
反应制取 的化学反应方程式为:
的化学反应方程式为:___________ ;
(2)①装置 中盛放的试剂名称为
中盛放的试剂名称为___________ ,作用是___________ ,现象是___________ ;
②装置 和
和 中出现的不同现象说明的问题是
中出现的不同现象说明的问题是___________ ;
③装置 的作用是
的作用是___________ ;
④写出装置 中发生反应的离子方程式
中发生反应的离子方程式___________ ;
(3)乙同学认为甲同学设计的实验有缺陷,不能确保最终通入 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与
与___________ 之间(填装置序号),装置中应放入___________ (填试剂或用品名称)。
 的过程中有水蒸气和
的过程中有水蒸气和 挥发出来,同时证明
挥发出来,同时证明 的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。
的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。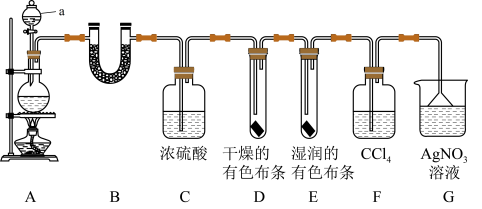
 仪器的名称是
仪器的名称是 反应制取
反应制取 的化学反应方程式为:
的化学反应方程式为:(2)①装置
 中盛放的试剂名称为
中盛放的试剂名称为②装置
 和
和 中出现的不同现象说明的问题是
中出现的不同现象说明的问题是③装置
 的作用是
的作用是④写出装置
 中发生反应的离子方程式
中发生反应的离子方程式(3)乙同学认为甲同学设计的实验有缺陷,不能确保最终通入
 溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入
溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在
溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与
与
您最近半年使用:0次
名校
3 . 氮是自然界中生物体生命活动不可缺少的重要元素,其化合物种类丰富。
Ⅰ.氨是重要的化工原料,某同学设计如图装置制备氨气并进行氨气的性质检验,部分夹持装置己省略,请回答下列问题: 的电子式为
的电子式为___________ 。
(2)试管内发生反应的化学方程式为___________ 。
(3)①实验之前先检验装置的气密性,然后放入试剂,打开止水夹a、c,关闭止水夹b,再点燃酒精灯,实验过程中丙装置的作用是___________ 。
②一段时间后, 充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为
充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为___________ 。
③为提高乙装置中实验的成功率,将盛放有___________ 的干燥管连接在甲、乙装置之间。
Ⅱ.研究氮的循环和转化对生产、生活有重要的价值,某工厂制硝酸的流程如图所示。___________ (填“ⅰ”“ⅱ”或“ⅲ”)。
(5)写出“氧化炉”中反应的化学方程式___________ 。
(6)“吸收塔”排出的尾气中会含有NO、 等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与
等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与 反应的化学方程式补充完整:
反应的化学方程式补充完整:______ 。
 ___________
___________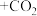 。
。
Ⅰ.氨是重要的化工原料,某同学设计如图装置制备氨气并进行氨气的性质检验,部分夹持装置己省略,请回答下列问题:
 的电子式为
的电子式为(2)试管内发生反应的化学方程式为
(3)①实验之前先检验装置的气密性,然后放入试剂,打开止水夹a、c,关闭止水夹b,再点燃酒精灯,实验过程中丙装置的作用是
②一段时间后,
 充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为
充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为③为提高乙装置中实验的成功率,将盛放有
Ⅱ.研究氮的循环和转化对生产、生活有重要的价值,某工厂制硝酸的流程如图所示。
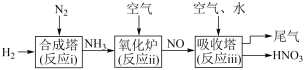
(5)写出“氧化炉”中反应的化学方程式
(6)“吸收塔”排出的尾气中会含有NO、
 等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与
等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与 反应的化学方程式补充完整:
反应的化学方程式补充完整: ___________
___________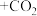 。
。
您最近半年使用:0次
名校
4 . 短周期主族元素W、X、Y和Z的原子序数依次增大,W原子是半径最小的原子,X原子的最外层电子数是内层电子数的3倍,元素Y是应用广泛的半导体材料,元素Z与X同主族。下列说法正确的是
| A.X、Y两种元素形成的化合物一定是共价化合物 |
| B.原子半径:Z>Y>X>W |
| C.最高价氧化物对应的水化物酸性:Y>Z |
| D.氢化物稳定性:X<Z |
您最近半年使用:0次
名校
5 . 下列离子方程式书写正确的是
A.锌与稀硝酸反应: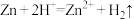 |
B. 溶液与 溶液与 溶液混合加热: 溶液混合加热: |
C.向 溶液中滴加氨水: 溶液中滴加氨水: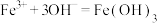 |
D.过量 气体通入氢氧化钠溶液中: 气体通入氢氧化钠溶液中: |
您最近半年使用:0次
名校
6 . 下列物质中,既含离子键又含共价键的是
A. | B. | C. | D. |
您最近半年使用:0次
名校
7 . 下列有关化学用语的表示正确的是
A. 的电子式: 的电子式: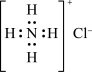 |
B. 的结构示意图: 的结构示意图: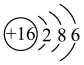 |
C.硝酸的电离方程式: |
| D.硅元素位于第三周期第ⅥA族 |
您最近半年使用:0次
8 . 2023年中国“大国重器”频频问世,彰显了中国科技发展的巨大成就。下列有关说法正确的是
| A.“梦天实验舱”原子钟利用电子跃迁计时,工作时发生化学变化 |
| B.“天问一号”火星车的保温材料为纳米气凝胶,能产生丁达尔效应 |
C.华为麒麟芯片是国产最强手机芯片,目前已经获得多个“世界第一”,芯片的半导体材料为 |
| D.中国天眼发现纳赫兹引力波,其使用的碳化硅材料为传统无机非金属材料 |
您最近半年使用:0次
解题方法
9 . 亚硝酰氯的化学式为NOCl,主要用于合成洗涤剂、触媒,也可用作有机合成中间体。其熔点-64.5℃,沸点-5.5℃,易水解。某实验小组用以下实验来探究亚硝酰氯的制备。回答下列问题:
(1)文献中记载可利用浓盐酸和 浓溶液反应制取少量的NOCl,装置如下图所示,
浓溶液反应制取少量的NOCl,装置如下图所示,________ 。
②用仪器X代替分液漏斗的优点是________ 。
③装置B中盛放无水 的仪器名称为
的仪器名称为________ ,装置C的作用是________ 。
(2)亚硝酰氯也可以用NO与 混合制取。
混合制取。
①实验室用铜和稀硝酸反应来制备NO,标准状况下1.92gCu完全反应理论上可产生________ LNO。
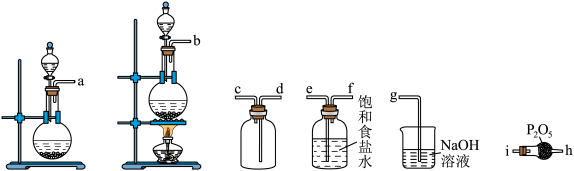
②选用如下图所示的部分装置,用二氧化锰制备一瓶纯净且干燥的氯气,各玻璃导管接口连接顺序为________ →d→c→g(气流方向从左至右,每组仪器最多使用一次)。实验室用二氧化锰制备氯气的离子方程式为________ 。 制取实验过程中“先通入
制取实验过程中“先通入 ,待反应装置中充满黄绿色气体时,再将NO缓缓通入”,此操作的目的是
,待反应装置中充满黄绿色气体时,再将NO缓缓通入”,此操作的目的是________ 。
(1)文献中记载可利用浓盐酸和
 浓溶液反应制取少量的NOCl,装置如下图所示,
浓溶液反应制取少量的NOCl,装置如下图所示,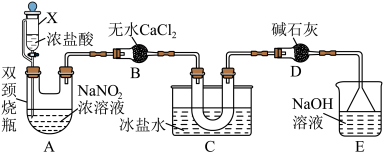
②用仪器X代替分液漏斗的优点是
③装置B中盛放无水
 的仪器名称为
的仪器名称为(2)亚硝酰氯也可以用NO与
 混合制取。
混合制取。①实验室用铜和稀硝酸反应来制备NO,标准状况下1.92gCu完全反应理论上可产生
②选用如下图所示的部分装置,用二氧化锰制备一瓶纯净且干燥的氯气,各玻璃导管接口连接顺序为
 制取实验过程中“先通入
制取实验过程中“先通入 ,待反应装置中充满黄绿色气体时,再将NO缓缓通入”,此操作的目的是
,待反应装置中充满黄绿色气体时,再将NO缓缓通入”,此操作的目的是
您最近半年使用:0次
解题方法
10 . 我国大飞机迅猛发展的背后离不开航空发动机技术的突破,而航空发动机技术的重大突破离不开一种关键的金属——铼(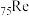 )。下列说法正确的是
)。下列说法正确的是
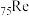 )。下列说法正确的是
)。下列说法正确的是A.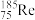 的摩尔质量为185 的摩尔质量为185 |
B.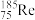 和 和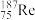 互为同位素 互为同位素 |
C.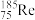 和 和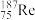 的性质完全相同 的性质完全相同 |
D.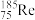 原子的中子数和质子数之差是110 原子的中子数和质子数之差是110 |
您最近半年使用:0次



