名校
解题方法
1 . 下列反应的离子方程式书写正确的是
A.碘化亚铁溶液中通入足量的氯气: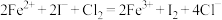 |
B.加碘盐与药物碘化钾片尽量不要同时服用: |
C.向 溶液中加入过量的NaOH溶液: 溶液中加入过量的NaOH溶液: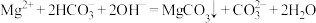 |
D.向 溶液中滴入 溶液中滴入 使 使 反应完全: 反应完全: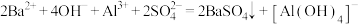 |
您最近半年使用:0次
今日更新
|
605次组卷
|
3卷引用:江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷
江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 (已下线)题型4 离子反应 氧化还原反应(25题)-2024年高考化学常考点必杀300题(新高考通用)湖南省“一起考”大联考2023-2024学年高三下学期3月模拟考试(模拟一)化学试题
2 . 某兴趣小组探究高锰酸钾和氨水的反应,实验如下:
注:实验中c(KMnO4) = 0.01 mol·L-1。
下列说法不正确 的是
| 序号 | 试剂 | 实验现象 |
| ① | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水+0.5 mL蒸馏水 | 溶液完全褪色所需时间:③<②<①。实验均产生棕褐色固体(经检验为MnO2),都伴有少量气泡产生(经检验为N2)。 |
| ② | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水 + 0.5 mL 1 mol·L-1稀硫酸 | |
| ③ | 2 mL KMnO4溶液 + 1 mL 10 mol·L-1氨水 + 0.5 mL 1 mol·L-1 Na2SO4溶液 | |
| ④ | 2 mL KMnO4溶液 + 1 mL 5 mol·L-1 (NH4)2SO4溶液 + 0.5 mL蒸馏水 | 无明显变化 |
下列说法
A.实验①中发生了反应2 MnO + 2NH3 = 2MnO2 + N2↑ + 2OH- + 2H2O + 2NH3 = 2MnO2 + N2↑ + 2OH- + 2H2O |
B.溶液完全褪色所需时间② < ①的主要原因:c(H+)增大,MnO 的氧化性增强 的氧化性增强 |
C.对比实验③④可得出,还原性:NH3 > NH |
| D.在实验④的试剂中,逐滴加入浓NaOH溶液,可观察到溶液褪色 |
您最近半年使用:0次
名校
解题方法
3 . 还原铁粉与水蒸气的反应装置如图所示。取少量反应后的固体加入稀硫酸使其完全溶解得溶液a;另取少量反应后的固体加入稀硝酸使其完全溶解,得溶液b.下列说法正确的是
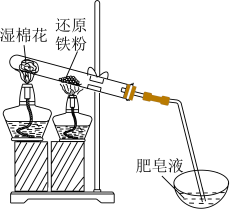
A.铁与水蒸气反应: |
B.肥皂液中产生气泡,不能证明铁与水蒸气反应生成 |
C.向溶液a中滴加 溶液,出现蓝色沉淀,说明铁粉未完全反应 溶液,出现蓝色沉淀,说明铁粉未完全反应 |
D.向溶液b中滴加 溶液,溶液变红,证实了固体中含有 溶液,溶液变红,证实了固体中含有 |
您最近半年使用:0次
7日内更新
|
390次组卷
|
3卷引用:北京市西城区2024届高三统一测试(一模)化学试题
北京市西城区2024届高三统一测试(一模)化学试题(已下线)题型6 元素及其化合物 化学实验基础(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届河南省焦作市博爱县第一中学高三下学期三模化学试题
4 . 化学与工农业生产、科学技术和日常生活密切相关。下列说法错误的是
| A.“天和核心舱”电推进系统中的腔体采用的氮化硼陶瓷属于新型无机非金属材料 |
| B.通过豆科植物的根瘤菌将氮气转化成氨,从而实现自然固氮 |
| C.丹霞地貌的岩层因含磁性氧化铁而成红色 |
| D.葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中产生了有香味的酯 |
您最近半年使用:0次
7日内更新
|
203次组卷
|
3卷引用:四川省绵阳南山中学2024届高三下学期三诊热身考试理综-化学试题
2024高三下·全国·专题练习
解题方法
5 .  具有强氧化性,可发生反应:
具有强氧化性,可发生反应:

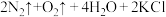 。下列说法不正确的是
。下列说法不正确的是
 具有强氧化性,可发生反应:
具有强氧化性,可发生反应:

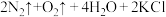 。下列说法不正确的是
。下列说法不正确的是A. 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 |
B. 仅作氧化剂 仅作氧化剂 |
C.生成1mol 转移电子的物质的量为5mol 转移电子的物质的量为5mol |
D.实验室不可用加热 固体的方法制备 固体的方法制备 |
您最近半年使用:0次
2024高三下·全国·专题练习
6 . I.“皮鞋很忙的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)计算、称量。配制该溶液需称取NaOH晶体的质量为_______ g。
(2)配制时,下列操作会导致所配溶液浓度偏高的是_______ 。
A.转移时有少量溶液溅出
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线
E.称量NaOH时用了生锈的砝码
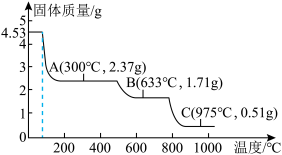
Ⅲ.取4.53gNH4Al(SO4)2∙12H2O加热分解,加热过程中固体质量随温度的变化如图所示。_______ 、_______ 。(填化学式)
A. 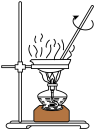 B.
B.  C.
C.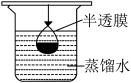
(1)计算、称量。配制该溶液需称取NaOH晶体的质量为
(2)配制时,下列操作会导致所配溶液浓度偏高的是
A.转移时有少量溶液溅出
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线
E.称量NaOH时用了生锈的砝码
Ⅲ.取4.53gNH4Al(SO4)2∙12H2O加热分解,加热过程中固体质量随温度的变化如图所示。
您最近半年使用:0次
7 . 铼(Re)是一种具有重要军事战略意义的金属。NH4ReO4是制备高纯度Re的重要中间体。
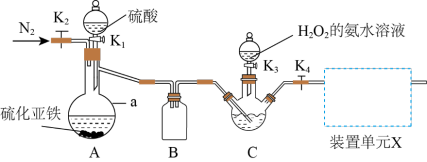
I.实验室制备NH4ReO4的装置如图所示。
②2NH4ReO4 2NH3↑+H2O+Re2O7
2NH3↑+H2O+Re2O7
回答下列问题:
(1)反应开始前先向C中三颈烧瓶内加入一定量的Re2O7和水。关闭K2、K3,打开K1、K4,三颈烧瓶内生成Re2S7。关闭K1,打开K2通入N2一段时间,通入N2的目的是_______ 。打开K3,滴入足量H2O2的氨水溶液,生成NH4ReO4;反应结束后从溶液中通过冷却结晶分离出NH4ReO4。
(2)下列装置可用作装置单元X的是_______ (填标号)。
I.实验室制备NH4ReO4的装置如图所示。
②2NH4ReO4
 2NH3↑+H2O+Re2O7
2NH3↑+H2O+Re2O7回答下列问题:
(1)反应开始前先向C中三颈烧瓶内加入一定量的Re2O7和水。关闭K2、K3,打开K1、K4,三颈烧瓶内生成Re2S7。关闭K1,打开K2通入N2一段时间,通入N2的目的是
(2)下列装置可用作装置单元X的是_______ (填标号)。
A. | B. |
C. | D. |
您最近半年使用:0次
8 . 实验室用废铁屑制取无水氯化铁并测其纯度。实验方案如下:
Ⅰ. 制备
制备
①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是_______ 。
(2)控制温度在40~50℃的原因是_______ 。
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为_______ 。
Ⅱ.无水 制备
制备
已知 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。
(4)按图装置进行实验。锥形瓶中生成无水 的总化学方程式为
的总化学方程式为_______ ;仪器A的作用是_______ 。
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用 溶液滴定(
溶液滴定(
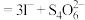 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。
①所制产品的纯度为_______ (以无水 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);
②所制产品中可能含有 杂质,检验
杂质,检验 的试剂为
的试剂为_______ (填化学式)溶液;产生 的原因可能是
的原因可能是_______ 。
Ⅰ.
 制备
制备①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是
(2)控制温度在40~50℃的原因是
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为
Ⅱ.无水
 制备
制备已知
 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。(4)按图装置进行实验。锥形瓶中生成无水
 的总化学方程式为
的总化学方程式为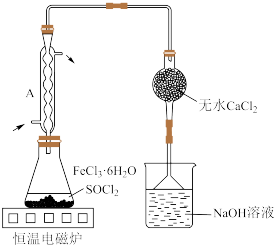
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用
 溶液滴定(
溶液滴定(
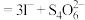 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。①所制产品的纯度为
 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);②所制产品中可能含有
 杂质,检验
杂质,检验 的试剂为
的试剂为 的原因可能是
的原因可能是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
9 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一种制备方法如下图所示:
的一种制备方法如下图所示: 粉进行转化反应的离子方程式为
粉进行转化反应的离子方程式为_______ ,生成的沉淀与硝酸反应,生成_______ 后可循环使用。
 的一种制备方法如下图所示:
的一种制备方法如下图所示:
 粉进行转化反应的离子方程式为
粉进行转化反应的离子方程式为
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
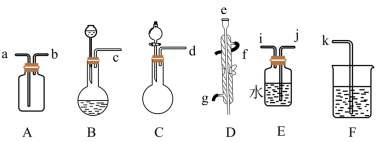
10 . 氯酸钠也能与盐酸反应生成氯气,同时还生成二氧化氯。二氧化氯(ClO2)熔点-59℃,沸点11℃,受热易分解,1体积水可溶解20体积的ClO2,下面是实验室用氯酸钠溶液与盐酸反应制取二氧化氯和氯水可能用到的实验装置和仪器(支持仪器和连接用橡胶管已略去);_______ 。
您最近半年使用:0次



