1 . 短周期主族元素W、X、Y、Z的原子序数依次增大。W的原子半径在短周期中最小;X、Z易形成两种常见的共价化合物,且其相对分子质量相差16;X、Z不属于同主族元素。下列说法正确的是
A.原子半径大小: | B.最高价氧化物对应的水化物的酸性: |
| C.X的氢化物的沸点一定低于Z的氢化物 | D.W、X、Y、Z四种元素可形成离子化合物 |
您最近半年使用:0次
2024-04-19更新
|
88次组卷
|
2卷引用:2024届青海省西宁市大通县高三下学期第二次模拟考试理科综合试题-高中化学
解题方法
2 . 已知蓝色环保颜料 由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
 由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是A.简单离子半径: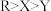 | B.最简单氢化物的稳定性: |
| C.Y的最高价氧化物对应的水化物为强酸 | D.W、Z形成的二元化合物为离子化合物 |
您最近半年使用:0次
解题方法
3 . 下列表示对应化学反应的离子方程式正确的是
A.用铝和氢氧化钠作管道疏通剂: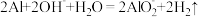 |
B. 在碱性环境中遇空气被氧化: 在碱性环境中遇空气被氧化: |
C.硫氢化钠溶液与稀硫酸混合有气泡产生: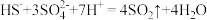 |
D.用 吸收 吸收 气体: 气体: |
您最近半年使用:0次
4 . Fe(OH)2具有较强的还原性,新制的白色Fe(OH)2会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色Fe(OH)2,某实验小组做了如下探究实验。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、___________ 、___________ 。
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是___________ 。
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:___________ 。___________ (用离子方程式表示)。
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:___________ 。
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
①由以上实验可得到的规律是___________ 。
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为___________ (填“1.0”“1.5”或“2.0”)mol/L。
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为___________ (任写一条)。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:

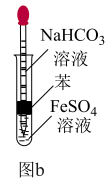
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
c(NaHCO3)/(mol/L) c(FeSO4)/(mol/L) | 1.0 | 1.5 | 2.0 | |
| 1.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 3.5 min | 9 min | 24 min | |
| 1.5 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 13 min | 15 min | 22 min | |
| 2.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率加快 | 常温下无现象,加热后产生白色沉淀 |
| 稳定时间 | 3 min | 8 min | 30 min | |
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为
您最近半年使用:0次
2024-04-16更新
|
146次组卷
|
2卷引用:2024届青海省百所名校高三下学期二模理科综合试题-高中化学
5 . 化学与生活密切相关.下列不涉及化学变化的是
| A.干冰摆盘 | B.燃放烟花 | C.食醋除水垢 | D.秸秆沤肥 |
您最近半年使用:0次
2024-04-15更新
|
80次组卷
|
2卷引用:2024届青海省百所名校高三下学期二模理科综合试题-高中化学
6 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.质量均为13g的 和 和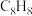 中含有的C原子数均为 中含有的C原子数均为 |
B. 的苯甲酸钠溶液中含有苯甲酸根离子的数目小于 的苯甲酸钠溶液中含有苯甲酸根离子的数目小于 |
C. 是正四面体网状结构,则 是正四面体网状结构,则 中含有的Si-O键数为 中含有的Si-O键数为 |
D.当氧化产物为 时,每生成22.4L(标准状况) 时,每生成22.4L(标准状况) 转移的电子数为 转移的电子数为 |
您最近半年使用:0次
名校
7 . 化学上,将质量数相同、质子数不同的核素称为同量素。某核聚变方程为 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是| A.X的金属性比Y的强 | B.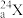 和 和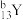 互为同量素 互为同量素 |
C.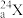 与 与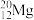 互为同位素 互为同位素 | D.X、Y最外层电子数之比为1:3 |
您最近半年使用:0次
2024-04-05更新
|
70次组卷
|
2卷引用:青海省海南州贵德高级中学2023-2024学年高三上学期10月月考化学试卷
解题方法
8 . 完成下列离子方程式。
(1)铁与稀硫酸反应________ ;
(2)碳酸钠溶液中加入稀盐酸________ ;
(3)氢氧化钡和稀硫酸反应________ 。
(1)铁与稀硫酸反应
(2)碳酸钠溶液中加入稀盐酸
(3)氢氧化钡和稀硫酸反应
您最近半年使用:0次
9 . 用双线桥表示下列氧化还原反应的情况:
(1)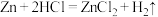
________ ;
(2)
________ 。
(1)
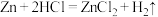
(2)

您最近半年使用:0次
10 . 按要求完成下列各题:
(1)19.2 g 在标准状况下的体积为
在标准状况下的体积为______ L,其中含氧原子的物质的量为______ mol。
(2)0.5 mol 的质量是
的质量是______ g,含______ 个 分子,含
分子,含______ mol氧原子。
(3)相同物质的量的CO和 ,含氧原子个数比为
,含氧原子个数比为______ ,它们的质量之比为______ 。
(4)相同质量的CO和 ,物质的量之比为
,物质的量之比为______ 。
(5)1 mol 中含
中含______ mol硫原子,______ 个氧原子。
(1)19.2 g
 在标准状况下的体积为
在标准状况下的体积为(2)0.5 mol
 的质量是
的质量是 分子,含
分子,含(3)相同物质的量的CO和
 ,含氧原子个数比为
,含氧原子个数比为(4)相同质量的CO和
 ,物质的量之比为
,物质的量之比为(5)1 mol
 中含
中含
您最近半年使用:0次
2024-04-03更新
|
34次组卷
|
2卷引用:青海省西宁市海湖中学2023-2024学年高一上学期第二次阶段考试化学试题



