名校
解题方法
1 . X、Y、Z均为元素周期表中前20号元素, Xb+、Yb-、Z(b+1)-三种简单离子的电子层结构相同,下列说法正确的是
| A.原子半径: Z>Y>X | B.离子半径:  |
C.气态氢化物的稳定性:  | D.Z(b+1) ⁻的还原性一定强于 Yb⁻ |
您最近半年使用:0次
2 . 工业上用S8(分子结构: )CH4为原料制备CS2,发生反应:
)CH4为原料制备CS2,发生反应: ,
, 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
A.1molH2S中含有的孤电子对数为 |
B.生成17gH2S,转移的电子数为 |
C.消耗1molS8,断裂的S-S键数目为 |
D.22.4LCH4中含有的电子数为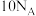 |
您最近半年使用:0次
解题方法
3 . Ⅰ.氯水具有多种性质,该小组同学用足量氯水分别与 溶液,
溶液, 溶液和
溶液和 溶液反应。完成下列问题:
溶液反应。完成下列问题:
已知:常温下发生反应:i. ;ii:
;ii:
(1)证明氯水中含有盐酸,可选择的试剂是________ 溶液(选填“石蕊溶液”或“ ”)。
”)。
(2)氯水与 溶液反应能证明氯水具有氧化性。请补充完整足量氯水与
溶液反应能证明氯水具有氧化性。请补充完整足量氯水与 溶液反应的离子方程式:
溶液反应的离子方程式:________ 。
________ ________
________ ________
________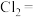 ________
________ ________
________ ________
________
Ⅱ.该小组同学在实验室中利用下图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
(3)写出装置①中制取氯气的离子方程式________ 。
(4)装置②盛装的试剂是________ ,其作用是________ 。
(5)装置③中反应化学方程式为________ ,反应结束后,取出③中试管,经冷却结晶,过滤,少量(冷)水洗涤,干燥,得到 晶体。
晶体。
(6)装置④中采用冰水浴冷却的目的是________ 。
(7)取少量 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫色。根据上述实验,以下结论正确的是________
层显紫色。根据上述实验,以下结论正确的是________
 溶液,
溶液, 溶液和
溶液和 溶液反应。完成下列问题:
溶液反应。完成下列问题:已知:常温下发生反应:i.
 ;ii:
;ii:
(1)证明氯水中含有盐酸,可选择的试剂是
 ”)。
”)。(2)氯水与
 溶液反应能证明氯水具有氧化性。请补充完整足量氯水与
溶液反应能证明氯水具有氧化性。请补充完整足量氯水与 溶液反应的离子方程式:
溶液反应的离子方程式:________
 ________
________ ________
________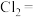 ________
________ ________
________ ________
________
Ⅱ.该小组同学在实验室中利用下图装置(部分装置省略)制备
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。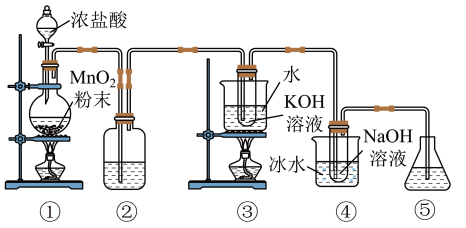
(3)写出装置①中制取氯气的离子方程式
(4)装置②盛装的试剂是
(5)装置③中反应化学方程式为
 晶体。
晶体。(6)装置④中采用冰水浴冷却的目的是
(7)取少量
 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫色。根据上述实验,以下结论正确的是________
层显紫色。根据上述实验,以下结论正确的是________A.氧化性: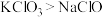 | B.氧化性: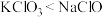 |
C.还原性: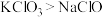 | D.还原性: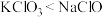 |
您最近半年使用:0次
4 . 在化学课上老师向NaOH溶液通入 后无明显现象。
后无明显现象。
(提出问题)如何通过实验证明 与NaOH发生了反应?
与NaOH发生了反应?
[查阅资料]①碳酸钠溶液中滴加少量的稀盐酸,会先反应生成碳酸氢钠(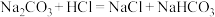 )
)
②碳酸钠在二氧化碳过量的条件继续与水和二氧化碳反应生成碱性较弱的碳酸氢钠。
(设计实验)
(1)反应物之-- 消失的角度,某同学设计了如下图所示的实验,打开活塞,向充满
消失的角度,某同学设计了如下图所示的实验,打开活塞,向充满 的瓶中滴入NaOH溶液,一会儿后观察到的现象是
的瓶中滴入NaOH溶液,一会儿后观察到的现象是________ 。据此现象判断NaOH与 发生了化学反应。
发生了化学反应。________ 。
(2)假设生成物为 ,分别设计了以下两个实验方案:
,分别设计了以下两个实验方案:
(实验拓展)该小组同学将过量的干冰放入氢氧化钠溶液中,利用数字化技术测定溶液pH变化,如图所示。请用化学方程式回答下列问题:________ ;
(4)CD段pH低于7的原因可能是________ 。
 后无明显现象。
后无明显现象。(提出问题)如何通过实验证明
 与NaOH发生了反应?
与NaOH发生了反应?[查阅资料]①碳酸钠溶液中滴加少量的稀盐酸,会先反应生成碳酸氢钠(
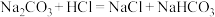 )
)②碳酸钠在二氧化碳过量的条件继续与水和二氧化碳反应生成碱性较弱的碳酸氢钠。
(设计实验)
(1)反应物之--
 消失的角度,某同学设计了如下图所示的实验,打开活塞,向充满
消失的角度,某同学设计了如下图所示的实验,打开活塞,向充满 的瓶中滴入NaOH溶液,一会儿后观察到的现象是
的瓶中滴入NaOH溶液,一会儿后观察到的现象是 发生了化学反应。
发生了化学反应。
(2)假设生成物为
 ,分别设计了以下两个实验方案:
,分别设计了以下两个实验方案:实验操作 | 实验现象 | 结论 |
| 方案一:向实验(1)所得的溶液中加入 | 有白色沉淀产生 | 有新物质 生成,发生反应。 生成,发生反应。 |
| 方案二:向实验(1)所得溶液中滴加过量稀盐酸 |
(实验拓展)该小组同学将过量的干冰放入氢氧化钠溶液中,利用数字化技术测定溶液pH变化,如图所示。请用化学方程式回答下列问题:
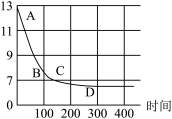
(4)CD段pH低于7的原因可能是
您最近半年使用:0次
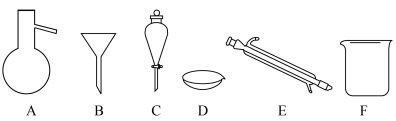
5 . 下图所示是分离混合物时常用的仪器,回答下列问题:________ 、________ 。
(2)在粗盐中含有 、
、 、
、 等杂质,精制时所用的试剂为:①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液。下列加入试剂的顺序中正确的是________(填字母)。
等杂质,精制时所用的试剂为:①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液。下列加入试剂的顺序中正确的是________(填字母)。
(3)现有十种物质:①铁单质②石墨 ③氯气 ④硫酸钡晶体⑤醋酸⑥盐酸⑦石灰水⑧乙醇⑨熔化的硝酸钾⑩纯碱。
其中能导电的是________ ,属于电解质的是________ 。
(4)选择下列实验方法分离物质,将分离方法的序号填在横线上
A.萃取分液 B.结晶 C.分液 D.蒸馏 E.过滤 F.升华 G.渗析
①________ 分离饱和食盐水与沙子的混合物。
②________ 除去 胶体中的少量碘化钠。
胶体中的少量碘化钠。
③________ 分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
④________ 从碘的水溶液里提取碘。
⑤________ 分离水和汽油的混合物。
⑥________ 分离碘单质和氯化钠固体混合物。
(2)在粗盐中含有
 、
、 、
、 等杂质,精制时所用的试剂为:①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液。下列加入试剂的顺序中正确的是________(填字母)。
等杂质,精制时所用的试剂为:①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液。下列加入试剂的顺序中正确的是________(填字母)。| A.①②③④ | B.②③④① | C.②④③① | D.③④②① |
(3)现有十种物质:①铁单质②石墨 ③氯气 ④硫酸钡晶体⑤醋酸⑥盐酸⑦石灰水⑧乙醇⑨熔化的硝酸钾⑩纯碱。
其中能导电的是
(4)选择下列实验方法分离物质,将分离方法的序号填在横线上
A.萃取分液 B.结晶 C.分液 D.蒸馏 E.过滤 F.升华 G.渗析
①
②
 胶体中的少量碘化钠。
胶体中的少量碘化钠。③
④
⑤
⑥
您最近半年使用:0次
6 . 下列反应的离子方程式或电离方程式正确的是
A. 在水中的电离: 在水中的电离: |
B.实验室制取 胶体: 胶体: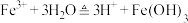 (胶体) (胶体) |
C.向碳酸氢钠溶液中滴加少量的澄清石灰水: |
D. 溶液中加入足量 溶液中加入足量 溶液: 溶液: |
您最近半年使用:0次
7 . 金属钠制取氧化钠通常利用反应: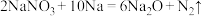 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
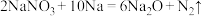 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温常压下,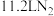 中含电子的个数为 中含电子的个数为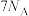 |
| B.23gNa在反应中失去电子的物质的量为1mol |
C. 的摩尔质量为28 的摩尔质量为28 |
D.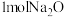 中含有的离子总数为 中含有的离子总数为 |
您最近半年使用:0次
8 . 科学家制得一种新型分子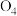 。关于
。关于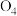 和
和 的下列说法不正确的是
的下列说法不正确的是
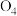 。关于
。关于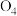 和
和 的下列说法不正确的是
的下列说法不正确的是A.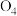 和 和 互为同位素 互为同位素 | B.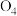 和 和 均属于纯净物 均属于纯净物 |
| C.都属于单质 | D. 和 和 的化学性质不相同 的化学性质不相同 |
您最近半年使用:0次
9 . 我国传统文化蕴含着丰富的化学知识,下列说法正确的
| A.“凡酸坏之酒,皆可蒸烧”,该过程利用了物质的溶解性不同 |
| B.“春蚕到死丝方尽,蜡炬成灰泪始干”,该过程不涉及氧化还原反应 |
| C.“青蒿一握,以水二升渍,绞取汁”,青蒿素的提取过程涉及化学变化 |
| D.“风干日曝咸味加,始灌潮波塯成卤”,该过程涉及的操作方法是蒸发结晶 |
您最近半年使用:0次
名校
解题方法
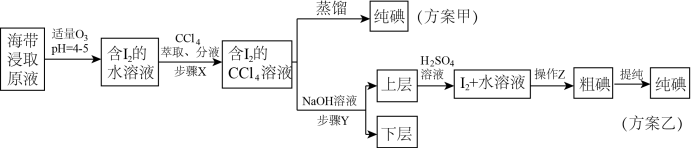
10 . 某学习小组按如下实验流程从海带中提取碘单质。 的沸点高于
的沸点高于 ,根据以上流程,判断下列说法错误的是
,根据以上流程,判断下列说法错误的是
 的沸点高于
的沸点高于 ,根据以上流程,判断下列说法错误的是
,根据以上流程,判断下列说法错误的是| A.“萃取、分液”时,获得下层溶液进行下一步操作 |
B.加入 溶液后发生反应的离子方程式为 溶液后发生反应的离子方程式为 |
C.方案甲采用蒸馏法的缺点在于 易与 易与 一同被蒸出,分离效果差 一同被蒸出,分离效果差 |
| D.步骤Y应加入过量氢氧化钠溶液,确保反萃取充分,下层液体可循环利用 |
您最近半年使用:0次



