1 . 下列化学用语正确的是
A.甲烷的结构式: | B.乙烷的结构简式; |
C.四氯化碳的电子式: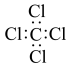 | D.甲基的电子式: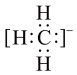 |
您最近半年使用:0次
名校
2 . 下列事实不能说明元素的金属性或非金属性相对强弱的是
| 选项 | 事实 | 推论 |
| A | 与冷水反应,K比Mg剧烈 | 金属性:K>Mg |
| B |  的碱性强于 的碱性强于 | 金属性:Ca>Mg |
| C | SO2与 溶液反应生成 溶液反应生成 | 非金属性:S>C |
| D | 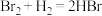 、 、 | 非金属性:Br>I |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
3 . 下列实验操作、现象和结论都正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向某溶液中加入 溶液并加热,产生能使湿润蓝色石蕊试纸变红的气体 溶液并加热,产生能使湿润蓝色石蕊试纸变红的气体 | 该溶液中一定含有 |
| B | 室温下,向 溶液中滴加少量 溶液中滴加少量 溶液,再滴加几滴淀粉溶液,溶液变蓝色 溶液,再滴加几滴淀粉溶液,溶液变蓝色 |  的氧化性比 的氧化性比 的强 的强 |
| C | 向溶液中加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失 | 一定有 |
| D | 向某溶液中加入少量新制氯水后再加几滴 溶液,溶液变为红色 溶液,溶液变为红色 | 该溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列表示对应化学反应的离子方程式正确的是
A.足量铁粉加入稀硝酸中: |
B.将 通入到 通入到 溶液中: 溶液中: |
C. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
D.向 溶液中通入 溶液中通入 气体使溶液棕黄色变浅: 气体使溶液棕黄色变浅: |
您最近半年使用:0次
名校
5 . 乙研究小组为了利用稀硫酸制备 ,进行了如图所示的实验设计。
,进行了如图所示的实验设计。 能加快生成
能加快生成 的反应速率,发挥作用的原理可表述为:
的反应速率,发挥作用的原理可表述为:
①
②……
(1)反应②的离子方程式 为______________ 。
(2)某小组通过向铜和稀硫酸的混合物中加入过氧化氢的方法制备硫酸铜,但是在实际操作时,发现所消耗的 的量往往会大于理论值,原因是
的量往往会大于理论值,原因是__________ 。
取 晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。
晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。 时,固体的成分为
时,固体的成分为________ (写出计算步骤 )。
(4)当剩余固体为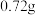 时,加热的温度不能低于
时,加热的温度不能低于_____ ℃,如果此时产生的气体中含有 ,请写出
,请写出 受热分解的化学方程式
受热分解的化学方程式________ 。
 ,进行了如图所示的实验设计。
,进行了如图所示的实验设计。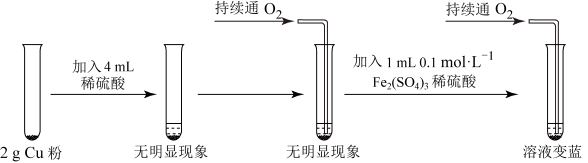
 能加快生成
能加快生成 的反应速率,发挥作用的原理可表述为:
的反应速率,发挥作用的原理可表述为:①

②……
(1)反应②的
(2)某小组通过向铜和稀硫酸的混合物中加入过氧化氢的方法制备硫酸铜,但是在实际操作时,发现所消耗的
 的量往往会大于理论值,原因是
的量往往会大于理论值,原因是取
 晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。
晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。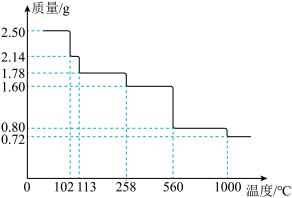
 时,固体的成分为
时,固体的成分为(4)当剩余固体为
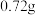 时,加热的温度不能低于
时,加热的温度不能低于 ,请写出
,请写出 受热分解的化学方程式
受热分解的化学方程式
您最近半年使用:0次
名校
解题方法
6 . 某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子。该小组同学取部分水样进行实验,向水样中先滴加足量硝酸钡溶液,产生白色沉淀;再滴加足量稀盐酸,沉淀部分溶解;最后滴加硝酸银溶液,又产生白色沉淀。下列说法正确的是
中的若干种离子。该小组同学取部分水样进行实验,向水样中先滴加足量硝酸钡溶液,产生白色沉淀;再滴加足量稀盐酸,沉淀部分溶解;最后滴加硝酸银溶液,又产生白色沉淀。下列说法正确的是
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子。该小组同学取部分水样进行实验,向水样中先滴加足量硝酸钡溶液,产生白色沉淀;再滴加足量稀盐酸,沉淀部分溶解;最后滴加硝酸银溶液,又产生白色沉淀。下列说法正确的是
中的若干种离子。该小组同学取部分水样进行实验,向水样中先滴加足量硝酸钡溶液,产生白色沉淀;再滴加足量稀盐酸,沉淀部分溶解;最后滴加硝酸银溶液,又产生白色沉淀。下列说法正确的是A.观察水样可以确定一定存在的离子只有 |
B.经过实验可以确定一定存在的离子是 、 、 、 、 、 、 |
C.水样中可能存在 |
D.水样中可能存在 |
您最近半年使用:0次
名校
解题方法
7 . 下列有关化学用语表示正确的是
A.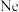 和 和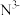 的结构示意图均为: 的结构示意图均为: | B.叠氮酸钠的分子式是: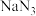 |
C.氨气的空间填充模型: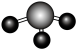 | D.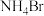 的电子式: 的电子式: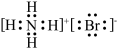 |
您最近半年使用:0次
8 . 应用下列装置能达到实验目的的是
| A | B | |
| 装置 |
|
|
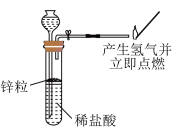
| 目的 | 从 溶液中制得 溶液中制得 晶体 晶体 | 可用于制备并检验氢气的可燃性 |
| C | D | |
| 装置 |
|
|
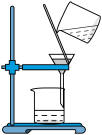
| 目的 | 除去 中的HCl并干燥 中的HCl并干燥 | 分离 胶体与NaCl溶液 胶体与NaCl溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
9 . 一节1号干电池可以让1平方米土地上的庄稼颗粒无收,回收电池既可以防止污染又可以变废为宝。废旧锌锰干电池内部的黑色物质A主要含有 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:________ (填化学式)。
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为 ,另一个是
,另一个是________ 。灼烧时,MnOOH与空气中的氧气反应的化学方程式为________________ 。
(3)第III步中为提高反应速率,可以采取的措施有________ (任写一条)。
(4)已知: 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为________________ ;
②操作VI中需要的玻璃仪器有________ ;
③你认为操作VII中检测的方法及现象是________ 时可继续进行操作VIII;
④操作VIII中用无水乙醇洗涤的目的是________ 。
 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为
 ,另一个是
,另一个是(3)第III步中为提高反应速率,可以采取的措施有
(4)已知:
 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: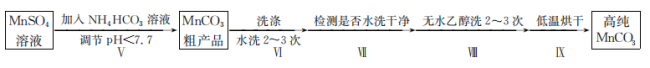
 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为②操作VI中需要的玻璃仪器有
③你认为操作VII中检测的方法及现象是
④操作VIII中用无水乙醇洗涤的目的是
您最近半年使用:0次
名校
10 . 下列实验“操作和现象”与“结论”对应关系正确的是
操作 | 现象 | 结论 | |
A. | 向NaBr溶液中滴入少量氯水和苯,振荡、静置 | 溶液上层呈橙色 | 还原性: |
B. | 将氯气缓缓通入到紫色的石蕊溶液中 | 石蕊溶液先变红后褪色 | 氯气与水反应生成了酸性物质和漂白性物质 |
C. | 将装满氯水的圆底烧瓶倒置在盛有水的水槽中,日光照射 | 烧瓶内有气泡生成 | 日光照射时,逸出的气体只可能是 |
D. | 分别加热 和 和 固体 固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次