名校
解题方法
1 . 下列离子方程式书写正确的是
A.向Mg(HCO3)2溶液中加入足量的澄清石灰水:Mg2++2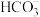 +Ca2++2OH-=MgCO3↓+CaCO3↓+2H2O +Ca2++2OH-=MgCO3↓+CaCO3↓+2H2O |
| B.XeF2通入水中:2XeF2+2H2O=2Xe+4F-+4H++O2 |
C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰使 沉淀完全 沉淀完全 +Al3++2 +Al3++2 +2Ba2++4OH-=Al(OH)3↓+NH3·H2O+2BaSO4↓ +2Ba2++4OH-=Al(OH)3↓+NH3·H2O+2BaSO4↓ |
| D.CuCl2溶液中加入NaHS溶液Cu 2++2HS-+2H2O=Cu(OH)2↓+2H2S↑ |
您最近半年使用:0次
名校
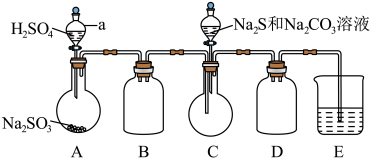
2 . 亚硫酸钠和硫代硫酸钠(Na2S2O3)都是重要的含硫化合物。某化学兴趣小组进行以下有关实验,填写下列空白。
实验Ⅰ:证明Na2SO3中硫元素的价态能发生+4→+6转化
(1)实验中,不需要用到的试剂有___________ (填标号)。
a.稀硫酸 b.H2O2溶液 c.稀盐酸 d.淀粉碘化钾溶液 e.BaCl2溶液
观察到的现象是___________ 。
实验Ⅱ:制取硫代硫酸钠
利用如图所示装置进行实验___________ 。
(3)装置D的作用是___________ 。
(4)实验中,为使 缓慢通入烧瓶C,采取的操作是
缓慢通入烧瓶C,采取的操作是___________ 。
实验Ⅲ:测定某硫代硫酸钠样品的纯度(设样品中只含Na2SO3杂质)
设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品7.9g,配制成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用0.1mol·L-1I2标准溶液滴定(发生反应:2S2O +I2=S4O
+I2=S4O +2I-),至滴定终点共消耗标准溶液23.60mL。
+2I-),至滴定终点共消耗标准溶液23.60mL。
(5)样品中Na2S2O3的百分含量为___________ (保留三位有效数字)。
实验Ⅰ:证明Na2SO3中硫元素的价态能发生+4→+6转化
(1)实验中,不需要用到的试剂有
a.稀硫酸 b.H2O2溶液 c.稀盐酸 d.淀粉碘化钾溶液 e.BaCl2溶液
观察到的现象是
实验Ⅱ:制取硫代硫酸钠
利用如图所示装置进行实验
(3)装置D的作用是
(4)实验中,为使
 缓慢通入烧瓶C,采取的操作是
缓慢通入烧瓶C,采取的操作是实验Ⅲ:测定某硫代硫酸钠样品的纯度(设样品中只含Na2SO3杂质)
设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品7.9g,配制成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用0.1mol·L-1I2标准溶液滴定(发生反应:2S2O
 +I2=S4O
+I2=S4O +2I-),至滴定终点共消耗标准溶液23.60mL。
+2I-),至滴定终点共消耗标准溶液23.60mL。(5)样品中Na2S2O3的百分含量为
您最近半年使用:0次
名校
解题方法
3 . 通过测定混合气中O2含可计算已变质的Na2O2(含Na2CO3)纯度的实验装置如图(Q为弹性良好的气囊)。下列分析正确的是
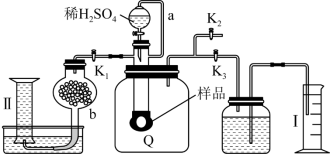
| A.b球形干燥管中装有氯化钙,用于除去气体中的水蒸气 |
| B.测定气体总体积必须关闭K1、K2,打开K3 |
| C.量筒Ⅰ用于测二氧化碳的量,干燥管b中装入碱石灰,量筒Ⅱ用于测氧气的量 |
| D.读完气体总体积后,关闭K3,缓缓打开K1、K2;可观察到Q气球慢慢变大 |
您最近半年使用:0次
名校
解题方法
4 . 将等物质的量的铁和铜的混合物24 g与600 mL稀硝酸恰好完全反应,生成NO 6.72 L(标准状况 ,向反应后的溶液中加入1mol/LNaOH溶液使金属离子恰好沉淀,过滤。下列有关说法正确的是
,向反应后的溶液中加入1mol/LNaOH溶液使金属离子恰好沉淀,过滤。下列有关说法正确的是
 ,向反应后的溶液中加入1mol/LNaOH溶液使金属离子恰好沉淀,过滤。下列有关说法正确的是
,向反应后的溶液中加入1mol/LNaOH溶液使金属离子恰好沉淀,过滤。下列有关说法正确的是| A.混合物溶解后的溶液中c(Fe3+):c(Fe2+) = 1:2 |
| B.需加入NaOH溶液600 mL |
| C.最后所得沉淀在空气中充分加热可得固体32 g |
| D.稀硝酸的物质的量浓度是1 mol/L |
您最近半年使用:0次
名校
解题方法
5 . 将15.6gNa2O2和5.4gAl 同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,下列说法错误的是
| A.最终溶液:c(Na+)= 2 mol·L-1 | B.标准状况下,反应过程中得到6.72L气体 |
| C.最终溶液:c(Na+) >c(Cl-) | D.最终得到7.8 g沉淀 |
您最近半年使用:0次
名校
解题方法
6 . M、W、X、Y、Z是同周期主族元素,X原子的最外层电子数是W原子次外层电子数的3倍,R元素是无机非金属材料的主角。M、W、X、Y、Z形成的化合物的结构如图所示。下列说法正确的是
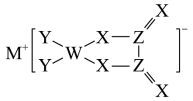
| A.M的单质通常保存在煤油中 | B.R的氧化物能溶于Y的氢化物的水溶液 |
| C.图中W原子不满足8电子稳定结构 | D.X、Y、Z的最简单氢化物的沸点:Y>X>Z |
您最近半年使用:0次
7 . 新冠肺炎疫情仍在全球肆虐,消毒消杀是做好疫情防控的一项关键性工作。ClO2、84消毒液等含氯消毒剂和臭氧等活性氧消毒剂均是应用广泛的消毒试剂。工业上制取ClO2的化学反应为:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。下列说法正确的是
| A.SO2在反应中得到电子 |
| B.NaClO3是氧化剂,在该反应中发生氧化反应 |
| C.氧化产物和还原产物的物质的量之比为:1:2 |
| D.生成224 mL ClO2时转移电子数为0.01NA |
您最近半年使用:0次
名校
8 . 常温下,下列各组离子在指定溶液中一定不能大量共存的是
A.0.1mol/L NaOH溶液:Na+、K+、CO 、NO 、NO |
| B.无色透明的溶液中:K+、Mg2+、SCN-、Cl- |
C.与Al反应能放出H2的溶液中:K+、Mg2+、NO 、SO 、SO |
D.能使石蕊变红的溶液中:NH 、Fe2+、I-、SO 、Fe2+、I-、SO |
您最近半年使用:0次
名校
解题方法
9 . 酸性条件下,FeS2催化氧化反应的化学方程式为2FeS2+7O2+2H2O=2Fe2++4SO +4H+该反应的物质间转化如图所示。下列分析正确的是
+4H+该反应的物质间转化如图所示。下列分析正确的是
 +4H+该反应的物质间转化如图所示。下列分析正确的是
+4H+该反应的物质间转化如图所示。下列分析正确的是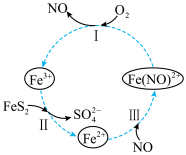
| A.黄铁矿催化氧化反应中NO是中间产物 |
| B.Fe3+是总反应的催化剂 |
| C.反应III是氧化还原反应 |
| D.反应I的离子方程式为4Fe(NO)2++O2+4H+=4Fe3++4NO+2H2O |
您最近半年使用:0次
名校
解题方法
10 . NaBO3·4H2O的阴离子结构如图所示。硼砂(Na2B4O7)与氢氧化钠的混合溶液中加入双氧水可以制备NaBO3·4H2O。下列说法正确的是
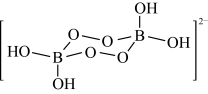
| A.硼砂与氢氧化钠、双氧水的反应为氧化还原反应 |
| B.NaBO3·4H2O不具有杀菌消毒功能与漂白性 |
| C.用浓硫酸处理NaBO3·4H2O可以得到O2 |
| D.分别向同体积的硼砂稀溶液和蒸馏水中加入相同的少量盐酸,前者pH变化大 |
您最近半年使用:0次



