名校
1 . 一节1号干电池可以让1平方米土地上的庄稼颗粒无收,回收电池既可以防止污染又可以变废为宝。废旧锌锰干电池内部的黑色物质A主要含有 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:________ (填化学式)。
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为 ,另一个是
,另一个是________ 。灼烧时,MnOOH与空气中的氧气反应的化学方程式为________________ 。
(3)第III步中为提高反应速率,可以采取的措施有________ (任写一条)。
(4)已知: 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为________________ ;
②操作VI中需要的玻璃仪器有________ ;
③你认为操作VII中检测的方法及现象是________ 时可继续进行操作VIII;
④操作VIII中用无水乙醇洗涤的目的是________ 。
 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为
 ,另一个是
,另一个是(3)第III步中为提高反应速率,可以采取的措施有
(4)已知:
 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: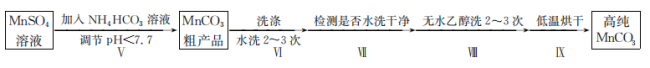
 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为②操作VI中需要的玻璃仪器有
③你认为操作VII中检测的方法及现象是
④操作VIII中用无水乙醇洗涤的目的是
您最近半年使用:0次
名校
2 . 下列实验“操作和现象”与“结论”对应关系正确的是
操作 | 现象 | 结论 | |
A. | 向NaBr溶液中滴入少量氯水和苯,振荡、静置 | 溶液上层呈橙色 | 还原性: |
B. | 将氯气缓缓通入到紫色的石蕊溶液中 | 石蕊溶液先变红后褪色 | 氯气与水反应生成了酸性物质和漂白性物质 |
C. | 将装满氯水的圆底烧瓶倒置在盛有水的水槽中,日光照射 | 烧瓶内有气泡生成 | 日光照射时,逸出的气体只可能是 |
D. | 分别加热 和 和 固体 固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 .  能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备
能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备 的原理为
的原理为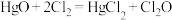 ,装置如图所示。
,装置如图所示。 的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;②
的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;② 与有机物、还原剂接触或加热时会发生燃烧并爆炸。
与有机物、还原剂接触或加热时会发生燃烧并爆炸。
下列说法中正确的是
 能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备
能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备 的原理为
的原理为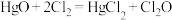 ,装置如图所示。
,装置如图所示。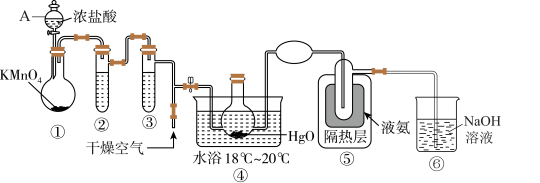
 的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;②
的熔点为116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;② 与有机物、还原剂接触或加热时会发生燃烧并爆炸。
与有机物、还原剂接触或加热时会发生燃烧并爆炸。下列说法中正确的是
A.装置②中盛装的试剂是浓硫酸,用来干燥 |
| B.装置④与⑤之间可用橡胶管连接 |
C. 易液化,装置⑤中的液氨只能冷凝 易液化,装置⑤中的液氨只能冷凝 ,因此从装置⑤中逸出气体的主要成分是 ,因此从装置⑤中逸出气体的主要成分是 |
D.通入干燥空气的目的是将生成的 稀释,减小爆炸危险 稀释,减小爆炸危险 |
您最近半年使用:0次
名校
解题方法
4 . 下列各组离子或分子在给定条件的溶液中可能大量共存的是
A.加入铝片有大量氢气产生的溶液中: 、 、 、 、 、 、 |
B.在0.1mol/L的盐酸中: 、 、 、 、 、 、 |
C.在强碱性溶液中: 、 、 、 、 、 、 |
D.碱性无色溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
名校
5 . NA代表阿伏加德罗常数的值,以下说法正确的是
| A.将足量Zn与100mL18mol/L浓硫酸反应,生成224mL气体,转移电子为0.02NA |
| B.在标准状况下,22.4LHF所含的原子总数为2NA |
C.1mol 固体中含离子总数与1mol 固体中含离子总数与1mol 固体中含离子总数之比为 固体中含离子总数之比为 |
D.1mol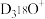 (其中D代表重氢原子符号)中含有的中子数为10NA (其中D代表重氢原子符号)中含有的中子数为10NA |
您最近半年使用:0次
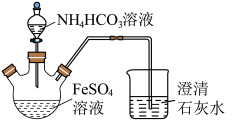
6 . 碳酸亚铁(FeCO3)难溶于水,常用于制取铁盐或补血剂。一种FeCO3的制备装置如图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得FeCO3沉淀。______________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是___________ 。
(3)FeCO3在潮湿的空气中会转化为Fe(OH)3并进步转化为Fe2O3。写出FeCO3在潮湿的空气中转化为Fe(OH)3的化学方程式:__________________ 。
(4)某FeCO3固体被部分氧化,为测定其中Fe3+的质量分数,现进行如下实验:称取5.000g固体样品,加足量盐酸溶解,将溶液稀释至100mL,量取20.00mL该溶液,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定,当滴定至终点时消耗Na2S2O3溶液20.00mL。已知实验过程中发生反应如下:2Fe3++2I-=2Fe2++I2,I2+2S2O =S4O
=S4O +2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
+2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程_________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是
(3)FeCO3在潮湿的空气中会转化为Fe(OH)3并进步转化为Fe2O3。写出FeCO3在潮湿的空气中转化为Fe(OH)3的化学方程式:
(4)某FeCO3固体被部分氧化,为测定其中Fe3+的质量分数,现进行如下实验:称取5.000g固体样品,加足量盐酸溶解,将溶液稀释至100mL,量取20.00mL该溶液,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定,当滴定至终点时消耗Na2S2O3溶液20.00mL。已知实验过程中发生反应如下:2Fe3++2I-=2Fe2++I2,I2+2S2O
 =S4O
=S4O +2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
+2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
您最近半年使用:0次
7 . AgCl可溶于氨水生成Ag(NH3)2Cl,Ag(NH3)2Cl与NH3反应可生成Ag。反应如下:4Ag(NH3)2Cl + N2H4 + 4H2O = 4Ag↓ + N2↑ + 4NH4Cl + 4NH3·H2O。下列关于该反应说法正确的是
| A.Ag(NH3)2Cl发生氧化反应 |
| B.还原性:N2H4<Ag |
C.N2H4的结构式为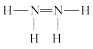 |
| D.每生成标准状况下11.2LN2,反应中转移2mol电子 |
您最近半年使用:0次
名校
8 . 配平方程式并标出电子转移方向及数目___________ 。
___________ ___________
___________ ___________
___________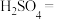 ___________
___________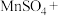 ___________
___________ ___________
___________ ___________
___________
___________
 ___________
___________ ___________
___________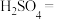 ___________
___________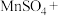 ___________
___________ ___________
___________ ___________
___________
您最近半年使用:0次
名校
9 . 下列叙述正确的
A.区别 和葡萄糖的方法是熔融状态下能否导电 和葡萄糖的方法是熔融状态下能否导电 |
B. 中含有共价键,所以 中含有共价键,所以 属于共价化合物 属于共价化合物 |
| C.非金属元素组成的化合物中只含共价键 |
| D.某纯净物在常温常压下为气体,则组成该物质的微粒一定含共价键 |
您最近半年使用:0次
名校
解题方法
10 . 下列有关化学用语表示正确的是
A.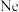 和 和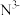 的结构示意图均为: 的结构示意图均为: | B.叠氮酸钠的分子式是: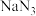 |
C.氨气的空间填充模型: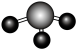 | D.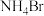 的电子式: 的电子式: |
您最近半年使用:0次



