解题方法
1 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液;②H2O2(在水中一部分可以电离出阴、阳离子);③ClO2;④O3;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号),“84”消毒液中有效成分的电离方程式为___________ ,双氧水的电子式为___________ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”),若1 mol NaClO参加反应,转移电子数___________ (阿伏加德罗常数为NA)。
②若混合使用“洁厕灵”(主要成分为盐酸)与“84”消毒液会产生氯气。原因是(用离子方程式表示)___________ 。
(3)ClO2在杀菌消毒过程中会产生亚氯酸盐(ClO ),需将其转化为Cl− 除去,下列试剂可将ClO
),需将其转化为Cl− 除去,下列试剂可将ClO 转化为Cl− 的是
转化为Cl− 的是___________ (填标号)。
a.FeSO4 b.O3 c.KMnO4 d.Na2CO3
(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
②若混合使用“洁厕灵”(主要成分为盐酸)与“84”消毒液会产生氯气。原因是(用离子方程式表示)
(3)ClO2在杀菌消毒过程中会产生亚氯酸盐(ClO
 ),需将其转化为Cl− 除去,下列试剂可将ClO
),需将其转化为Cl− 除去,下列试剂可将ClO 转化为Cl− 的是
转化为Cl− 的是a.FeSO4 b.O3 c.KMnO4 d.Na2CO3
您最近半年使用:0次
解题方法
2 . 铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为_______ ,发生反应的离子方程式为_______ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是_______ 。
(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为_______ 。
(4)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:_______ 。
② 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为_______ 。
③滤液II中溶质的用途之一是_______ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为
(4)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:
②
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为③滤液II中溶质的用途之一是
您最近半年使用:0次
解题方法
3 . 现有下列10种物质:①液态HCl;② 固体;③NaCl溶液;④
固体;③NaCl溶液;④ ;⑤蔗糖溶液;⑥
;⑤蔗糖溶液;⑥ 粉末;⑦稀硫酸;⑧氨水;⑨
粉末;⑦稀硫酸;⑧氨水;⑨ ;⑩Zn。
;⑩Zn。
(1)物质中属于电解质的有_______ (填序号,下同),能导电的有_______ 。
(2)写出⑨与⑩在水溶液中反应的离子方程式:_______ 。
(3)写出过氧化钠与④反应的化学方程式并用双线桥表示其得失电子情况:_______ 。
(4)同温、同压下等质量的 和CO,它们所占的体积比为
和CO,它们所占的体积比为_______ 。
(5)将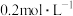 的
的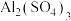 和
和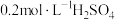 溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
_______  。
。
(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为____ 。
 固体;③NaCl溶液;④
固体;③NaCl溶液;④ ;⑤蔗糖溶液;⑥
;⑤蔗糖溶液;⑥ 粉末;⑦稀硫酸;⑧氨水;⑨
粉末;⑦稀硫酸;⑧氨水;⑨ ;⑩Zn。
;⑩Zn。(1)物质中属于电解质的有
(2)写出⑨与⑩在水溶液中反应的离子方程式:
(3)写出过氧化钠与④反应的化学方程式并用双线桥表示其得失电子情况:
(4)同温、同压下等质量的
 和CO,它们所占的体积比为
和CO,它们所占的体积比为(5)将
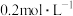 的
的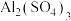 和
和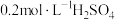 溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中
 。
。(6)印刷电路板是电子元器件电气连接的提供者,制作印刷电路板主要原料是铜板。在制作过程中产生的铜粉,用稀硫酸和过氧化氢混合溶液溶解,可生成硫酸铜和水,其反应的离子方程式为
您最近半年使用:0次
解题方法
4 . 下表是元素周期表的一部分。请按要求回答下列问题:___________ ,⑦的最高价氧化物对应水化物的化学式___________ 。
(2)上述所列元素最高价氧化物对应水化物碱性最强的是___________ (填化学式)。
(3)写出由上述所列元素形成的18电子的双原子分子的化学式___________ 。
(4)下列说法不正确的是___________。
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式___________ 。
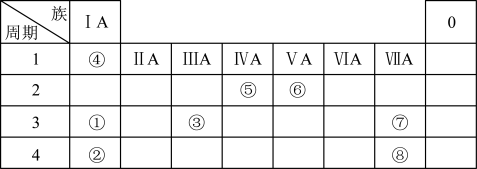
(2)上述所列元素最高价氧化物对应水化物碱性最强的是
(3)写出由上述所列元素形成的18电子的双原子分子的化学式
(4)下列说法不正确的是___________。
| A.⑥形成的最简单氢化物比⑤形成的最简单氢化物的稳定性高 |
| B.元素最高正价与最低负价绝对值相等的元素一定处于第ⅣA族 |
| C.第5周期第ⅦA族元素的原子序数为53 |
| D.周期表中当某元素的周期序数大于其主族序数时,该元素可能属于金属或非金属 |
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式
您最近半年使用:0次
5 . 按要求回答问题:
(1)①铁红的化学式是___________ ;②氨气的电子式___________ 。
(2)NaHCO3在水中的电离方程式:___________ 。
(3)写出铁与水蒸气反应的化学方程式为并用单线桥法表示出该反应中电子转移的方向和数目___________ 。
(4)关于固体NaHSO4的组成和性质的表述正确的是:___________ (填写符合要求的序号)。
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电
(1)①铁红的化学式是
(2)NaHCO3在水中的电离方程式:
(3)写出铁与水蒸气反应的化学方程式为并用单线桥法表示出该反应中电子转移的方向和数目
(4)关于固体NaHSO4的组成和性质的表述正确的是:
①电解质;②非电解质;③酸;④碱;⑤盐;⑥导电
您最近半年使用:0次
解题方法
6 . 一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如下。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)__________________ 。
(2)④所代表的物质是______ (用化学式表示)。
(3)操作方法a、b、c中是过滤的是______ (填序号)。
(4)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是_________________ 。
(5)试剂⑥是 时,发生反应的化学方程式是
时,发生反应的化学方程式是__________________ 。
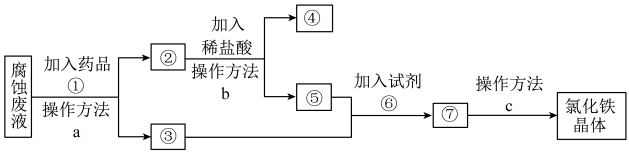
(2)④所代表的物质是
(3)操作方法a、b、c中是过滤的是
(4)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)试剂⑥是
 时,发生反应的化学方程式是
时,发生反应的化学方程式是
您最近半年使用:0次
名校
7 . 配平方程式并标出电子转移方向及数目___________ 。
___________ ___________
___________ ___________
___________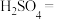 ___________
___________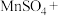 ___________
___________ ___________
___________ ___________
___________
___________
 ___________
___________ ___________
___________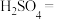 ___________
___________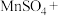 ___________
___________ ___________
___________ ___________
___________
您最近半年使用:0次
名校
解题方法
8 . X、Y、Z、W、M、N是原子序数依次增大的短周期主族元素,它们的结构或性质信息如表所示,请回答下列问题:
(1)M在元素周期表中的位置为________ ,请写出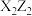 的电子式:
的电子式:________ 。
(2)Z、W、M、N的简单离子半径由大到小的顺序为______________ (写离子符号)。
(3)
________ (填“是”或“不是”)电解质,向其水溶液中滴加少量M的盐酸盐溶液,发生反应的离子方程式为__________________ 。
(4)Y的最简单氢化物与过量的N的最高价氧化物对应的水化物反应得到一种酸式盐a,a在水中的电离方程式为_______________ ,向a溶液中滴加少量 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_____________________ 。
元素 | 结构或性质信息 |
X | 元素周期表中,X的半径最小 |
Y | K层电子数比L层少3 |
Z | 最外层电子数是其周期数的3倍 |
W | 其单质的氧化性最强 |
M | W的核外电子数是M的最外层电子数的3倍 |
N | 最外层电子数是其周期数的2倍 |
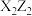 的电子式:
的电子式:(2)Z、W、M、N的简单离子半径由大到小的顺序为
(3)

(4)Y的最简单氢化物与过量的N的最高价氧化物对应的水化物反应得到一种酸式盐a,a在水中的电离方程式为
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
您最近半年使用:0次
名校
9 . 近年来,利用SRB(硫酸盐还原菌)治理废水中的有机物、 及重金属污染取得了新的进展。
及重金属污染取得了新的进展。
(1)图1表示 和
和 在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样
在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样 ,在SRB的作用下,废水中的有机物(主要为
,在SRB的作用下,废水中的有机物(主要为 )将
)将 还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:
还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:____________ 。 还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。______ 。
②负极附近的 的变化:
的变化:______ (“减小”或“增大”)。
(3)SRB可用于处理废水中含重金属锑(Sb)的离子。
①通过两步反应将 转化为
转化为 除去,转化过程中有单质生成。完成第一步反应的离子方程式。
除去,转化过程中有单质生成。完成第一步反应的离子方程式。
第一步________
______ ______
______ _______+______↓+______
_______+______↓+______
第二步:
 及重金属污染取得了新的进展。
及重金属污染取得了新的进展。(1)图1表示
 和
和 在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样
在水溶液中各种微粒物质的量分数随pH的变化曲线。某地下水样 ,在SRB的作用下,废水中的有机物(主要为
,在SRB的作用下,废水中的有机物(主要为 )将
)将 还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化:
还原为-2价硫的化合物,请用离子方程式表示该过程中的化学变化: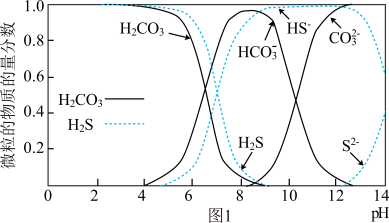
 还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
还能用于构造微生物电池,某pH下该微生物燃料电池的工作原理如图2所示。
②负极附近的
 的变化:
的变化:(3)SRB可用于处理废水中含重金属锑(Sb)的离子。
①通过两步反应将
 转化为
转化为 除去,转化过程中有单质生成。完成第一步反应的离子方程式。
除去,转化过程中有单质生成。完成第一步反应的离子方程式。第一步
______
 ______
______ _______+______↓+______
_______+______↓+______
第二步:

您最近半年使用:0次
解题方法
10 . 特殊的分散系——胶体
把一种或多种物质分散在另一种物质中所得到的体系称为分散系,接照分散质的大小可将分散系分为溶液、胶体和浊液三类。三者之间无明显界限。胶体是物质的一种分散状态,比较稳定,外观上胶体溶液不浑浊,用肉眼或普通显微镜均不能辨别。很多蛋白质、淀粉、血液、淋巴液等都属于胶体。胶体还可以按照分散剂的状态分为固溶胶如有色玻璃、气溶胶如雾、烟和液溶胶如FeOH3胶体。1.胶体可以稳定存在的主要原因是______。
| A.胶体粒子直径在1~100nm之间 | B.胶体具有丁达尔现象 |
| C.胶粒带电 | D.胶体外观均匀 |
| A.在豆浆中加入盐卤做豆腐 |
| B.河流入海处易形成沙洲 |
| C.一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路 |
| D.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
| A.蛋白质溶液 | B.氨水 | C.食盐水 | D.酒精溶液 |
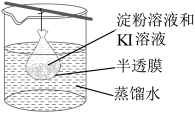
5.在小烧杯中加入20mL蒸馏水加热煮沸后,向沸水申滴入几滴饱和的FeCl3溶液,继续煮沸至溶液呈色即制得FeOH3胶体。
①写出上述胶体制备的化学反应方程式
②取制得的FeOH3胶体装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,说明氢氧化铁胶粒带
③另取制得的FeOH3胶体于洁净的试管中,向其中逐滴滴加过量稀硫酸,边滴边振荡,观察到的现象是
您最近半年使用:0次



