名校
1 . 2021年《科学》杂志刊登了用 为原料,不依赖光合作用,可人工合成淀粉,其前两步的合成路线如下。用
为原料,不依赖光合作用,可人工合成淀粉,其前两步的合成路线如下。用 表示阿伏加德罗常数值,下列说法正确的是。
表示阿伏加德罗常数值,下列说法正确的是。

 为原料,不依赖光合作用,可人工合成淀粉,其前两步的合成路线如下。用
为原料,不依赖光合作用,可人工合成淀粉,其前两步的合成路线如下。用 表示阿伏加德罗常数值,下列说法正确的是。
表示阿伏加德罗常数值,下列说法正确的是。
A. 中含有σ键的数目为 中含有σ键的数目为 |
B. 的甲醇水溶液中含有的 的甲醇水溶液中含有的 数为 数为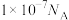 |
C.步骤Ⅱ中每消耗 转移的电子数为 转移的电子数为 |
D.90g甲醛和葡萄糖的混合物中含有的氧原子数为 |
您最近半年使用:0次
2023-02-03更新
|
472次组卷
|
2卷引用:广东省茂名市第一中学2022-2023学年高三上学期期末化学诊断检测题
解题方法
2 . 2021年9月,我国科学家宣布首次在实验室由CO2人工合成淀粉(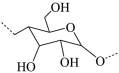 ),实现了颠覆性的突破。下列说法不正确的是
),实现了颠覆性的突破。下列说法不正确的是
 ),实现了颠覆性的突破。下列说法不正确的是
),实现了颠覆性的突破。下列说法不正确的是| A.人工合成的淀粉溶液不能产生丁达尔效应 |
| B.该方法为推进“碳达峰”和“碳中和”目标实现的技术路线提供了一种新思路 |
| C.由CO2合成淀粉过程中有碳碳键形成 |
| D.合成淀粉过程中还需要氢气等原料 |
您最近半年使用:0次
名校
解题方法
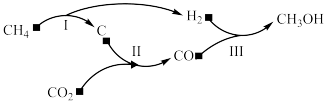
3 . 以天然气为原料经由合成气(CO、 )制化学品是目前天然气转化利用的主导技术路线。制备
)制化学品是目前天然气转化利用的主导技术路线。制备 的反应转化关系如图所示。设
的反应转化关系如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 )制化学品是目前天然气转化利用的主导技术路线。制备
)制化学品是目前天然气转化利用的主导技术路线。制备 的反应转化关系如图所示。设
的反应转化关系如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.用1 mol  理论上能生产标准状况下 理论上能生产标准状况下 |
B.等物质的量的 和 和 , , 的质子数比 的质子数比 多 多 |
C.44 g  气体和44 g 气体和44 g  与CO的混合气体,所含C原子数均为 与CO的混合气体,所含C原子数均为 |
D.用 制备合成气的反应中,若生成1 mol CO,反应转移电子数为 制备合成气的反应中,若生成1 mol CO,反应转移电子数为 |
您最近半年使用:0次
解题方法
4 . 已知短周期元素 、
、 、
、 、
、 、
、 分布在三个周期,
分布在三个周期, 、
、 最外层电子数相同,物质
最外层电子数相同,物质 由原子序数依次增大的元素
由原子序数依次增大的元素 、
、 、
、 组成,其中
组成,其中 的简单离子半径在同周期中最小,
的简单离子半径在同周期中最小, 、
、 、
、 简单离子的核外电子排布相同,物质
简单离子的核外电子排布相同,物质 的结构式如下图所示:
的结构式如下图所示:
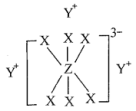
回答下列问题:
(1) 、
、 元素的中文名称为徐寿确定并使用至今,
元素的中文名称为徐寿确定并使用至今, 在周期表中的位置是
在周期表中的位置是___________ ,写出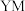 的电子式:
的电子式:___________ 。
(2) 、
、 、
、 、
、 简单离子的半径由大到小的顺序(用对应离子符号表示):
简单离子的半径由大到小的顺序(用对应离子符号表示):___________ 。
(3)在 ,与
,与 的混合液中,通入足量
的混合液中,通入足量 ,是工业制取
,是工业制取 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:___________ 。
(4)镓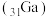 与
与 为同主族元素,氮化镓
为同主族元素,氮化镓 和砷化镓
和砷化镓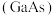 作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是___________ 。
a. 位于元素周期表第四周期ⅣA族
位于元素周期表第四周期ⅣA族
b. 为新型无机非金属材料
为新型无机非金属材料
c. 的最高价氧化物对应水化物的碱性比
的最高价氧化物对应水化物的碱性比 元素最高价氧化物对应水化物的碱性强
元素最高价氧化物对应水化物的碱性强
d.酸性:
②废弃的含 的半导体材料可以用浓硝酸溶解,生成
的半导体材料可以用浓硝酸溶解,生成 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为___________ 。
(5) 是有机合成的重要还原剂,其合成路线如图所示
是有机合成的重要还原剂,其合成路线如图所示
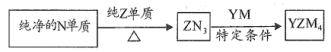
利用 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。
①其反应的化学方程式为___________ 。
②现设计如图四种装置测定 样品的纯度(假设杂质不参与反应)。
样品的纯度(假设杂质不参与反应)。
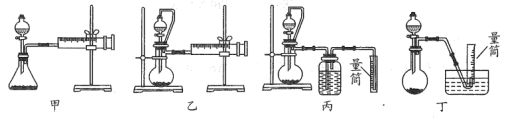
从简约性、准确性考虑,最适宜的方案是___________ (填编号)。
③取样品 ,若实验测得氢气的体积为
,若实验测得氢气的体积为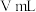 (标准状态),则
(标准状态),则 样品纯度为
样品纯度为___________ (用代数式表示)。
 、
、 、
、 、
、 、
、 分布在三个周期,
分布在三个周期, 、
、 最外层电子数相同,物质
最外层电子数相同,物质 由原子序数依次增大的元素
由原子序数依次增大的元素 、
、 、
、 组成,其中
组成,其中 的简单离子半径在同周期中最小,
的简单离子半径在同周期中最小, 、
、 、
、 简单离子的核外电子排布相同,物质
简单离子的核外电子排布相同,物质 的结构式如下图所示:
的结构式如下图所示: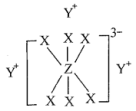
回答下列问题:
(1)
 、
、 元素的中文名称为徐寿确定并使用至今,
元素的中文名称为徐寿确定并使用至今, 在周期表中的位置是
在周期表中的位置是 的电子式:
的电子式:(2)
 、
、 、
、 、
、 简单离子的半径由大到小的顺序(用对应离子符号表示):
简单离子的半径由大到小的顺序(用对应离子符号表示):(3)在
 ,与
,与 的混合液中,通入足量
的混合液中,通入足量 ,是工业制取
,是工业制取 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:(4)镓
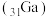 与
与 为同主族元素,氮化镓
为同主族元素,氮化镓 和砷化镓
和砷化镓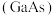 作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。①下列有关说法正确的是
a.
 位于元素周期表第四周期ⅣA族
位于元素周期表第四周期ⅣA族b.
 为新型无机非金属材料
为新型无机非金属材料c.
 的最高价氧化物对应水化物的碱性比
的最高价氧化物对应水化物的碱性比 元素最高价氧化物对应水化物的碱性强
元素最高价氧化物对应水化物的碱性强d.酸性:

②废弃的含
 的半导体材料可以用浓硝酸溶解,生成
的半导体材料可以用浓硝酸溶解,生成 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为(5)
 是有机合成的重要还原剂,其合成路线如图所示
是有机合成的重要还原剂,其合成路线如图所示
利用
 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。①其反应的化学方程式为
②现设计如图四种装置测定
 样品的纯度(假设杂质不参与反应)。
样品的纯度(假设杂质不参与反应)。
从简约性、准确性考虑,最适宜的方案是
③取样品
 ,若实验测得氢气的体积为
,若实验测得氢气的体积为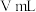 (标准状态),则
(标准状态),则 样品纯度为
样品纯度为
您最近半年使用:0次
名校
解题方法
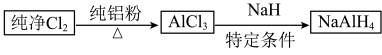
5 . 铝氢化钠( )是有机合成的重要还原剂,其合成路线如下:
)是有机合成的重要还原剂,其合成路线如下:
(1)已知 的熔点为190℃,沸点为178℃,在潮湿的空气中易水解。某实验小组利用下图中的装置制备无水
的熔点为190℃,沸点为178℃,在潮湿的空气中易水解。某实验小组利用下图中的装置制备无水 (部分夹持装置略去)。
(部分夹持装置略去)。
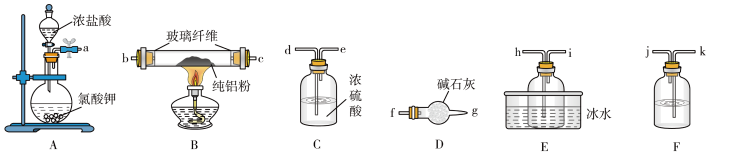
①圆底烧瓶中发生反应的化学方程式为___________ 。
②按气流方向连接各仪器接口,顺序为a→___________ (填接口字母)。
③装置A盛放浓盐酸的仪器名称为___________ ,装置D的作用是___________ 。
(2) 与NaH反应时,需先将
与NaH反应时,需先将 溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是
溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是___________ 。
(3)通过测定铝氢化钠与水反应生成氢气的体积来测定铝氢化钠样品的纯度。
①铝氢化钠与水反应的化学方程式为___________ 。
②设计如下四种装置(部分夹持装置略去)测定铝氢化钠样品的纯度(杂质只有氢化钠)。从简约性、准确性考虑,最恰当的装置是___________ (填编号)。
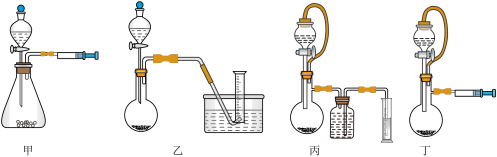
 )是有机合成的重要还原剂,其合成路线如下:
)是有机合成的重要还原剂,其合成路线如下:
(1)已知
 的熔点为190℃,沸点为178℃,在潮湿的空气中易水解。某实验小组利用下图中的装置制备无水
的熔点为190℃,沸点为178℃,在潮湿的空气中易水解。某实验小组利用下图中的装置制备无水 (部分夹持装置略去)。
(部分夹持装置略去)。
①圆底烧瓶中发生反应的化学方程式为
②按气流方向连接各仪器接口,顺序为a→
③装置A盛放浓盐酸的仪器名称为
(2)
 与NaH反应时,需先将
与NaH反应时,需先将 溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是
溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是(3)通过测定铝氢化钠与水反应生成氢气的体积来测定铝氢化钠样品的纯度。
①铝氢化钠与水反应的化学方程式为
②设计如下四种装置(部分夹持装置略去)测定铝氢化钠样品的纯度(杂质只有氢化钠)。从简约性、准确性考虑,最恰当的装置是

您最近半年使用:0次
解题方法
6 . 铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成路线如下:
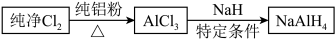
(1)已知AlCl3的熔点为190℃,沸点为178℃,在潮湿的空气中易水解。某实验小组利用下图中装置制备无水AlCl3(夹持装置略去)。
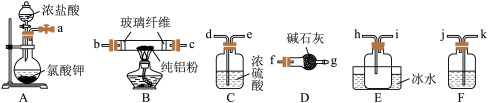
①圆底烧瓶中发生反应的化学方程式为___________ 。
②按气流方向连接各仪器接口,顺序为a→___________ →b→c→h→i→f→g(填接口字母)。
③装置A盛放浓盐酸的仪器名称为___________ ,装置F中应盛放的试剂是___________ ,装置D的作用是___________ 。
(2)AlCl3与NaH反应时,需先将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是___________ 。
(3)通过测定铝氢化钠与水反应生成氢气的体积来测定铝氢化钠样品的纯度。
①铝氢化钠与水反应的化学方程式为___________ 。
②设计如下四种装置(夹持装置略去)测定铝氢化钠样品的纯度(杂质只有氢化钠)。从简约性、准确性考虑,最恰当的装置是___________ (填编号)。
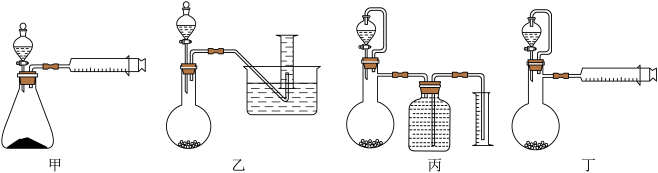
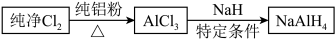
(1)已知AlCl3的熔点为190℃,沸点为178℃,在潮湿的空气中易水解。某实验小组利用下图中装置制备无水AlCl3(夹持装置略去)。

①圆底烧瓶中发生反应的化学方程式为
②按气流方向连接各仪器接口,顺序为a→
③装置A盛放浓盐酸的仪器名称为
(2)AlCl3与NaH反应时,需先将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是
(3)通过测定铝氢化钠与水反应生成氢气的体积来测定铝氢化钠样品的纯度。
①铝氢化钠与水反应的化学方程式为
②设计如下四种装置(夹持装置略去)测定铝氢化钠样品的纯度(杂质只有氢化钠)。从简约性、准确性考虑,最恰当的装置是

您最近半年使用:0次
名校
解题方法
7 . 以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线。制备 的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
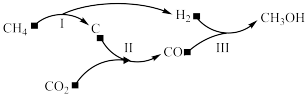
 的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
A.用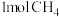 理论上能生产的 理论上能生产的 中含有极性键的数目为4 NA 中含有极性键的数目为4 NA |
B.等物质的量的 和 和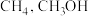 的质子数比 的质子数比 多8 NA 多8 NA |
C.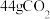 气体和 气体和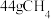 与 与 的混合气体,所含C原子数均为NA 的混合气体,所含C原子数均为NA |
D.用 制备合成气的反应中,若生成 制备合成气的反应中,若生成 ,反应转移电子数为3 NA ,反应转移电子数为3 NA |
您最近半年使用:0次
2021-11-30更新
|
537次组卷
|
3卷引用:吉林省东北师范大学附属中学2021-2022学年高三上学期一模考试化学试题
2024高三下·全国·专题练习
解题方法
8 . 氯化亚铜是一种应用较广的催化剂,易水解,微溶于水,不溶于乙醇。以低品位铜矿砂(主要成分 )为原料制备氯化亚铜的路线如下:
)为原料制备氯化亚铜的路线如下:

(1)“酸溶1”步骤中发生反应的化学方程式为___________ 。
(2)“除锰”步骤中Mn2+转化为MnCO3沉淀,CuSO4转变为Cu(NH3)4CO3留在溶液中。则“除锰”步骤中发生反应的离子方程式为___________ 。
(3)“合成”步骤加入Na2SO3的速率不宜过快,否则会产生___________ 气体(写化学式),除可能与酸溶时硫酸过量有关,还可能的原因是___________ 。(用离子方程式表示)。
 )为原料制备氯化亚铜的路线如下:
)为原料制备氯化亚铜的路线如下:
(1)“酸溶1”步骤中发生反应的化学方程式为
(2)“除锰”步骤中Mn2+转化为MnCO3沉淀,CuSO4转变为Cu(NH3)4CO3留在溶液中。则“除锰”步骤中发生反应的离子方程式为
(3)“合成”步骤加入Na2SO3的速率不宜过快,否则会产生
您最近半年使用:0次
名校
9 . 2021年,英国剑桥大学Dominic S.Wright课题组设计了一种新型电池中电解质(结构如图所示)的合成路线。已知X、Y、Z为原子序数依次增大的短周期主族元素,三者的核外电子数之和等于35,Y与Z位于同一周期,则下列说法正确的是


| A.简单离子的半径:X>Y |
| B.Z的最高价氧化物对应水化物是强酸 |
| C.工业上常采用电解Y的氧化物冶炼单质Y |
| D.该化合物阴离子中各原子均满足8电子稳定结构 |
您最近半年使用:0次
名校
10 . 2021年,英国剑桥大学Dominic S.Wright课题组设计了一种新型电池中电解质(结构如图所示)的合成路线。已知X、Y、Z为原子序数依次增大的短周期主族元素,X的电负性为4,三者的核外电子数之和等于35,Y与Z位于同一周期,则下列说法正确的是
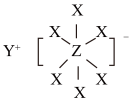

| A.简单离子的半径:X>Y |
| B.Z的最高价氧化物对应水化物是强酸 |
| C.工业上常采用电解Y的氧化物冶炼单质Y |
| D.该化合物阴离子中各原子均满足8电子稳定结构 |
您最近半年使用:0次
2022-05-30更新
|
283次组卷
|
6卷引用:山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题
山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题(已下线)专题06物质结构元素周期律-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题06物质结构元素周期律-2022年高考真题+模拟题汇编(全国卷)(已下线)专题06物质结构元素周期律-三年(2020~2022)高考真题汇编(全国卷)北京市海淀区中关村中学2022届高三下学期三模化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)



