名校
解题方法
1 . 碳酸亚铁难溶于水,在医学常用于补铁剂的基础原料,某实验小组同学拟用下图装置先制备 ,再用
,再用 与葡萄糖酸反应进一步反应,合成易溶于水的补铁剂葡萄糖酸亚铁
与葡萄糖酸反应进一步反应,合成易溶于水的补铁剂葡萄糖酸亚铁 。
。

请回答下列问题:
(1)与普通分液漏斗对比,分液漏斗 的优点是
的优点是___________ 。
(2)按上图连接好装置,检查气密性后加入药品,先打开 和
和 ,关闭
,关闭 。
。
①b中的实验现象为___________ 。
②一段时间后,关闭___________ ,打开___________ (选填“ ”、“
”、“ ”或“
”或“ ”),观察到b中的溶液会流入c中,同时c中析出
”),观察到b中的溶液会流入c中,同时c中析出 沉淀。
沉淀。
③b中产生的气体的作用是___________ 。
(3) 中制得的碳酸亚铁在空气中过滤时间较长时,表面会变为红褐色,用化学方程式说明其原因
中制得的碳酸亚铁在空气中过滤时间较长时,表面会变为红褐色,用化学方程式说明其原因___________ 。
(4)有同学提出使用 溶液代替
溶液代替 溶液也能制得的碳酸亚铁,请写出离子方程式
溶液也能制得的碳酸亚铁,请写出离子方程式___________ 。
(5)将葡萄糖酸与碳酸亚铁混合,须将溶液的 调节至
调节至 ,其原因是
,其原因是___________ 。
 ,再用
,再用 与葡萄糖酸反应进一步反应,合成易溶于水的补铁剂葡萄糖酸亚铁
与葡萄糖酸反应进一步反应,合成易溶于水的补铁剂葡萄糖酸亚铁 。
。
请回答下列问题:
(1)与普通分液漏斗对比,分液漏斗
 的优点是
的优点是(2)按上图连接好装置,检查气密性后加入药品,先打开
 和
和 ,关闭
,关闭 。
。①b中的实验现象为
②一段时间后,关闭
 ”、“
”、“ ”或“
”或“ ”),观察到b中的溶液会流入c中,同时c中析出
”),观察到b中的溶液会流入c中,同时c中析出 沉淀。
沉淀。③b中产生的气体的作用是
(3)
 中制得的碳酸亚铁在空气中过滤时间较长时,表面会变为红褐色,用化学方程式说明其原因
中制得的碳酸亚铁在空气中过滤时间较长时,表面会变为红褐色,用化学方程式说明其原因(4)有同学提出使用
 溶液代替
溶液代替 溶液也能制得的碳酸亚铁,请写出离子方程式
溶液也能制得的碳酸亚铁,请写出离子方程式(5)将葡萄糖酸与碳酸亚铁混合,须将溶液的
 调节至
调节至 ,其原因是
,其原因是
您最近一年使用:0次
2021-10-20更新
|
179次组卷
|
2卷引用:甘肃省兰州市第一中学2021-2022学年高三上学期第一次月考(10月)化学试题
2 . 亚硝酰氯(NOCl)常用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成亚硝酰氯。
已知:①NOCl是黄色气体,熔点:—64.5℃,沸点:—5.5℃;NOCl遇水易反应生成一种无氧酸和两种氮的常见氧化物;NOCl对眼睛、皮肤和黏膜有强烈刺激性,具有类似氯气和氮氧化物的毒作用。
②Ag2CrO4是砖红色沉淀。
实验1:制备原料气NO和Cl2
利用如图1所示装置制备纯净的NO和Cl2。
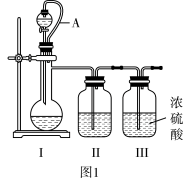
(1)制备纯净的Cl2,烧瓶中反应的化学方程式为___ 。
(2)制备纯净的NO,烧瓶中盛有Cu,装置Ⅱ中盛有___ (填试剂名称);导管A的作用是___ 。
实验2:制备NOCl。
利用实验1中制得的NO和Cl2制备NOCl,装置如图2所示。
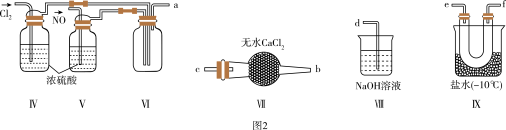
(3)仪器接口的连接顺序为a→___ (按气流从左到右顺序填写)。
(4)装置Ⅳ、Ⅴ除进一步干燥NO和Cl2外,另一作用是____ 。
(5)装置Ⅷ用于吸收尾气,NOCl发生反应的化学方程式为____ 。
实验3:测定NOCl的纯度
将所得亚硝酰氯(NOCl)产品13.5g溶于水,配成250ml该溶液,取出25.00ml该溶液,以K2CrO4溶液为指示剂,用1.0mol/LAgNO3标准溶液滴定至终点,再重复上述实验操作2次,测得三次实验消耗AgNO3标准溶液的平均体积为20.00ml。
(6)达到滴定终点的现象是____ 。
(7)产品中亚硝酰氯(NOCl)的质量分数为___ (保留两位小数)。
已知:①NOCl是黄色气体,熔点:—64.5℃,沸点:—5.5℃;NOCl遇水易反应生成一种无氧酸和两种氮的常见氧化物;NOCl对眼睛、皮肤和黏膜有强烈刺激性,具有类似氯气和氮氧化物的毒作用。
②Ag2CrO4是砖红色沉淀。
实验1:制备原料气NO和Cl2
利用如图1所示装置制备纯净的NO和Cl2。

(1)制备纯净的Cl2,烧瓶中反应的化学方程式为
(2)制备纯净的NO,烧瓶中盛有Cu,装置Ⅱ中盛有
实验2:制备NOCl。
利用实验1中制得的NO和Cl2制备NOCl,装置如图2所示。

(3)仪器接口的连接顺序为a→
(4)装置Ⅳ、Ⅴ除进一步干燥NO和Cl2外,另一作用是
(5)装置Ⅷ用于吸收尾气,NOCl发生反应的化学方程式为
实验3:测定NOCl的纯度
将所得亚硝酰氯(NOCl)产品13.5g溶于水,配成250ml该溶液,取出25.00ml该溶液,以K2CrO4溶液为指示剂,用1.0mol/LAgNO3标准溶液滴定至终点,再重复上述实验操作2次,测得三次实验消耗AgNO3标准溶液的平均体积为20.00ml。
(6)达到滴定终点的现象是
(7)产品中亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
2020-08-21更新
|
443次组卷
|
3卷引用:甘肃省天水市第一中学2021-2022高三上学期第三次考试化学试题



