名校
1 . 六种短周期主族元素A、B、C、D、E、F的原子序数依次增大,A和D同主族,C和F同主族。B、C、D、E的离子均具有相同的电子层结构,E在同周期元素中离子半径最小。A和B、C、F均能形成共价化合物,A和B形成的化合物Y在水中呈碱性,D和F形成的化合物在水中呈中性。下列说法错误的是
| A.简单离子半径:B > D |
| B.简单氢化物水溶液酸性:F > C > B |
| C.D的单质能将E单质从EF3的溶液中置换出来 |
| D.化合物AF与化合物Y可反应生成含有共价键的离子化合物 |
您最近一年使用:0次
名校
解题方法
2 . 现有下列短周期元素的数据(已知Be的原子半径为0.111 nm):
下列说法正确的是
| 元素 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/nm | 0.066 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.070 | 0.086 |
| 最高化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低化合价 | -2 | -3 | -1 | -3 |
| A.③的单质保存在煤油中 |
| B.⑧的最高价氧化物对应的水化物能与⑤的最高价氧化物对应水化物反应 |
| C.简单氢化物稳定性:①>⑦>④ |
| D.②的单质在⑦的单质中燃烧生成的物质中既含有离子键又含有共价键 |
您最近一年使用:0次
名校
3 . Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Q与Z同主族,Y原子最外层电子数是Q原子内层电子数的2倍。下列说法正确的是
| A.单质氧化性:Q<Z | B.最高价含氧酸的酸性:Z>Y |
| C.简单氢化物的沸点:Z>Q | D.熔点:X的单质>X的氧化物 |
您最近一年使用:0次
名校
4 . 一位同学设计了一套用浓盐酸和高锰酸钾固体制取少量氯气并能比较氯气与碘单质氧化性强弱的微型装置,如图所示。
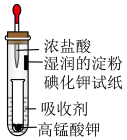
下列说法不正确的是

下列说法不正确的是
| A.吸收剂可以是饱和NaOH溶液 |
| B.湿润的淀粉碘化钾试纸变蓝说明Cl的非金属性强于I |
| C.该实验中浓盐酸体现了还原性和酸性 |
| D.高锰酸钾是共价化合物 |
您最近一年使用:0次
名校
解题方法
5 . X、Y、Z是相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31,下列关于三种元素说法不正确的是
| A.Y元素是O | B.X的原子半径最小 |
| C.简单氢化物沸点最高的是Y | D.Z的单质有多种同素异形体 |
您最近一年使用:0次
6 . 已知NA为阿伏加德罗常数的值,下列说法正确的是
| A.2.0 g H218O与D2O的混合物中所含中子数为NA |
B.235 g核素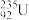 发生裂变反应: 发生裂变反应: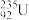 + + 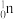 → → 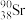 + + 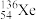 + 10 + 10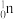 ,净产生的中子( ,净产生的中子(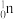 )数为10NA )数为10NA |
| C.标况下,4.48 L CO2分子中含有的共用电子对数为0.4NA |
| D.1.4 g锂单质在足量的氧气中燃烧,生成的产物中含有的非极性键数目为0.1NA |
您最近一年使用:0次
名校
7 . 下列叙述能说明氯元素的非金属性强于硫元素的组合是
①HCl的溶解度比H2S大
②HCl的稳定性比H2S强
③盐酸的酸性比氢硫酸强
④HCl的还原性比H2S强
⑤Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑥HClO4的酸性比H2SO3强
⑦Cl2能与H2S反应生成S
⑧在元素周期表中Cl与S同周期且Cl在S的右侧
⑨Cl2与H2反应比S单质容易
①HCl的溶解度比H2S大
②HCl的稳定性比H2S强
③盐酸的酸性比氢硫酸强
④HCl的还原性比H2S强
⑤Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑥HClO4的酸性比H2SO3强
⑦Cl2能与H2S反应生成S
⑧在元素周期表中Cl与S同周期且Cl在S的右侧
⑨Cl2与H2反应比S单质容易
| A.②④⑦⑧⑨ | B.①④⑤⑥⑦ | C.②③⑥⑦⑨ | D.②⑤⑦⑧⑨ |
您最近一年使用:0次
名校
8 . 下列说法正确的有
①质量数为133、中子数为78的铯原子符号: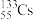
②S2-的结构示意图: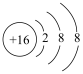
③用电子式表示HCl的形成过程:
④CaCl2的电子式:
⑤次氯酸分子的结构式:H-O-Cl
⑥熔融NaHSO4破坏离子键和共价键
⑦PCl3和CO2均满足8电子稳定结构
①质量数为133、中子数为78的铯原子符号:
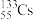
②S2-的结构示意图:

③用电子式表示HCl的形成过程:

④CaCl2的电子式:

⑤次氯酸分子的结构式:H-O-Cl
⑥熔融NaHSO4破坏离子键和共价键
⑦PCl3和CO2均满足8电子稳定结构
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
名校
解题方法
9 . “化学——人类进步的关键”。下列化学知识的说法中正确的有
①任何原子核内均含质子和中子
②门捷列夫根据质子数制作出第一张元素周期表
③科学家在周期表中金属与非金属分界线处找到了半导体材料
④原子序数为22的元素位于元素周期表的第4周期ⅡB族
⑤带相反电荷离子之间的静电吸引叫做离子键
⑥同主族两种元素原子的核外电子数的差值可能为36
⑦同一周期的甲、乙两种元素,甲位于第ⅡA族,序数为x,乙位于第ⅢA族,则乙的序数可能为x+10
⑧砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀酸
⑨Na2O和Na2O2中阴阳离子个数比都是1:2
⑩卤素单质的熔点从F2到I2逐渐升高,碱金属单质的熔点从Li到Cs也逐渐升高
①任何原子核内均含质子和中子
②门捷列夫根据质子数制作出第一张元素周期表
③科学家在周期表中金属与非金属分界线处找到了半导体材料
④原子序数为22的元素位于元素周期表的第4周期ⅡB族
⑤带相反电荷离子之间的静电吸引叫做离子键
⑥同主族两种元素原子的核外电子数的差值可能为36
⑦同一周期的甲、乙两种元素,甲位于第ⅡA族,序数为x,乙位于第ⅢA族,则乙的序数可能为x+10
⑧砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀酸
⑨Na2O和Na2O2中阴阳离子个数比都是1:2
⑩卤素单质的熔点从F2到I2逐渐升高,碱金属单质的熔点从Li到Cs也逐渐升高
| A.③⑥⑧⑨ | B.①③④⑦⑨ | C.②⑤⑥⑨ | D.③⑥⑧⑩ |
您最近一年使用:0次
名校
解题方法
10 . 人类对原子结构的认识经历了一个漫长的、不断深化的过程,下列原子结构模型属于卢瑟福提出的核式原子模型的是
A. | B. | C. | D.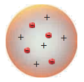 |
您最近一年使用:0次



