1 . 在标准状况下进行甲、乙、丙三组实验:三组各取30.0mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
合金中Mg、Al的物质的量之比为_____ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 产生气体体积/mL | 280 | 336 | 336 |
您最近一年使用:0次
2 . 下列关于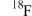 与
与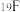 说法正确的是
说法正确的是
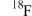 与
与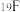 说法正确的是
说法正确的是| A.是同种核素 | B.是同素异形体 |
C.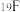 比 比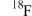 多一个电子 多一个电子 | D.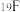 比 比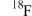 多一个中子 多一个中子 |
您最近一年使用:0次
解题方法
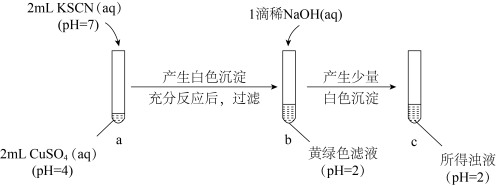
3 . 资料显示:由于CuI沉淀强烈吸附I2,故在接近滴定终点时必需加入适量的KSCN,释放出被吸附的I2。
已知:Cu2+可与SCN-反应生成 CuSCN(白色沉淀)和(SCN)2;(SCN)2的性质与Cl2相似,在水溶液中呈黄色,可与水、碱等发生反应。常温下,某同学对Cu2+与SCN-的反应进行探究:___________ ;分析往b中加入1滴浓NaOH溶液后,产生少量白色沉淀的化学原理___________ 。
已知:Cu2+可与SCN-反应生成 CuSCN(白色沉淀)和(SCN)2;(SCN)2的性质与Cl2相似,在水溶液中呈黄色,可与水、碱等发生反应。常温下,某同学对Cu2+与SCN-的反应进行探究:
您最近一年使用:0次
名校
解题方法
4 . 土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理为:
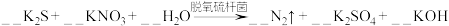 。
。
(1)配平上述反应方程式,并用单线桥标出电子转移的方向和数目___________ 。
(2)被氧化的元素是___________ 。
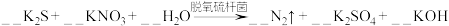 。
。(1)配平上述反应方程式,并用单线桥标出电子转移的方向和数目
(2)被氧化的元素是
您最近一年使用:0次
名校
5 . 元素周期表是指导我们系统学习化学的重要工具,下图是元素周期表的一部分。请回答以下问题:___________ 数相同,卤族元素处于同一纵行,是由于它们的___________ 数相同。
(2)碘元素在元素周期表中的位置是___________ ,它所在的周期共有___________ 种元素。
(3)根据同主族元素原子结构的相似性,可以推测磷元素气态氢化物的电子式为___________ 。
(4)某元素的原子L层电子数比K层电子数多 2个,与该元素同一主族的短周期元素是___________ (填元素符号)。
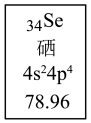
(5)硒元素在元素周期表中的具体信息如图所示,“78.96”的含义是___________ ,硒原子的结构示意图为___________ 。

(2)碘元素在元素周期表中的位置是
(3)根据同主族元素原子结构的相似性,可以推测磷元素气态氢化物的电子式为
(4)某元素的原子L层电子数比K层电子数多 2个,与该元素同一主族的短周期元素是
(5)硒元素在元素周期表中的具体信息如图所示,“78.96”的含义是
您最近一年使用:0次
名校
解题方法
6 . 硫化细菌是好氧菌,而反硫化细菌是厌氧菌,两类细菌参与了土壤中硫循环。___________ 剂(填“氧化”或“还原”)。
(2)“硫化细菌浸矿法”可将矿石中的CuS转化为可溶性铜盐,离子方程式是___________ 。
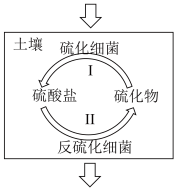
(2)“硫化细菌浸矿法”可将矿石中的CuS转化为可溶性铜盐,离子方程式是
您最近一年使用:0次
解题方法
7 . 某次高空探测,收集到含O3、O2、N2(其他气体忽略不计)的大气样本,在实验室中微热一段时间后,O3全部转化为O2(2O3=3O2),若气体总体积增加了0.36%,则大气样本中O3的体积分数为___________ (反应前后温度和压强均保持不变)。
您最近一年使用:0次
8 .  、
、 、
、 、
、 、
、 、
、 是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。 的焰色试验为黄色,且
的焰色试验为黄色,且 为化合物,回答下列问题:
为化合物,回答下列问题:
1. 与
与 反应的离子方程式为
反应的离子方程式为_______ 。
2.若 为强还原性的非金属单质,通常为黑色粉末,则
为强还原性的非金属单质,通常为黑色粉末,则 的电子式为
的电子式为_______ 。
3.若 为一种造成温室效应的气体,则鉴别等浓度的
为一种造成温室效应的气体,则鉴别等浓度的 、
、 溶液,可选择的试剂为_______。
溶液,可选择的试剂为_______。
4.若 为
为 ,则
,则 与
与 反应的化学方程式为
反应的化学方程式为_______ ,并写出 的一种用途
的一种用途_______ 。
若 为黄绿色气体单质,具有很强的氧化性。
为黄绿色气体单质,具有很强的氧化性。
5.组成物质 的元素在元素周期表中的位置是
的元素在元素周期表中的位置是_______ 。
6. 的水溶液放置一段时间后,溶液的酸性
的水溶液放置一段时间后,溶液的酸性_______ (填“增强”、“减弱”或“不变”)。
7.若 为强电解质,则
为强电解质,则 可能为_______。
可能为_______。
8.请写出 与冷的石灰乳反应的化学方程式:
与冷的石灰乳反应的化学方程式:_______ 。
 、
、 、
、 、
、 、
、 、
、 是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。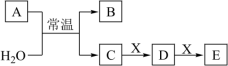
 的焰色试验为黄色,且
的焰色试验为黄色,且 为化合物,回答下列问题:
为化合物,回答下列问题:1.
 与
与 反应的离子方程式为
反应的离子方程式为2.若
 为强还原性的非金属单质,通常为黑色粉末,则
为强还原性的非金属单质,通常为黑色粉末,则 的电子式为
的电子式为3.若
 为一种造成温室效应的气体,则鉴别等浓度的
为一种造成温室效应的气体,则鉴别等浓度的 、
、 溶液,可选择的试剂为_______。
溶液,可选择的试剂为_______。| A.酚酞溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
 为
为 ,则
,则 与
与 反应的化学方程式为
反应的化学方程式为 的一种用途
的一种用途若
 为黄绿色气体单质,具有很强的氧化性。
为黄绿色气体单质,具有很强的氧化性。5.组成物质
 的元素在元素周期表中的位置是
的元素在元素周期表中的位置是6.
 的水溶液放置一段时间后,溶液的酸性
的水溶液放置一段时间后,溶液的酸性7.若
 为强电解质,则
为强电解质,则 可能为_______。
可能为_______。A. | B. | C. | D. |
 与冷的石灰乳反应的化学方程式:
与冷的石灰乳反应的化学方程式:
您最近一年使用:0次
名校
解题方法
9 . 同周期的 A族和
A族和 A族的元素原子序数不可能相差
A族的元素原子序数不可能相差
 A族和
A族和 A族的元素原子序数不可能相差
A族的元素原子序数不可能相差| A.2 | B.12 | C.17 | D.26 |
您最近一年使用:0次
10 . 原子最外层有2个电子的元素不可能位于元素周期表的
A. A族 A族 | B.第15族 | C.副族 | D.0族 |
您最近一年使用:0次



