名校
1 . 下列实验过程可以达到实验目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 配制0.4mol/L的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至500mL容量瓶中定容 |
| B | 探究H2O2的还原性 | 向盛有2 mL酸性高锰酸钾溶液的试管中滴加H2O2溶液,观察颜色变化 |
| C | 制取干燥纯净的氢气 | 向稀盐酸中加入锌粒,将生成的气体依次通过浓硫酸、NaOH溶液,然后收集 |
| D | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和氯化铁溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 制备 | 向饱和食盐水中通入 后,再通 后,再通 |
| B | 配制1 L 1.0 mol/L NaCl溶液 | 将58.5 g NaCl固体直接溶于1 L水中 |
| C | 鉴别 和 和 | 取样,加入澄清石灰水,若有白色沉淀生成,则为 |
| D | 检验NaOH中的阳离子 | 用洁净的铂丝蘸取待测液,在酒精灯火焰上灼烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 如图所示装置的实验中,能达到实验目的的是
| 选项 | A | B | C | D |
| 实验装置 | 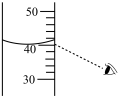 | 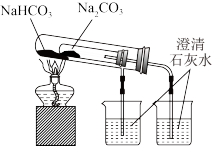 | 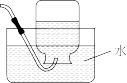 | 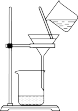 |
| 实验目的 | 配制氯化钠溶液时量取水的体积 | 比较 、 、 的稳定性 的稳定性 | 排水法收集NO | 分离氯化铁溶液和氢氧化铁胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . I.氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂;某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气;并模拟工业制漂白粉。请回答下列问题:
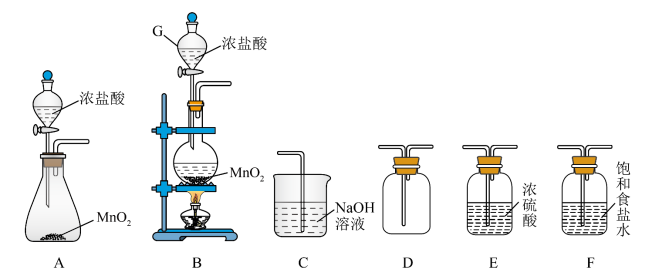
(1)装置G的名称为___________ 。
(2)图中制氯气的化学方程式___________ 。
(3)从图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用);仪器连接顺序为(用仪器下方字母表示:如A→B→…)___________ 。
II.漂白粉的制备
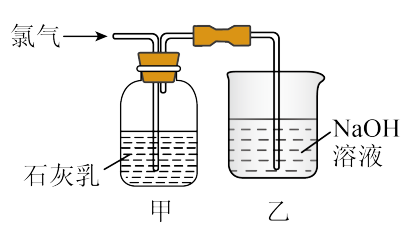
已知:①氯气和石灰乳在反应的过程中会放出热量
②加热条件下氯气与碱会发生歧化反应生成氯酸盐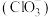
(4)写出制取漂白粉的化学方程式___________ 。
(5)兴趣小组制得的漂白粉中 的含量远超过预期;而
的含量远超过预期;而 含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)
含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)___________ 。
(6)为提高产品中有效成分 的含量;在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)
的含量;在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)___________ 。
(7)本实验使用的浓盐酸试剂瓶标签上的有关数据如下图。
①该浓盐酸中HCl的物质的量浓度为___________ 。
②若用该浓盐酸和蒸馏水配制500mL0.400mol/L的稀盐酸,需要量取_______ mL上述浓盐酸进行配制。

(1)装置G的名称为
(2)图中制氯气的化学方程式
(3)从图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用);仪器连接顺序为(用仪器下方字母表示:如A→B→…)
II.漂白粉的制备

已知:①氯气和石灰乳在反应的过程中会放出热量
②加热条件下氯气与碱会发生歧化反应生成氯酸盐
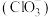
(4)写出制取漂白粉的化学方程式
(5)兴趣小组制得的漂白粉中
 的含量远超过预期;而
的含量远超过预期;而 含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)
含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)(6)为提高产品中有效成分
 的含量;在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)
的含量;在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)(7)本实验使用的浓盐酸试剂瓶标签上的有关数据如下图。
| 盐酸 分子式:HCl 相对分子质量:36.5 密度: 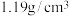 HCl的质量分数:36.5% 体积:500nL |
②若用该浓盐酸和蒸馏水配制500mL0.400mol/L的稀盐酸,需要量取
您最近一年使用:0次
名校
5 . NaClO2是一种高效的氧化剂和优质漂白剂,在水中溶解度较大,遇酸放出ClO2,某探究小组制备NaClO2所需装置如图所示(夹持装置略):

已知:①2ClO2+H2O2+2NaOH = 2NaClO2+O2+2H2O;
②ClO2气体极易溶于水,但不与水反应,可与碱溶液反应;纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
回答下列问题:
(1)完成该实验需要450 mL 4 mol·L-1的NaOH溶液,配制该溶液需要的玻璃仪器除烧杯、胶头滴管和量筒外,还需要_______ ,所需NaOH固体的质量为_______ 。
(2)仪器A的名称是_______ ,装置连接顺序为_______ (按气流方向,用小写字母表示,每个装置仅使用一次)。
(3)装置④中发生反应的化学方程式为_______ 。
(4)②中NaOH溶液的作用是_______ ;打开K通入足量空气的目的是_______ 。
(5)ClO2作消毒剂后转化为Cl-,则其消毒效率(以单位物质的量得到的电子数表示)是Cl2的_______ 倍。

已知:①2ClO2+H2O2+2NaOH = 2NaClO2+O2+2H2O;
②ClO2气体极易溶于水,但不与水反应,可与碱溶液反应;纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
回答下列问题:
(1)完成该实验需要450 mL 4 mol·L-1的NaOH溶液,配制该溶液需要的玻璃仪器除烧杯、胶头滴管和量筒外,还需要
(2)仪器A的名称是
(3)装置④中发生反应的化学方程式为
(4)②中NaOH溶液的作用是
(5)ClO2作消毒剂后转化为Cl-,则其消毒效率(以单位物质的量得到的电子数表示)是Cl2的
您最近一年使用:0次
2023-05-16更新
|
408次组卷
|
2卷引用:山东省烟台市2022-2023学年高一上学期期末考试化学试题



