名校
解题方法
1 . 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为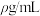 ,质量分数为
,质量分数为 ,物质浓度为c mol/L,则下列关系中正确的是
,物质浓度为c mol/L,则下列关系中正确的是
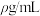 ,质量分数为
,质量分数为 ,物质浓度为c mol/L,则下列关系中正确的是
,物质浓度为c mol/L,则下列关系中正确的是A.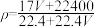 |
B.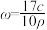 |
C.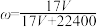 |
D. |
您最近一年使用:0次
2022-10-25更新
|
643次组卷
|
2卷引用:山东省青岛第五十八中学2022-2023学年高一上学期10月月考化学试题
名校
解题方法
2 . 环境问题是广大群众关注的热点话题之一,化工厂排放的废水、废渣一般利用化学原理可以进行排放物达标检测与无害化处理。某皮革厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:
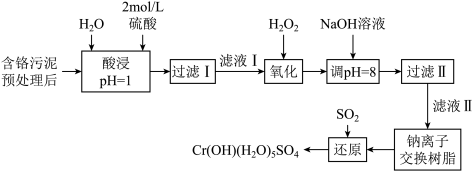
已知:①酸浸后的溶液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)如需配制480 mL酸浸环节所需的硫酸,需要用量筒量取18.4 mol·L-1的浓硫酸___________ mL;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需哪些仪器___________
(2)经氧化环节滤液Ⅰ中的Cr3+转化为Cr2O ,写出此反应的离子方程式:
,写出此反应的离子方程式:___________
(3)调pH=8环节,既可以将溶液中某些杂质离子转化为沉淀,同时又可以将Cr2O 转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因
转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因___________
(4)钠离子交换树脂的反应原理为Mn++nNaR MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有___________
(5)请写出流程中用SO2进行还原时发生反应的离子方程式:___________

已知:①酸浸后的溶液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 沉淀完全时的pH | 3.7 | 11.1 | 5.4 | 9 |
| 沉淀溶解时的pH | — | — | >8溶解 | >9溶解 |
(2)经氧化环节滤液Ⅰ中的Cr3+转化为Cr2O
 ,写出此反应的离子方程式:
,写出此反应的离子方程式:(3)调pH=8环节,既可以将溶液中某些杂质离子转化为沉淀,同时又可以将Cr2O
 转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因
转化为某种含铬元素微粒,溶液颜色由橙色变为黄色,请结合离子反应方程式解释该颜色变化的原因(4)钠离子交换树脂的反应原理为Mn++nNaR
 MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有
MRn+nNa+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有(5)请写出流程中用SO2进行还原时发生反应的离子方程式:
您最近一年使用:0次
名校
3 . 下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法正确的是


| A.该硫酸的物质的量浓度为9.2 mol·L-1 |
| B.1 mol Zn与足量的该硫酸反应,标准状况下产生22.4 L气体时,转移的电子数为NA |
| C.配制200 mL 4.6 mol·L-1的稀硫酸需取该硫酸50 mL |
| D.该硫酸与等体积的水混合后所得溶液的物质的量浓度等于9.2 mol·L-1 |
您最近一年使用:0次
名校
4 . 按照下列操作配出的溶液,物质的量浓度是1mol/L的是
| A.将53gNa2CO3溶于水配成500mL溶液 | B.将40g氢氧化钠溶于1L水中 |
| C.将1L10mol/L的NaCl溶液溶于9L水中 | D.将22.4LHCl溶于水配成1L溶液 |
您最近一年使用:0次
名校
5 . 向100g密度为1.84g/mL质量分数为98%的浓硫酸中加入一定体积的水稀释成9.2mol/L的硫酸,则加入水的体积( )
| A.>100mL | B.=100mL | C.< 100mL | D.无法确定 |
您最近一年使用:0次
名校
6 . 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法正确的是


| A.该硫酸的物质的量浓度为9.2mol·L-1 |
| B.该硫酸与等体积的水混合所得溶液的质量分数小于49% |
| C.配制200mL4.6mol·L-1的稀硫酸需取该硫酸50.0mL |
| D.该硫酸50.0mL与足量的铜反应可得到标准状况下SO2气体10.304L |
您最近一年使用:0次
2019-09-11更新
|
613次组卷
|
2卷引用:内蒙古鄂尔多斯市第一中学2020届高三9月月考化学试题
11-12高一上·陕西西安·期中
名校
解题方法
7 . 有下列化学仪器:①托盘天平;②玻璃棒;③药匙;④烧杯;⑤量筒;⑥容量瓶;⑦胶头滴管。
(1)现需要配制500 mL 1 mol/L硫酸溶液,需用质量分数为98%、密度为1.84 g/cm3的浓硫酸________ mL。
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是_______ 。
(3)容量瓶使用前检验漏水的方法是_______ 。
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)
①未经冷却趁热将溶液注入容量瓶中,_______________ ;
②摇匀后发现液面低于刻度线再加水,_____________ ;
③容量瓶中原有少量蒸馏水,_______________ ;
④定容时观察液面俯视,_____________ ;
⑤未将洗涤液注入容量瓶中,_______________ 。
(1)现需要配制500 mL 1 mol/L硫酸溶液,需用质量分数为98%、密度为1.84 g/cm3的浓硫酸
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是
(3)容量瓶使用前检验漏水的方法是
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)
①未经冷却趁热将溶液注入容量瓶中,
②摇匀后发现液面低于刻度线再加水,
③容量瓶中原有少量蒸馏水,
④定容时观察液面俯视,
⑤未将洗涤液注入容量瓶中,
您最近一年使用:0次
2020-02-01更新
|
415次组卷
|
4卷引用:2011-2012学年陕西省长安一中高一上学期期中考试化学试卷
(已下线)2011-2012学年陕西省长安一中高一上学期期中考试化学试卷云南省楚雄市紫溪中学2018-2019学年高一上学期期中考试化学试题湖北省荆州市沙市区沙市中学2019-2020学年高一化学过关训练9《化学计量在实验中的应用》云南省昭通市昭阳区第一中学2020-2021学年高一上学期期中考试化学试题
名校
8 . 下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500mL的操作,请按要求填空:
(1)所需浓H2SO4的体积为__________ (用下一小题的仪器量取)。
(2)如果实验室有15mL、20mL、50mL量筒,应选用_______ mL量筒最好。
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的烧杯里,并不断搅拌。
(4)将冷却至室温的上述溶液沿__________ 注入____________ 中,并用50mL蒸馏水洗涤烧杯2~3次,洗涤液要注入上述仪器中,并摇匀。
(5)加水至距刻度___________ 时,改用胶头滴管加水,使溶液的凹液面正好跟刻度相平。
(6)误差分析:请用“偏高 ”“偏低 ”或“无影响 ”进行填空
① 定容时,观察液面俯视:_____________ 。
② 摇匀后,液面低于刻度线,没有再加水:_____________ 。
③ 取浓H2SO4时,倒出浓H2SO4后的量筒中还残留少量液体未处理:_____________ 。
(1)所需浓H2SO4的体积为
(2)如果实验室有15mL、20mL、50mL量筒,应选用
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的烧杯里,并不断搅拌。
(4)将冷却至室温的上述溶液沿
(5)加水至距刻度
(6)误差分析:请用“
① 定容时,观察液面俯视:
② 摇匀后,液面低于刻度线,没有再加水:
③ 取浓H2SO4时,倒出浓H2SO4后的量筒中还残留少量液体未处理:
您最近一年使用:0次
2017-11-08更新
|
265次组卷
|
2卷引用:新疆呼图壁县一中2017-2018学年高一上学期期中考试化学试卷



