名校
1 . 下列反应的离子方程式正确的是
A.少量 通入 通入 中: 中: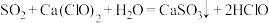 |
B.向二元弱酸 溶液中滴入足量烧碱溶液: 溶液中滴入足量烧碱溶液: |
C. 溶于HI溶液: 溶于HI溶液: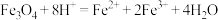 |
D.向含 的溶液通入标准状况下 的溶液通入标准状况下 : : |
您最近一年使用:0次
2 . 部分含铁物质的分类与相应铁元素的化合价关系如图。下列说法不正确的是
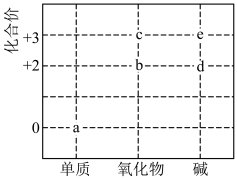
| A.b可被还原为a | B.d在空气中可被还原为e |
| C.一定条件下a能与水蒸气反应 | D.c溶于盐酸后所得溶液能使KSCN溶液变红 |
您最近一年使用:0次
3 . 下列说法不正确的是
| A.铁元素在自然界中以化合态和游离态形式存在 |
B. 中铁的化合价有 中铁的化合价有 和 和 价,是一种混合物 价,是一种混合物 |
C.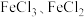 和 和 都可以通过化合反应制取 都可以通过化合反应制取 |
D. 铁与足量稀盐酸反应,转移电子数为 铁与足量稀盐酸反应,转移电子数为 |
您最近一年使用:0次
4 . 下图是一种综合处理SO2废气的工艺流程。下列说法正确的是
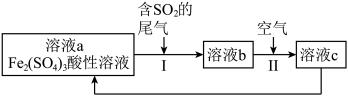
| A.操作Ⅱ发生反应的离子方程式为:2Fe2++4H++O2=2Fe3++2H2O |
| B.溶液b中阳离子只有Fe2+ |
| C.溶液a转化为溶液b的反应中,SO2被氧化 |
| D.加入FeO可以使溶液c转化为溶液a |
您最近一年使用:0次
5 . 某实验小组探究Fe2+与H2O2反应中滴加KSCN溶液变红色后又褪色的原因,提出如下假设:
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
| 实验 | 滴加试剂 | 现象 |
| I | i.向2mLFeCl2溶液中滴加2滴0.1mol·L-1KSCN溶液 ii.再滴加5滴5%H2O2溶液(物质的量浓度约为1.5mol·L-1、pH约为5) | i.无明显现象 ii.溶液变红,大约10秒左右红色褪去,并测得生成了两种可直接排放到空气中的气体 |
| II | iii.取褪色后溶液两份,一份滴加FeC13溶液;另一份滴加KSCN溶液 iV.取褪色后溶液,滴加盐酸和BaCl2溶液 | iii.一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色 iV.产生白色沉淀 |
| III | V.向2mL0.1mol·L-1FeCl3溶液中滴加2滴0.1mol·L-1KSCN溶液,观察现象;后通入O2,观察现象 | V.先变红,通入氧气后无明显变化 |
| A.实验I褪色后的溶液中n(H+)变小 | B.通过实验II、III可验证假设c正确 |
C.实验II证明SCN-被氧化成SO | D.实验III的目的是排除假设b |
您最近一年使用:0次
解题方法
6 . 电子工业常用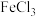 溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含
溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含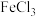 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得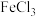 溶液,处理流程如下:
溶液,处理流程如下:
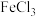 溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含
溶液腐蚀覆铜板上的铜箔,制造印刷电路板。从腐蚀废液(主要含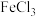 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得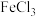 溶液,处理流程如下:
溶液,处理流程如下: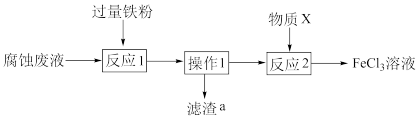
A. 溶液腐蚀铜箔的原理为 溶液腐蚀铜箔的原理为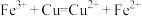 |
| B.反应1和反应2都发生了氧化还原反应 |
| C.实验室中进行操作1时,用到的主要玻璃仪器有漏斗、烧杯和玻璃棒 |
| D.滤渣a的主要成分是Cu和Fe,物质X可以选用氯气 |
您最近一年使用:0次
7 . 下列离子方程式正确的是
A.过氧化钠和稀盐酸反应: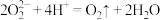 |
B.将 通入含 通入含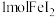 的溶液中: 的溶液中: |
C.向饱和碳酸钠溶液中通入足量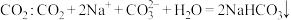 |
D.工业上制备漂白粉的离子方程式: |
您最近一年使用:0次
解题方法
8 . 下列各组离子能在溶液中大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
解题方法
9 . 部分含铁微粒所带的电荷数与其中铁元素化合价的关系如图所示。下列推断不合理的是

| A.含R的合金是用量最大、用途最广的合金 |
B.高温条件下,红热的 与水蒸气反应生成 与水蒸气反应生成 |
C.可用 溶液检验溶液中 溶液检验溶液中 是否被氧化 是否被氧化 |
D.根据 中铁元素的价态,可判断 中铁元素的价态,可判断 具有氧化性 具有氧化性 |
您最近一年使用:0次
10 . 化学与生活紧密相关,下列有关说法不正确的是
| A.重庆素有雾都之称,雾是一种气溶胶,光束透过大雾可观察到丁达尔效应 |
| B.生铁的含碳量比钢的含碳量高,合金的熔点一般比其成分金属的熔点高 |
C. 作补血剂时可与维生索 作补血剂时可与维生索 同时服用 同时服用 |
| D.漂白粉可用于漂白棉、麻、纸张等,其长期露置在空气中会失效 |
您最近一年使用:0次



