名校
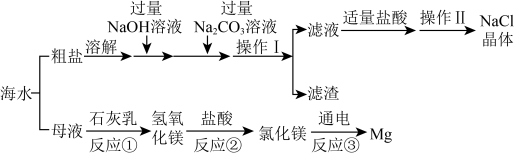
1 . 海洋是一个巨大的资源宝库。海水资源综合利用的部分途径如下图:
已知:粗盐中的杂质有泥沙、 、
、 ,流程中部分操作及试剂已省略。
,流程中部分操作及试剂已省略。
(1)“操作I”中玻璃棒的作用是_______ 。
(2)滤渣中除泥沙外还有_______ (填化学式)。
(3)反应①和③的化学反应方程式分别为_______ ;_______ 。
(4)海水中本身就有氯化镁,请分析反应①、②转化过程的目的_______ 。
(5)根据图中KNO3、NaCl的溶解度曲线,下列说法不正确的是_______ (填字母)。
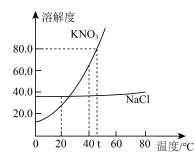
A.t℃时,将45g KNO3固体放入50g水中充分溶解,所得溶液的质量为95g
B.NaCl溶液中含有少量KNO3,可以采用蒸发结晶的方法提纯NaCl
C.40℃时,将KNO3的饱和溶液降温至20℃,溶液的溶质质量分数减小(不考虑水分损失)
(6)同学们查阅NaCl的溶解度曲线后,欲配制20℃时100g溶质质量分数为10%的NaCl溶液。已知配制溶液的步骤有:①溶解 ②计算 ③装瓶存放 ④称量。上述步骤的正确顺序为_______ (填序号)。

已知:粗盐中的杂质有泥沙、
 、
、 ,流程中部分操作及试剂已省略。
,流程中部分操作及试剂已省略。(1)“操作I”中玻璃棒的作用是
(2)滤渣中除泥沙外还有
(3)反应①和③的化学反应方程式分别为
(4)海水中本身就有氯化镁,请分析反应①、②转化过程的目的
(5)根据图中KNO3、NaCl的溶解度曲线,下列说法不正确的是

A.t℃时,将45g KNO3固体放入50g水中充分溶解,所得溶液的质量为95g
B.NaCl溶液中含有少量KNO3,可以采用蒸发结晶的方法提纯NaCl
C.40℃时,将KNO3的饱和溶液降温至20℃,溶液的溶质质量分数减小(不考虑水分损失)
(6)同学们查阅NaCl的溶解度曲线后,欲配制20℃时100g溶质质量分数为10%的NaCl溶液。已知配制溶液的步骤有:①溶解 ②计算 ③装瓶存放 ④称量。上述步骤的正确顺序为
您最近一年使用:0次
2 . 工业上用“碳捕捉”技术将CO和 混合气体中的
混合气体中的 捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):
捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):
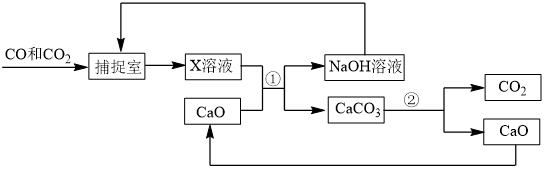
(1)反应②分离出的 可制成干冰,干冰常用于
可制成干冰,干冰常用于___________ 。
(2)反应①在“反应分离室”内进行,涉及到的化学反应方程式为:___________ 、___________ ;将NaOH溶液和 分离,得到纯净的
分离,得到纯净的 的操作是
的操作是___________ 。
(3)下列有关该捕捉过程的叙述正确的有___________;(填序号)
(4) 过量排放对环境影响很大,发展“低碳经济”是全社会的共识。下列说法错误的是___________;(填序号)
过量排放对环境影响很大,发展“低碳经济”是全社会的共识。下列说法错误的是___________;(填序号)
 混合气体中的
混合气体中的 捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):
捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):
(1)反应②分离出的
 可制成干冰,干冰常用于
可制成干冰,干冰常用于(2)反应①在“反应分离室”内进行,涉及到的化学反应方程式为:
 分离,得到纯净的
分离,得到纯净的 的操作是
的操作是(3)下列有关该捕捉过程的叙述正确的有___________;(填序号)
A.捕捉到的 可用于制备其他化工产品,减少了温室气体的排放 可用于制备其他化工产品,减少了温室气体的排放 |
| B.“反应分离室”中的反应要吸收大量热 |
| C.整个过程中只有一种物质可循环利用 |
| D.能耗大是该捕捉技术的一大缺点 |
 过量排放对环境影响很大,发展“低碳经济”是全社会的共识。下列说法错误的是___________;(填序号)
过量排放对环境影响很大,发展“低碳经济”是全社会的共识。下列说法错误的是___________;(填序号)A. 大量排放导致酸雨 大量排放导致酸雨 |
B.将 转变为稳定的碳酸盐,可实现 转变为稳定的碳酸盐,可实现 的长期封存 的长期封存 |
C.利用 合成聚碳酸酯类可降解塑料,可实现“碳”的循环利用 合成聚碳酸酯类可降解塑料,可实现“碳”的循环利用 |
D.利用化学试剂吸收 可实现“碳捕捉” 可实现“碳捕捉” |
您最近一年使用:0次



