1 . 亚硫酸的性质
(1)弱酸性:___________ (电离方程式)。
(2)不稳定性:___________ 。
(3)强还原性(与O2、H2O2反应):___________ 。
(4)弱氧化性(与H2S反应):___________ 。
(1)弱酸性:
(2)不稳定性:
(3)强还原性(与O2、H2O2反应):
(4)弱氧化性(与H2S反应):
您最近半年使用:0次
2 . 亚硫酸钠中+4价的硫既有氧化性又有还原性。现有试剂:氯水、硫化钠溶液、亚硫酸钠溶液、稀硫酸、氢氧化钠溶液。
(1)要证明亚硫酸溶液具有还原性,应选用什么试剂____ ?会观察到什么现象____ ?写出反应的离子方程式____ 。
(2)要证明亚硫酸钠溶液具有氧化性,应选用什么试剂____ ?会观察到什么现象____ ?写出反应的离子方程式____ 。
(3)如何通过实验证明亚硫酸钠已被氧化____ ?
(1)要证明亚硫酸溶液具有还原性,应选用什么试剂
(2)要证明亚硫酸钠溶液具有氧化性,应选用什么试剂
(3)如何通过实验证明亚硫酸钠已被氧化
您最近半年使用:0次
3 . 当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态,即台阶式升降,可用如图表示。

(1)H2S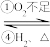 S
S SO2
SO2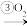 SO3
SO3
写出③④⑤的化学方程式(选考):
③____ 。
④____ 。
⑤____ 。
(2)Na2S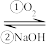 S
S Na2SO3
Na2SO3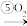 Na2SO4
Na2SO4
写出①②⑤的化学方程式(选考):
①____ 。
②____ 。
⑤____ 。

(1)H2S
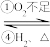 S
S SO2
SO2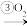 SO3
SO3写出③④⑤的化学方程式(选考):
③
④
⑤
(2)Na2S
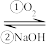 S
S Na2SO3
Na2SO3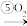 Na2SO4
Na2SO4写出①②⑤的化学方程式(选考):
①
②
⑤
您最近半年使用:0次
解题方法
4 . 实验室洗涤试管壁上附着的硫单质,常用两种方法。
(1)物理方法:用CS2洗涤,利用单质硫的性质为____ 。
(2)化学方法:用热的NaOH溶液洗涤,该反应原理为3S+6NaOH 2Na2S+Na2SO3+3H2O,在该反应中,硫单质表现
2Na2S+Na2SO3+3H2O,在该反应中,硫单质表现____ 性和____ 性,氧化剂和还原剂的物质的量之比为____ ,写出上述反应的离子方程式:____ 。
(3)向上述反应的溶液中再加入适量的稀H2SO4,会产生淡黄色沉淀,写出该反应的离子方程式:____ 。
(1)物理方法:用CS2洗涤,利用单质硫的性质为
(2)化学方法:用热的NaOH溶液洗涤,该反应原理为3S+6NaOH
 2Na2S+Na2SO3+3H2O,在该反应中,硫单质表现
2Na2S+Na2SO3+3H2O,在该反应中,硫单质表现(3)向上述反应的溶液中再加入适量的稀H2SO4,会产生淡黄色沉淀,写出该反应的离子方程式:
您最近半年使用:0次



