2023高三·全国·专题练习
1 . 已知Na2SO3具有强还原性,能够被Cl2氧化。某化工厂排出的废水中含0.014mol·L-1 Cl2、0.001mol·L-1 H+,废水排出的速度为10.0mL·s-1,为了除去此废水中的游离氯分子,并使废水变为中性,有人提出如下建议:在废水排出管A和B处分别注入一定流量的Na2SO3溶液(0.10mol·L-1)和烧碱溶液(0.10mol·L-1)。下列说法错误的是
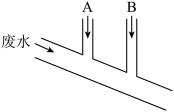

A.排出管A处发生的反应为 +Cl2+H2O= +Cl2+H2O= +2Cl-+2H+ +2Cl-+2H+ |
| B.废水排出管B处发生的反应为Cl2+2OH-=Cl-+ClO-+H2O |
| C.A处溶液的流量为1.4mL·s-1 |
| D.B处溶液的流量为2.8mL·s-1 |
您最近一年使用:0次
名校
解题方法
2 . 2021年7月我国科研人员报道了利用高铁Fe(VI) (实际物质为 在碱性溶液中稳定,在酸性溶液中分解)降解废水的电子转移过程如下(
在碱性溶液中稳定,在酸性溶液中分解)降解废水的电子转移过程如下(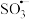 、
、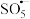 表示自由基,其中一个O原子上含有一个单电子):
表示自由基,其中一个O原子上含有一个单电子):
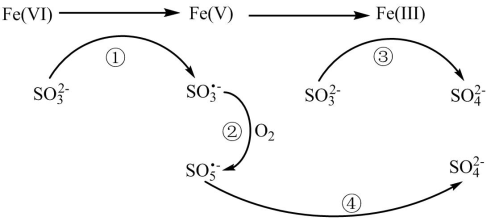
下列说法不正确的是
 在碱性溶液中稳定,在酸性溶液中分解)降解废水的电子转移过程如下(
在碱性溶液中稳定,在酸性溶液中分解)降解废水的电子转移过程如下(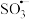 、
、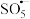 表示自由基,其中一个O原子上含有一个单电子):
表示自由基,其中一个O原子上含有一个单电子):
下列说法不正确的是
A. 在酸性溶液中分解产生的氧化产物与还有产物物质的量之比为4:3 在酸性溶液中分解产生的氧化产物与还有产物物质的量之比为4:3 |
B.过程①中 与 与 反应的物质的量之比为1:1 反应的物质的量之比为1:1 |
C.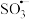 中硫的化合价为+5, 中硫的化合价为+5,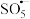 中硫的化合价为+9 中硫的化合价为+9 |
D.过程④中Fe(V)与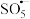 反应生成 反应生成 与 与 |
您最近一年使用:0次



